Radioaktivní isotopy pro výzkum, medicínu, technologie
1.
Jaderná a radiační fyzika
1.0. Fyzika - fundamentální
přírodní věda
1.1. Atomy a
atomová jádra
1.2. Radioaktivita
1.3. Jaderné
reakce
1.4.
Radionuklidy
1.5. Elementární
částice
1.6. Ionizující
záření
1.4.
Radionuklidy
V této kapitole si přiblížíme
vznik a vlastnosti
nejdůležitějších radionuklidů -
důležitých buď z hlediska fyzikálního či obecně
přírodovědeckého, nebo radionuklidů používaných v
různých oblastech vědy a techniky včetně medicíny, v
průmyslových aplikacích, radionuklidů vyskytujících se v
životním prostředí a pod.
Mendělejova periodická tabulka obsahuje 118 nyní známých
prvků. Radionuklidů je však podstatně větší počet než
stabilních nuklidů, celkem je jich známo přes 2000. V rámci
jediného prvku je obvykle zastoupeno několik
radioisotopů, někdy i deset a více.
Přírodní radionuklidy
Kromě stabilních chemických prvků se v přírodním
prostředí vyskytují ve velmi nízkých koncentracích i radioaktivní
prvky přírodního původu. Tyto přírodní
radionuklidy můžeme rozdělit do tří kategorií podle svého
původu a vzniku :
Primární (primordiální)
radionuklidy ([pra]původní,
fosilní)
Jsou to radionuklidy, které vznikaly spolu s
ostatními (stabilními) jádry těžších prvků při
kosmické nukleogenezi termonukleárními
reakcemi v nitrech hvězd (jak
bylo zmíněno v §1.1. v odstavci "Kosmická
alchymie" - "jsme potomky hvězd!"), které pak vybuchly jako supernovy a obohatily
o tyto prvky zárodečný oblak, z něhož vzniklo naše
Slunce a sluneční soustava. Součástí Země se tak
staly již při formování Sluneční soustavy před cca
4-5 miliardami let, Země si je přinesla z
vesmíru. Do dnešní doby se ovšem zachovaly
pouze ty radionuklidy, které mají velmi dlouhý
poločas rozpadu - větší než cca 108roků.
Pozn.: Některé
primární radionuklidy mají m.j. geologický
význam. Teplo uvolňované radioaktivním
rozpadem přírodních radionuklidů,
uranu 235,238U, thoria 232Th a draslíku 40K, je patrně důležitým zdrojem geotermální
energie, zahřívající nitro Země (viz níže "Geologický
význam přírodní radioaktivity").
Nejrozšířenějším primárním
radionuklidem v pozemské přírodě je draslík 40K, jehož průměrný obsah v
zemské kůře je asi 3.10-3 %. Draslík 40 se s poločasem T1/2 = 1,27.109roků rozpadá
beta--radioaktivitou na argon 40Ar (89%) a elektronovým záchytem na vápník 40Ca (11%) - viz níže "Draslík - 40-K"; oba tyto
dceřinné isotopy jsou stabilní, další rozpad již
nepokračuje.
Dalším všeobecně rozšířeným přírodním
primárním radionuklidem je thorium 232Th (koncentrace
v zemské kůře cca 8-12.10-6), které se s poločasem
T1/2 =
1,39.1010roků rozpadá alfa-radioaktivitou (v kombinaci s beta)
postupně na řadu radionuklidů tzv. thoriové řady
(obr.1.4.1 vlevo).
Nejvýznamnějšími přírodními
radionuklidy tohoto primordiálního původu v zemské
kůře jsou však uran 238U (průměrná koncentrace v
zemské kůře cca 2-4.10-6, T1/2 = 4,51.109roků), a uran 235U (koncentrace cca 2-3.10-8, T1/2 = 7,1.108roků). Oba
tyto izotopy uranu se alfa-rozpadem (v
kombinaci s beta) přeměňují
postupně na řadu radionuklidů obou uranových
rozpadových řad - obr.1.4.1 uprostřed a vpravo, je
popsáno níže.
Pozn.: Prvek uran,
poprve v čisté formě izolovaný v r.1841, dostal svůj
název podle tehdy nově objevené planety Uran
(ta zase byla pojmenována podle boha Urana v antické
řecké mytologii). Je to těžký stříbřitý kov
(hustota 19g/cm3), na vzduchu oxidující tmavě šedým
povlakem. Používal se k barvení skla. V přírodní
uranové rudě byla H.Becquerelem v r.1896 poprve
objevena radioaktivita. Pro svou vysokou hustotu se 238U
("ochuzený uran") používá i pro některé
"nejaderné" aplikace (např. projektily s
vysokou průbojností, pro stínění a pod.). Hlavní
využití má však uran v jaderné technice
jako štěpný materiál - viz §1.3
"Jaderné reakce", především část "Štěpení atomových jader".
V malých stopových
množstvích se v přírodě vyskytují i další
primordiální radionuklidy s dlouhými poločasy
rozpadu: chlór 36Cl (T1/2=3.105let), berylium 10Be (T1/2=1,52.106let), lutetium 176Lu (T1/2=3,8.1010let), rhenium 187Re (T1/2=4,16.1010let), rubidium 87Rb (T1/2=4,88.1010let), samarium 147Sm (T1/2=1,06.1011let), .... Některé z nich se používají pro
radiometrické datování hornin (viz
níže "Radioisotopové
datování").
Pozn.:
Bezvýznamné z radiačního
hlediska jsou některé isotopy s extrémně
dlouhým poločasem rozpadu (pohybujícím se
většinou mezi 1014 až 1018 let), jejichž radioaktivita není často ani
bezpečně prokázána - např. 48Ca, 64,70Zn, 76Ge, 82Se, 92,100Mo, 116Cd, 124Sn, 123Sb, 136,142Ce, 144,145,150Nd, 147-149Sm, 152Gd, 156Dy, 165Ho, 180,182,183,186W, 192Os, 190,192,198Pt, 196Hg, 209Bi.
 |
Obr.1.4.1. Přírodní
rozpadové řady thoria 232Th a uranu 235U a 238U.
Neptuniová rozpadová řada je zobrazena
níže v pasáži "Aktinium 225Ac", na schématu vlevo nahoře.
Omluva:...obrázek je
nedokončen! -přijdou doplnit poločasy, energie
+ grafická úprava...... |
Druhotné (sekundární)
radionuklidy -
rozpadové produkty primárních radionuklidů
Rozpadem těžkých primárních radionuklidů
průběžně vzniká celá řada druhotných
radionuklidů. Přírodní radionuklidy 232Th, 238U a 235U se
přeměňují (alfa a později i beta rozpadem) na
jádra, která jsou také radioaktivní, stejně jako
jejich další a další přeměnové produkty.
Říkáme, že tyto radionuklidy vytvářejí radioaktivní
rozpadové řady - řetězce (decay chain),
kde jednotlivé dceřinné produkty vykazují alfa i beta
radioaktivitu a excitovaná jádra emitují záření
gama. V těchto rozpadových řadách je ustavena tzv. sekulární
radioaktivní rovnováha (viz §1.2 "Radioaktivita").
V terminologii pasáže "Stabilita a nestabilita
jader" §1.2
"Radioaktivita" lze říci, že těžké
nuklidy thoria a uranu "skákají" dolů po
energetických stupních a "valí" se do
údolí stability, až dosáhnou rovnovážné
konfigurace olova či vizmutu.
Radioaktivní
rozpadové řady
V přírodě se vyskytují tři radioaktivní rozpadové
řady (obr.1.4.1): rozpadová řada thoria 232Th (vlevo), rozpadová řada uranu 238U (uran-radiová řada
- její součástí je radium 226Ra - na obr. vpravo) a rozpadová řada uranu 235U (uprostřed) zvaná uran-aktiniová řada *).
Uměle lze získat rozpadovou řadu neptuniovou 237Np (je
zobrazena níže v pasáži "Aktinium
225Ac",
na obrázku vlevo nahoře).
*) Součástí rozpadové řady
uranu-235 je aktinium 227Ac. 235U se ve starší literatuře často nazýval aktinouran
a jeho rozpadová řada aktiniová.
Tyto rozpadové řetězce těžkých jader jsou si do
určité míry podobné :
¨ Primární mateřské
nuklidy mají velmi dlouhé poločasy rozpadu
- miliony až miliardy let. V důsledku toho se v
rozpadových řadách ustavuje trvalá (dlouhodobá) tzv.
sekulární radioaktivní rovnováha *) (viz §1.2, část "Obecné zákonitosti
přeměny atomových jader").
*) Přesněji řečeno, tak by tomu
bylo u hermeticky uzavřených
preparátů. V přírodě bývá tato rovnováha
narušena únikem některých isotopů
rozpadové řady (především plynného radonu) z
ložiska.
¨ Rozpadové řady tvoří
isotopy těžkých prvků vykazující
většinou radioaktivitu alfa (menší část i beta).
¨ Nukleonová
(hmotnostní) čísla členů řady odpovídají vzorcům
(n je celé číslo): 4.n pro
thoriovou řadu, 4.n+1 pro neptuniovou
řadu, 4.n+2 pro uranovou řadu 238U a 4.n+3
pro řadu 235U (aktiniovou). Je to způsobeno tím, že a-rozpad
snižuje nukleonové číslo o 4 (b-rozpad je
nemění). Z této zákonitosti plyne, že existují
právě 4 základní nezávislé
rozpadové řady.
¨ Zhruba v polovině řady
se vyskytují isotopy plynného radonu
(dříve zvaného emanace).
¨ Některé
dceřinné nuklidy (jako je 211,212,213Bi a 227Ac) se přeměňují jak a tak b
radioaktivitou, což vede k větvení
rozpadového řetězce. Za rozpadem b zde pak následuje
rozpad a a za rozpadem a naopak rozpad b, takže
obě větve se zase spojují.
¨ Přírodní rozpadové
řady končí stabilními isotopy olova,
neptuniová řada bismutem.
Přírodní
rozpadové řady jsou podrobněji rozvedeny na obr.1.4.1,
sumárně se dají zapsat takto :
232Th ® 6 a + 4 b + 208Pb ; 238U ® 8 a + 6 b + 206Pb ; 235U ® 7 a + 4 b + 207Pb ; 237Np ® 7 a + 4 b + 209Bi.
Neptuniová rozpadová řada je podrobněji nakreslena
níže na ovrázku v pasáži Aktinium-225.
Podrobnosti přeměn jednotlivých
radionuklidů v rozpadových řadách jsou značně
složité a do obr.1.4.1 se vůbec nevejdou. Některé
nuklidy rozpadových řad jsou čistými zářiči a (např. 232Th, 238U, 216Po, ......)
nebo b (např. 228Ra, 206Tl, ........), většina jader se však
přeměňuje na excitované hladiny dceřinných jader a
vyzařují proto i záření g (jsou to např. 228Ac, 214Pb, 214,212Bi, 210Tl, ......a
další, u některých je však g zastoupeno slabě,
např. u 222Rn, 239Pu, ...).
Rozpadové řady
transuranů
Analogické rozpadové řady jsou i u
uměle vyrobených transuranů, které
nakonec navazují na zmíněné základní řady. Např. 241Am ® a + 237Np ® 7 a + 4 b + 209Bi - neptuniová
rozpadová řada; 239Pu ® a + 235U ® 7 a + 4 b + 207Pb - 235U-aktiniová
rozpadová řada; 252Cf ® a + 248Cm ® a + 244Pu ® a + 240U ® b + 240Np ® b + 240Pu ® a + 236U ® a + 232Th ® 6 a + 4 b + 208Pb - thoriová
rozpadová řada. U těžkých transuranů k tomu ještě
přistupuje spontánní štěpení jader
(§1.2, část ""Exotické" druhy
radioaktivity").
Kosmogenní radionuklidy
Jsou to přírodní radionuklidy, které průběžně
vznikají jadernými reakcemi při průchodu
vysokoenergetického kosmického záření
(jeho sekundární složky) zemskou atmosférou. Patří
sem především radiouhlík 14C a tritium 3H, ve velmi malých
množstvích vznikají i některé další kosmogenní
radionuklidy - např. 7,10Be, 32P, 35S, 36Cl. Mechanismus vzniku kosmogenních
radionuklidů je nastíněn v §1.6, část "Kosmické záření", obr.1.6.7.
Kosmogenní radiouhlík 14C se
používá v archeologii pro radiometrické
určování stáří předmětů biologického
původu (viz níže "Radioisotopové
datování").
Když to shrneme, v naší
pozemské přírodě se vyskytují především dlouhodobé
radioisotopy s poločasem přeměny delším než cca
100 milionů let. Z krátkodobějších pak pouze ty, které jsou
nepřetržitě vytvářeny přírodními procesy - kosmickým
zářením nebo v rozpadových řetězcích dlouhodobých
isotopů. Všechny ostatní krátkodobé radioisotopy,
vznikající při hvězdné nukleogenezi ve velkém množství (především v supernovách), se
na Zemi nezachovaly - nazývají se někdy zaniklé,
vymřelé, vyhynulé, zhasnuté radionuklidy; pro jejich
bývalou existenci svědčí pozorovaný nadbytek stabilních
produktů jejich rozpadu (srov. níže
"Radiometrické datování", pasáž "Datování pomocí
rozpadlých radionuklidů"). Takovými důležitými zaniklými radioisotopy jsou
jód 129I, hliník 26Al a železo 60Fe, jejichž
radioaktivita se mohla uplatňovat při procesech formování
protoplanetárního disku, planet a asteroidů na počátku
vývoje sluneční soustavy.
Radioaktivita
v životním prostředí
Veškerá příroda (pozemská i vesmírná) obsahuje určité malé
množství radioaktivity, především výše uvedených
přírodních radioaktivních prvků. Sloučeniny primárních a
sekundárních radionuklidů (radioaktivních rozpadových řad)
se z hornin při jejich erozi dostávají do půdy,
do vody a do vzduchu (především přes plynný radon).
Při spalování uhlí se do ovzduší
dostávají některé přírodní radionuklidy (především radon 222Rn, polonium 210Po a olovo 210Pb), které se ve větších
hloubkách hromadí v důsledku rozpadu primárních
přírodních radionuklidů uranu a thoria. Při sopečné
činnosti je ve vyvrhovaných oblacích sopečného
kouře a prachu obsaženo značné množství radionuklidů
radonu, polonia-210, olova-210 z velkých podzemních hloubek.
Rovněž sloučeniny kosmogenních radionuklidů se z atmosféry
dostávají do biosféry. Z půdy, vody a vzduchu se přírodní
radionuklidy dostávají do rostlin a v potravním řetězci
dále do živočichů i člověka.
V našem životním prostředí jsme tudíž
neustále vystaveni ionizující radiaci z
kosmického záření a z přírodních radionuklidů ve vzduchu,
v obklopujících předmětech, v půdě a horninách,
stavebních materiálech i v našich tělech.

Obr.1.4.2. Scintilační spektrum záření gama hlíny (vzorek 200g orné půdy ze střední Moravy). Jsou patrné slabé gama-píky ze sekundárních
radionuklidů uranové a thoriové rozpadové řady (isotopy
bismutu, thalia, olova) a poměrně výrazný pík 1460keV
primárního radionuklidu draslíku 40-K.
V posledních desítiletích k
tomu přistupuje radiační zátěž i z umělých
zdrojů záření - rentgenek, urychlovačů, umělých
radionuklidů. A to jak při cíleném použití v medicínské
radiodiagnostice a radioterapii, tak příp. i z nechtěných radioaktivních
kontaminací (radiační havárie, jaderné odpady) -
§5.2, část "Zdroje ozáření ionizujícím
zářením". Příznivé
i nepříznivé biologické účinky toho přírodního a
umělého záření jsou podrobně rozebírány v §5.2 "Biologické účinky ionizujícího
záření".
Geologický význam
přírodní radioaktivity
I když relativní obsah přírodních radionuklidů ve
"stavebním" materiálu Země není vysoký, jejich
úhrnné množství v zemském nitru a kůře je natolik velké,
že jimi radioaktivně uvolňovaná energie
může mít značný geotermální význam.
Podle současných geologických
poznatků se naše planeta Země skládá z
několika vrstev. Pevný povrch tvoří poměrně tenká vrstva zemské
kůry, tzv. litosféra (řec. lithos=kámen), o
síle cca 5-50 km (podle toho, zda se nacházíme v oblasti
moře, pevniny, pohoří). Zemská kůra není celistvá, ale je
"rozlámána" na jednotlivé litosférické desky,
které se vůči sobě zvolna pohybují. Pod ní se rozprostírá
zemský plášť (rozděluje se dále na svrchní
a spodní plášť), který je do určité míry
tvárný (plastický) a tvoří největší část objemu a
hmotnosti zeměkoule. Sestává z částečně roztavených
hornin o teplotě cca 600-1250°C. V plášti probíhá tepelná
konvekce, kterou se teplo z vnitřní části Země
přenáší k povrchu. Plasticita pláště, na němž
"plavou" jednotlivé části (desky, "kry")
zemské kůry a konvekce tepla je hybnou silou posunů
kontinentů, deskové tektoniky a sopečné (vulkanické)
činnosti *). V nitru Země se nachází zemské jádro
(velikosti Měsíce), v němž teplota pravděpodobně přesahuje
4000°C; jeho vnější část je tekutá, vnitřní jádro v
samotném středu Země je (podle nepřímých geologických
měření) pevné. Pevné železité vnitřní jádro Země
"plave" a rotuje v tekutém vnějším jádře, což
generuje geomagnetické pole. Toto magnetické pole vytváří
"štít" proti ionizační vesmírné radiaci a
slunečnímu "větru". Bez něho by život na planetě
nebyl možný.
*) Jsou to "běžné" vulkány
nacházející se v místech, kde na sebe litosférické desky
narážejí. Avšak pod tenkou slupkou zemské kůry, v zemském
plášti, jako "časovaná bomba" tepelnou konvekcí
stoupají mohutné proudy žhavých roztavených hornin.
Pokud se protaví až na povrch, pod velkým tlakem vytrysknou
jako ničivé supervulkány.
Celkový tepelný
tok z nitra Země se odhaduje na cca 45 Terawattů *).
Tak mohutný tepelný tok je těžko vysvětlitelný pomocí
tepla zbylého v nitru Země (vzhledem k
dlouhé době cca 4,5 miliardy let od vzniku Země), nebo slapového gravitačního působení při rotaci
Země, oběhu Měsíce kolem Země a Země kolem Slunce (§1.2, pasáž "Gravitační
gradienty - slapové síly"
v knize "Gravitace, černé díry..."). Na vývinu tepla v zemském nitru by se zhruba 60%
mohl podílet radioaktivní rozpad přírodních
radionuklidů. Po 8-10 TW by mohly dodávat rozpadové řady
isotopů 232Th a 238+235U, radioaktivní draslík 40K by přispíval hodnotou 3-5 TW tepelného toku. Bez
tepla z přírodně se vyskytující radioaktivity by zemské
jádro již před miliardami let vychladlo a ztuhlo, což by
pravděpodobně znemožnilo vznik a rozvoj života na Zemi ("Antropický princip aneb kosmický
Bůh", část "Hvězdy, planety, život ")..!..
*) Průměrná hustota geotermálního toku
tepla u povrchu Země činí asi 65-100 mW/m2, což je méně než desetitisícina intenzity
dopadajícího slunečního záření.
Vyskytla se i hypotéza, že v nitru Země by mohl
pracovat přírodní štěpný jaderný reaktor
podobný tomu, jehož pozůstatky se nalezly v dole v Oklo
(viz §1.3, část "Jaderné
reaktory", pasáž "Přírodní
jaderné reaktory?"). Před
několika miliardami let, kdy byla koncentrace štěpného uranu 235U ještě
dostatečně vysoká, je to docela pravděpodobné. Aby takový
reaktor mohl fungovat i v současnosti, kdy podíl štěpného 235U značně poklesl,
musela by koncentrace uranu v materiálu v nitru Země být
podstatně vyšší, než v nám známých horninách zemské
kůry; o tom nemáme žádné indicie.
O struktuře nám nedostupných oblastí zemského nitra
máme jen poměrně málo nepřímo získaných informací.
Důležité údaje o rozložení radioaktivních prvků v nitru
Země by bylo možno získat pomocí detekce neutrin,
tzv. geoneutrin, vznikajících při b-radioaktivním
rozpadu přírodních radionuklidů, které z nitra Země volně
procházejí mocnými vrstvami horniny až na povrch (viz §1.2, část "Neutrina - "duchové"
mezi částicemi",
pasáž "Neutrina z přírodní radioaktivity").
Radioisotopové
(radiometrické) datování
Nezávislost rychlosti (poločasu) radioaktivního rozpadu na
vnějších podmínkách *) umožňuje využít exponenciální rozpadový
zákon radioaktivity jako jakési hodiny - přírodní
"chronometr".
*) Situace, kdy průběh a rychlost
radioaktivního rozpadu může poněkud záviset na vnějších
radiačních či chemických faktorech, jsou diskutovány v
§1.2, pasáž "Nezávislost radioaktivního
rozpadu na vnějších podmínkách".
Základní idea použití radioaktivního rozpadu
k měření času je jednoduchá. Pokud známe počáteční
počet N0
(v čase t=0) radioaktivních jader mateřského nuklidu X
se známým poločasem rozpadu T1/2 ve vzorku, pak změřením absolutní aktivity A(t)
vzorku, nebo poměru koncentrace mateřských X a
dceřinných Y isotopů, v nějakém pozdějším čase t
můžeme z rozpadového zákona stanovit tento čas t,
uplynulý od vzniku vzorku (t=0) do doby měření - tedy stáří
vzorku. Z rozpadového zákona radioaktivity (odvozeného v §1.2, část"Obecné zákonitosti přeměny
atomových jader") NX(t) = NX(0).e-l.t = NX(0).e-t.(ln2/T1/2) = NX(0).2-t /T1/2 ; NY(t) = NX(0).[1-e-l.t] = NX(0).[1-e-t.(ln2/T1/2)] = NX(0).[1-2-t /T1/2], pro hledané stáří t vyplývá vzorec:
t = T1/2 . ln2.[1 + NX(t)/NY(t)] ,
kde NX(t)
je nynější množství mateřského prvku X a NY(t) je nynější
množství dceřinného prvku Y ve zkoumaném vzorku (počáteční množství NX(0) mateřského radionuklidu většinou neznáme,
někdy se ho pokoušíme odhadnout, např. u 14C).
Všechny materiály (na Zemi i ve vesmíru)
obsahují určité malé množství přírodních
radionuklidů s dlouhými poločasy rozpadu. Rychlosti
jejich radioaktivní přeměny lze za určitých podmínek
využít k určování stáří různých
předmětů a vzorků materiálů. Tato metoda určování
stáří vzorků se obecně nazývá radioaktivní,
radioisotopové či radiometrické datování,
nebo radioisotopová chronometrie; podle
vyšetřovaných nuklidů pak např. radiokarbonové
datování (s použitím uhlíku-14,
je popsáno níže), draslík-argonové
či uran-olovnaté datování. Používá se v
archeologii, paleontologii, geologii (geochronologie) i
astronomii (stáří meteoritů a planet).
Jsou dvě základní podmínky, které by měly
být splněny pro přesné radioisotopové datování :
1. Jsou známé počáteční podmínky -
koncentrace nebo poměry mateřského a dceřinného isotopu v
době přírodního vzniku vyšetřovaného materiálu (v čase
"0");
2. Vyšetřované materiály musí být od
svého vzniku uzavřené či izolované
systémy, takže žádné mateřské ani dceřinné isotopy z
nich neunikly ani do nich nevstoupily.
Tyto podmínky nejsou nikdy 100-% splněny, takže
"přímočaré" radiometrické datování není zcela
přesné. Níže bude nastíněno, jakými metodami lze provést
nezávislé kalibrace a zvýšit přesnost a
spolehlivost radioisotopového datování (je
popsáno tzv. izochronní a
korkondantní datování).
Radiouhlíková datovací metoda (zvaná též uhlíková chronometrie)
používá radiouhlík 14C, který vzniká účinkem neutronů,
vyrážených kosmickým zářením z jader atomů, na dusík ve
vyšších vrstvách zemské atmosféry: no + 14N7 ® 14C6 + p+ (viz
§1.6, část "Kosmické záření", obr.1.6.7). Takto
vznikají asi 2 atomy 14C za sekundu na 1cm3 atmosféry. Uhlík 14C, jakožto dlouhodobý radionuklid (T1/2 = 5730roků, čistý b-,
energie 158keV) neustále kontaminuje
biosféru, v atmosféře oxiduje na 14CO2, vstupuje do biocyklu
- do potravinového řetězce živých organismů na Zemi.
Fotosyntézou se z atmosféry dostává do rostlin, odtud
potravou do těl živočichů. Je proto obsažen ve všech
živých organismech. Ustaví se koncentrace 1 atomu 14C na cca 8.1013 atomů běžného 12C; jeden gram
přírodního uhlíku ve všech živých organismech obsahuje
aktivitu asi 0,25 Bq 14C. Po odumření organismu se jeho metabolický styk s
atmosférou a přísun 14C přeruší, takže koncentrace radiouhlíku se začne
snižovat jeho radioaktivním b-rozpadem 14C ® 14N + e- + n´ s poločasem 5730
roků. Mění se tím i relativní zastoupení mezi
uhlíkovými isotopy 14C, 13C a 12C.
Z poměru mezi relativním zastoupením radioaktivního istopu 14C a stabilními
isotopy uhlíku ve zkoumaném historickém předmětu biologického
původu (třebas dřevo, pozůstatky organismů a pod.)
můžeme přibližně stanovit stáří tohoto
předmětu - dobu, která uplynula od uhynutí organismů, z
nichž daný předmět pocházel. Poprve
tuto metodu použil W.F.Libby v r.1946.
V nejjednodušším případě změříme specifickou
aktivitu 14C ve zkoumaném historickém předmětu biologického
původu a srovnáme to s rovnovážnou specifickou aktivitou
radiouhlíku v atmosféře a v živých organismech.
Citlivost měření aktivity 14C pomocí proporciálních nebo scintilačních
detektorů s kapalnými scintilátory (viz §2.6, část "Kapalné
scintilátory"), vzhledem k poločasu
rozpadu 14C
5730 let, omezuje časový dosah této metody na cca 30 000 let.
Podstatně nižší hodnoty zastoupení 14C/12C lze zjišťovat pomocí metody hmotnostní
spektrometrie (viz §2.6, pasáž "Magnetické spektrometry").
Předpokladem správnosti radiouhlíkové chronometrie je, že
poměr zastoupení 14C/12C byl v minulosti, během období z něhož pocházejí
měřené vzorky, vždy stejný. Aby tento poměr zůstal
konstantní, musí zůstat konstantní intenzita a složení
kosmického záření a jeho působení na horní vrstvy
atmosféry. Primární kosmické záření přicházející z
mezihvězdného prostoru má pravděpodobně neměnnou intenzitu
v období nejméně 105let. Složka přicházející ze Slunce je však
časově proměnná v závislost na sluneční aktivitě (výskyt
slunečních skvrn). Působení kosmického záření na horní
vrstva atmosféry závisí na tom, jak silné je stínění
magnetickým polem Země. Intenzita geomagnetického pole
kolísá o cca 50% v časových obdobích cca 104let. Dalším
problémem je antropogenní vliv (lidskou civilizační
činností) na distribuci radionuklidů v atmosféře. Je to
jednak spalování fosilních paliv ovlivňující obsah CO2 v atmosféře, jednak radiouhlík
uvolněný do atmosféry jadernými zkouškami hlavně v
50.letech. Stanovování koncentrace radiouhlíku tak má i
značný ekologický význam. Pro přesnou
radiohlíkovou chronometrii jsou všechny tyto vlivy
zkreslující, je třeba na ně vzít korekci, sestavit kalibrační
křivku porovnáním s jinými nezávislými metodami (např. s dendrochronologií - datování
pomocí letokruhů ve dřevě starých stromů).
Chronologie
přírodních dějů pomocí 10Be
Dalším kosmogenním radionuklidem s dlouhým poločasem rozpadu
je berylium 10Be. Vzniká v horních vrstvách
atmosféry z kyslíku a dusíku jadernými reakcemi se
sekundárními neutrony vyráženými vysokoenergetickým
kosmickým zářením. 10Be se s poločasem T1/2 1,6x106 let beta- -radioaktivitou rozpadá na stabilní isotop 10B. Používá se k
průzkumu zvětrávání hornin, tvorby a eroze půdy,
chronologie jezerních sedimentů. Zajímavé je měření
koncentrace isotopu berylia 10Be v různých vrstvách ledovců jako
indikátoru sluneční činnosti v dávných dobách - jako
výsledek interakce kosmického záření a slunečního větru (modulace kosmického záření slunečním větrem je
diskutována v §1.6, pasáži "Hvězdný
- sluneční - "vítr"").
Luminiscenční
datování - optické a termoluminiscenční,
je založeno na "ukládání" elektronů, uvolněných
při dlouhodobém ozařování materiálů přírodní radiací,
v metastabilních hladinách a jejich následné
uvolnění zahříváním či světelným ozařováním vzorku
(viz §2.2, pasáž "Termoluminiscenční a fotoluminiscenční
dozimetrie", odstavec "Luminiscenční
archeologické datování").
Dlouhodobé
datování minerálů
Radiouhlíková
metoda není použitelná pro datování anorganických látek jako jsou horniny, a
též pro velmi dlouhá časová období milonů
či miliard let. Zde lze za určitých
okolností využít rozpady dalších dlouhodobých přírodních radioaktivních izotopů, jako je
rozpad draslíku 40K na argon, rozpad radioaktivního izotopu rubidia 87 na
stroncium, nebo rozpad uranu a thoria na konečný prvek
rozpadové řady - olovo. Radioaktivní datování pomocí
stanovení relativního zastoupení dceřinných radiogenních
produktů rozpadu vzhledem k mateřským nuklidům
umožňuje v geologii určit absolutní stáří hornin
*), trvání jednotlivých geologických epoch, stáří
meteoritů, samotné Země, Měsíce i sluneční soustavy.
Přesnost těchto metod je však, vedle technických obtíží
stanovení nepatrných množství nuklidů, omezena
různorodostí nalezených vzorků a jejich předchozích osudů.
*) Stáří
hornin
Pod stářím nerostů se v mineralogii a
geologii rozumí časový interval od doby vzniku
minerálu tuhnutím a krystalizací z roztavené hmoty,
do dnešní doby (doby měření). Předpokládá se, že při
ztuhnutí dochází k uzavření
("zakonzervování") látkového složení minerálu,
které se již pak nemění jinak, než příp. radioaktivní
přeměnou.
Pozn: Vzhledem k nepatrným koncentracím
zkoumaných radionuklidů a jejich dlouhým poločasům nelze
použít jednoduchou metodu měření radioaktivity vzorků.
Stanovení koncentrace analyzovaných nuklidů se provádí
metodou hmotnostní spektrometrie (viz §2.6, pasáž "Magnetické spektrometry").
Draslík
- argonová metoda určování stáří nerostů
Datovací metoda K-Ar v jaderné geochronologii
využívá rozpadu přírodního (primordiálního)
radioaktivního draslíku 40K s
poločasem 1,26 miliad roků na stabilní argon 40Ar.
Přírodní draslík je tvořen třemi isotopy: 39K
(93,258% - stabilní), 40K
(0,0117% - radioaktivní) a 41K
(6,73% - stabilní). Radioaktivní isotop 40K
se s poločasem 1,28.109 let
rozpadá dvěma způsoby: b- (89,1%) 40K ® 40Ca + e-
+ n na vápník ; b+ (10,9%) 40K ® 40Ar + e+
+ n na argon. V
nerostu obsahujícím draslík od okamžiku jeho vzniku v
krystalické formě (a uzavření) ubývá radioaktivní isotop
draslíku 40K a hromadí se
stabilní isotop argonu 40Ar,
vznikající přeměnou 40K.
Změřením obsahu obou těchto isotopů ve vzorku lze stanovit
stáří minerálu. Obsah 40K se
stanoví změřením obsahu draslíku v nerostu a známého
zastoupení isotopu 40K v
draslíku. Pro stanovení obsahu 40Ar
se vzorek zahřeje ve vakuu na teplotu cca 2000°C, čímž se
plynný argon uvolní z krystalové mřížky a obsah 40Ar se stanoví hmotnostní
spektrometrií.
Doplňující a
upřesňující metodou K-Ar datovací metody je metoda argon-argon
(40Ar/39Ar)
datování. Vzorek minerálu se nejprve ozařuje
neutrony v jaderném reaktoru, čímž na jádrech
stabilního isotopu draslíku 39K
probíhá reakce 39K(n,p)39Ar. Pak se ozářený vzorek
zahřeje ve vakuu, čímž se uvolní oba isotopy argonu a jejich
obsah se stanoví hmotnostní spektrometrií. Stáří nerostu se
stanoví z poměru obsahu obou isotopů argonu (neboť množství
39Ar vzniklého reakcí s
neutrony je úměrné obsahu draslíku v nerostu).
Rubidium-stronciové
datování
je založeno na beta--radioaktivní
přeměně přírodního primordiálního isotopu rubidia-87:
87Rb ® 87Sr
+ e- + n´ na stroncium-87 s
poločasem 4,8.1010
roků. Pokud minerál obsahuje aspoň malé množství
rubidia, tato velmi pomalá radioaktivní přeměna způsobuje,
že od doby vzniku nerostu krystalizací z roztavené horniny se
v něm obsah přírodního rubidia 87Rb
zmenšuje a obsah radiogenního stroncia 87Sr
se zvětšuje. Ze změřeného poměru zastoupení obou isotopů
lze určit stáří minerálu. Komplikací však je, že
minerály mohou obsahovat i určitá množství přírodního
stroncia a tím i isotopu 87Sr
neradiogenního původu *). Pro přesné určení stáří
analyzovaného nerostu je proto potřeba zjištěný obsah 87Sr korigovat na obsah
neradiogenního 87Sr. K tomu se
využívá stanovení dalšího isotopu stroncia - 86Sr
(opět pomocí hmotnostní spektrometrie). Na základě známého
poměru 87Sr/86Sr
neradiogenních isotopů v přírodním stronciu (v minerálech
které neobsahují rubidium) lze pak od zjištěného obsahu 87Sr odečíst obsah neradiogenního 87Sr.
*) Jádra isotopu 87Sr neradiogenního původu vznikla spolu s jinými
isotopy stroncia při nukleární syntéze prvků ve vesmíru (v
supernovách), nikoli radioaktivními přeměnami 87Rb.
Datování
hornin pomocí rozpadu uranu a thoria na olovo
Tato metoda U-Pb, Th-Pb je založena na měření nynějšího
množství mateřského prvku X (uranu 235U, 238U či thoria 232Th)
a koncového dceřinného prvku Y příslušné rozpadové
řady (olova 207Pb, 206Pb či 208Pb)
- viz výše "Přírodní
rozpadové řady", obr.1.4.1. Z rozpadového zákona
příslušného mateřského prvku X s poločasem rozpadu
T1/2 pak dostaneme pro
výsledné stáří t vztah:
t = T1/2 . ln2.[1 + NX(t)/NY(t)]
,
kde NX(t) je nynější
množství mateřského prvku X a NY(t)
je nynější množství dceřinného prvku Y
(příslušného isotopu olova).
Vhodným minerálem sloužícím jako "nosič" uranu
či thoria je křemičitan zirkonu ZrSiO4,
který se běžně vyskytuje v horninách sopečného původu.
Při tvorbě krystalu zirkonu se do jeho krystalové mřížky
snadno dostává uran nebo thorium, avšak nikoli olovo. Při
datování proto můžeme předpokládat, že veškeré olovo ve
vzorku je radiogenního původu - vzniklo rozpadem uranu
či thoria. .............
.....konkordantní datování - níže...........
Datování
pomocí rozpadlých radionuklidů
Výše uvedené metody radiometrického datování vyžadují,
aby v měřeném vzorku zůstala určitá malá, ale měřitelná
porce výchozího mateřského radionuklidu. To může být
problém u nejstarších vzorků
pocházejících např. z počátků formování naší
sluneční soustavy. V takovém případě může paradoxně
pomoci datování pomocí radioisotopů s kratším
poločasem, které se již rozpadly
("vymřely") a ve vzorku nejsou přítomné. Ve vzorku
jsou však přítomné produkty jejich rozpadu,
stabilní dceřinné nuklidy. Měřením
koncentrace těchto dceřinných produktů vymřelých
radionuklidů hmotnostním spektrometrem lze pak určit
relativní stáří analyzovaného vzorku. V koprodukci s
isochronní technikou lze kalibrovat např. metodu U-Pb a
zpřesnit stanovení absolutního stáří.
Do této kategorie patří 129I-129Xe
jód-xenonová chronometrie. Při výbuchu
supernovy vzniká m.j. i velké množství radioaktivního jódu 129I. Radionuklid jód 129I
se s poločasem 15,7 milionů let (který se z
běžného pohledu jeví dlouhý, avšak z astronomického
hlediska je docela krátký...) přeměňuje beta--radioaktivitou na stabilní isotop xenonu 129Xe.
V xenonu izolovaném z kamenných meteoritů chondritů
byl nalezem vyšší obsah isotopu xenonu 129Xe, než odpovídá
jeho obvyklému zastoupení v přírodním xenonu.
Přebytek 129Xe se v chondritech
vytvořil radioaktivní přeměnou isotopu 129I
(radiogenní 129Xe),
který byl v materiálu chondritů uzavřen při
vzniku pevné silikátové hmoty po ochlazení horké plynné
mlhoviny z výbuchu supernovy. U protoplanetárního stádia
naší sluneční soustavy k tomu docházelo v období mezi cca
4,8-4,5.109 let, před vznikem
naší planetární soustavy.
Při praktickém použití je
jód-xenonová chronometrie poměrně složitá izochronní
laboratorní metoda. Vzorky se ozařují neutrony v jaderném
reaktoru, čímž se záchytem neutronu stabilní isotop jódu 127I přeměňuje na
radioaktivní 128I a následnou beta-přeměnou na stabilní xenon 128Xe. Po ozáření se
vzorek zahřívá a uvolňovaný xenon se analyzuje v
hmotnostním spektrometru, porovnává se obsah 129- a
129-xenonu. ......
Určování
doby vzniku meteoritů
Meteority, zvláště některé kamenné typy zvané chondrity,
patří mezi nejstarší tělesa v naší sluneční soustavě.
Vznikaly již při chladnutí protoplanetárního disku, před
vznikem planet (.....). ...odkaz.....
Isochronní
metoda datování
Jednoduché datovací metody mohou být nepříznivě ovlivněny
neznalostí a variabilitou počátečních podmínek (různou
koncentrací mateřských a dceřinných nuklidů) a možností
migrace příslušných nuklidů mezi analyzovaným materiálem a
okolním prostředím. Pro eliminaci těchto vlivů a zpřesnění
dlouhodobého radioisotopového datování byla
vypracována tzv. isochronní metoda. Tato
složitější (ale velmi elegantní) metoda používá sběr
minerálních vzorků ze dvou nebo lépe několika
různých částí (složek) analyzované horniny a
isotopovou analýzu provádí pomocí třech isotopů:
nejen mateřského a dceřinného prvku, ale navíc se měří
obsah dalšího isotopu dceřinného prvku.
Máme tedy v analyzovaném materiálu
výchozí mateřský radioaktivní nuklid X, který se s
pločasem T1/2 rozpadá na
stabilní dceřinný radiogenní nuklid Y´; příslušný
dceřinný prvek má ještě další stabilní isotop Y
(neradiogenního původu). Jelikož všechny isotopy dceřinného
prvku Y mají shodné chemické vlastnosti, je poměr
zastoupení těchto isotopů NY´/NY v celé analyzované hornině
stejný. Naopak isotop X má jiné chemické vlastnosti a
počáteční poměr NX/(NY´+NY)
je v době vzniku horniny různý pro různé minerály. V
důsledku rozpadu radioaktivního isotopu X budou po
dostatečně dlouhé době relativní zastoupení NX/NY a NY´/NY v různých minerálech horniny
různá.
Množství nuklidu Y´ v
analyzovaném materiálu se skládá z původního
počátečního množství NY´(0)
a z jader vzniklých radioaktivním rozpadem radionuklidu X.
Z exponenciálního zákona rozpadu mateřského radionuklidu X
plyne pro časový růst koncentrace dceřinného stabilního
radoiogenního nuklidu Y´ vztah NY´(t) = NY´(0) + NX(t).[el.t
-1].
Vydělením tohoto vztahu množstvím NY
dalšího stabilního isotopu Y dostaneme rovnici pro poměry
koncentrací nuklidů:
[NY´/NY](t) = [NY´/NY](0)
+ [NX/NY](t).[el.t -1] .
Zvolíme-li si čast t jako parametr, je to v poměrech
koncentrací nuklidů lineární rovnice y = a.x
+ b, jejímž grafem je přímka zvaná isochrona
( řec. isos=stejný, chronos=čas -
isochrona je čára spojující na grafu místa se stejným
časem výskytu zobrazovaného jevu). Sklon této přímky
tga ş
a = el.t -1 určuje čas t (stáří), průsečík
(intercept) se svislou osou b = [NY´/NY](0) určuje jinak neznámý
počáteční poměr nuklidů Y´ a Y.
Změříme tedy současný obsah NX(t), NY´(t),
NY(t) těchto tří isotopů v
několika vzorcích a vyneseme do grafu poměr NX/NY
na vodorovnou osu a poměr NY´/NY na svislou osu (obr.1.4.3 vlevo).
Vzniklými body metodou nejmenších čtverců proložíme lineární
regresní funkci - přímku představující isochronu.
Jestliže je závislost NY´/NY lineárně rostoucí funkcí NX/NY
(jednotlivé body dobře "sedí" na přímce),
svědčí to pro dobrou korelaci mezi
změřeným úbytkem radioisotopu X a změřeným přírustkem
dceřinného isotopu Y´. Regresní přímka má tvar y = a.x +
b, kde b představuje původní poměr prvků NY´(0)/NY(0).Výsledné
stáří t se pak stanoví ze vztahu :
t = (ln2/T1/2) . [NY´(t)/NY(t)
- NY´(0)/NY(0)] / [NX(t)/NY(t)] ,
kde T1/2 je poločas rozpadu
výchozího mateřského radionuklidu X. Počáteční
poměr NY´(0)/NY(0)
zjistíme z regresní přímky.
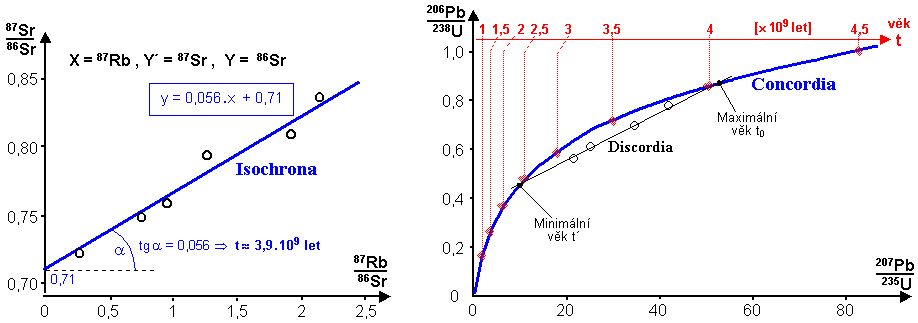
| Obr.1.4.3.
Isochronní a konkordantní analýza u
dlouhodobého radiometrického datování. |
| Vlevo:
Lineární regresní funkce - isochrona
pro Rb/Sr datování - proložená body [NX/NY, NY´/NY]
z několika vzorků téže horniny. |
Vpravo:
Křivka concordia pro 235U + 238U
datování, spolu s discordií (chybovou
přímkou) proloženou změřenými hodnotami
vzorků téže horniny. |
|
Velkou výhodou
izochronní metody je její nezávislost na
původním poměru isotopů dceřinného prvku: tento neznámý
původní poměr získáme z regresní přímky. Původní poměr
isotopů Y a Y´ mohl být v minulosti velmi
různý a přesto nám vyjde stejné stáří.
Pokud body v grafu isochrony neleží na přímce, svědčí to
pro nějaké události, které v průběhu historie narušily
uzavřený systém horniny. Výsledná hodnota stáří
pak nebude přesná, přičemž z regresní
analýzy můžeme stanovit střední kvadratickou chybu
získané průměrné hodnoty.
Nejčastěji používané trojice
isotopů pro isochronní datovací metodu jsou uvedeny v tabulce
(X- výchozí mateřský radoionuklid, Y´-
jeho stabilní dceřinný nuklid, Y- další
stabilní isotop tohoto dceřinného prvku) :
| X |
T1/2
[roky] |
Rozpad radionuklidu X®Y´ |
Y´ |
Y |
| 87Rb |
4,72.109 |
b- : 87Rb ® 87Sr + e- + n´ |
87Sr |
86Sr |
| 147Sm |
1,06.1011 |
a : 147Sm ® 143Nd
+ a |
143Nd |
144Nd |
| 176Lu |
3,8.1010 |
b- : 176Lu ® 176Hf + e- + n´ |
176Hf |
177Hf |
| 187Re |
4,3.1010 |
b- : 187Re ® 187Os + e- + n´ |
187Os |
186Os |
| 235U |
7,04.108 |
a,b- : 235U ® 7 a + 4 b +
207Pb |
207Pb |
204Pb |
| 238U |
4,5.109 |
a,b- : 238U ® 8 a + 6 b +
206Pb |
206Pb |
204Pb |
Jak bylo výše zmíněno,
spolehlivost a přesnost dlouhodobých datovacích technik je,
vedle technických obtíží, omezena různorodostí nalezených
vzorků a zejména neznalostí jejich předchozích osudů během
miliónů či dokonce milard let jejich historie. Při exaktním
archeologickém, paleontologickém a geologickém datování se
proto velký důraz klade na souhlasnost
výsledků získaných různými nezávislými metodami
- mluvíme o tzv. konkordantním datování (lat. concordantiae = shoda,souhlas,soulad).
Konkordantní radioisotopové datování
U radioisotopového datování lze soulad (konkordanci)
analyzovat použitím dvou různých radionuklidů,
především uranu 235U a
238U. Využívá se zde toho,
že v nitru vzorku pomyslně "tikají" dvoje
radiaktivní hodiny: rychleji "tikající"
uran-235 se přeměňuje s poločasem 700 miliónů let,
pomalejší hodiny jsou založeny na uranu-238 s poločasem cca
4,5 miliard let. Porovnání výsledků z obou těchto
chronometrů umožňuje zpřesnit stanovení stáří vzorku.
Z rozpadových zákonů pro
oba urany plynou dvě isochronní rovnice :
[206Pb/204Pb](t) = [206Pb/204Pb](0) + [238U/204Pb](t).[el238U.t -1] ,
[207Pb/204Pb](t) = [207Pb/204Pb](0) + [235U/204Pb](t).[el235U.t -1] .
Jestliže z několika naměřených vzorků téže horniny
dostaneme pomocí těchto rovnic dvě stejné nezávislé
hodnoty stáří t - došlo ke konkordanci
(souladu), je to významná indicie správnosti
datovací metody.
Z těchto dvou izochronních
rovnic dále můžeme vytvořit tzv. diagram konkordance
(obr.1.4.3 vpravo). Na vodorovnou osu vyneseme (v lineárním
měřítku) poměr 207Pb/235U a na svislou osu poměr 206Pb/238U
*). Čas t použijeme jako parametr: pro různé hodnoty t
graficky vyneseme body {[207Pb/235U](t); [206Pb/238U](t)}. Vznikne tím teoretická křivka
zvaná concordia, jejíž každý bod udává
konkordantní hodnotu stáří t a poměru koncentrací
isotopů olova a uranu za předpokladu, že do vzorku nevstoupily
ani z něho neunikly žádné nuklidy. Do tohoto grafu se pak
vynášejí hodnoty konkrétních vzorků z analyzovaného
minerálu. Dostáváme body, které obecně neleží na
concordii, neboť předpoklad uzavřenosti nemusí být splněn.
Jelikož všechny isotopy uranu a isotopy olova mají stejné
chemické vlastnosti, jejich příp. únik z materiálu je
stejný a měřené hodnoty poměru uranu a olova by měly ležet
na přímce. Proložíme tedy měřenými body přímku - zvanou discordia
(lat. nejednotnost, nesvár, nesoulad),
jejíž průsečiky s konkordií představují počáteční čas
t0 krystalizace materiálu
("maximální věk") a čas t´ ("minimální
věk") odpovídající možné události metamorfózy během
historie vzorku. Konkordantní diagram slouží jako vnitřní
kontrola datovací metody, umožňující odhalit
události, které narušily podmínky správného datování.
*) Jedná se zde o radiogenní olovo 207Pb a 206Pb: od celkového
změřeného množství těchto isotopů je pomocí isochronní
metody odečteno iniciání množství 207Pb(0) a 206Pb(0).
Stanovení stáří Země a
Sluneční soustavy
Radiometrické datování s pomocí radionuklidů s velmi
dlouhým poločasem rozpadu se významě uplatnilo nejen u
geologických minerálů, ale umožnilo stanovit i stáří
naší planety Země a celé Sluneční soustavy. Pomocí pouze
geologických metod je určení stáří Země problematické,
nepřesné, v podstatě nemožné. V důsledku
geologických procesů - zvětrávání, desková tektonika,
vulkanismus, hydrotermální procesy - se chemické a fyzikální
složení hornin výrazně měnilo.
V první polovině 20.stol.
byl hlavním průkopníkem radiometrického datování hornin, geochronologie,
A.Holmes, který s postupným upřesňováním metod uran-olovo
stanovoval stáří hornin v rozmezí cca 1,5-3 miliardy let.
Jeho nástupce C.C.Patterson použil metodu uran-olovo i na stáří
meteoritů pocházejících z raných období po
zformování naší planety. Meteority jakožto vesmírná
tělesa jsou výhodnější pro datování, neboť nebyly
pozměněny žádnými geologickými procesy. Patterson v r.1965
měřil vzorky z meteoritů nalezených v okolí impaktního
kráteru Barringer v Arizoně a dospěl k hodnotě jejich
stáří 4,55 miliardy let. Tato měření byla mnohokrát
opakována, dospělo se k průměrné hodnotě 4,56
miliardy let (± 1% odchylky).
Toto je tedy hodnota stáří
planety Země a zároveň i celé Sluneční
soustavy. Veškerý materiál ve Sluneční soustavě se
totiž utvořil ve zhruba stejné době, různé chemické látky
včetně radioaktivních isotopů vznikly společně. Ukazují to
měření různých meteoritů pocházejících z odlišných
oblastí Sluneční soustavy - jednotlivé planety se zformovaly
prakticky ve stejné době (z astronomického
hlediska).
O vzniku hvězd a planet a
jejich chemickém vývoji viz §4.1, část "Evoluce
hvězd", o primordiální kosmologické
nukleosystéze §5.4, část "Leptonová
éra. Prvotní nukleosyntéza"
monografie "Gravitace,
černé díry a fyzika prostoročasu". O stanovování stáří různých objektů ve
vesmíru (hvězd, galaxií, celého
vesmíru) viz §4.1, pasáž "Stáří
objektů ve vesmíru".
Výroba umělých radionuklidů
Pro potřeby současné vědy a techniky, průmyslu a
zdravotnictví, zdaleka nevystačíme s těmi několika
radionuklidy přírodního původu (přírodní
radionuklidy uran 235 a 238 jsou však základem štěpných
jaderných reaktorů a na nich založené jaderné energetiky). Musíme tedy radionuklidy vyrábět uměle.

Obr.1.4.4. Ostřelováním terčíkového
jádra A urychlenou elementární částicí vzniká jadernou
reakcí výsledné jádro B.
Výsledné jádro B vzniká zpočátku obvykle v
excitovaném stavu B' s následnou deexcitací
emisí fotonů gama. Toto pro výrobu radionuklidů většinou
není důležité, s výjimkou situací, kdy excitované jádro
je metastabilní s dlouhým poločasem.
Abychom ze stabilního jádra
vyrobili jádro radioaktivní, je nutno změnit počet
protonů či neutronů tak, aby byla porušena
rovnovážná konfigurace. Jak bylo rozebíráno v předchozím
§1.3 "Jaderné reakce",
dosáhneme toho podle obr.1.4.4 ostřelováním
výchozího terčíkového jádra A
vhodnými částicemi - protony či neutrony (popř. i
alfa-částicemi, deuterony, ojediněle těžšími ionty),
které vstupují do jádra a vyvolávají tam příslušné
změny - jaderné reakce; vzniká výsledné
jádro B (většinou v excitovaném stavu B´,
po vyzáření záření gama pak v základním stavu), které je často radioaktivní.
Produkční rovnice a
výtěžnost
Ozařujeme-li tedy terčík obsahující N atomů
výchozího ozařovaného prvku (jader A) svazkem
částic (protonů či jiných nabitých částic z cyklotronu,
nebo neutronů z jaderného reaktoru) o intenzitě I
[počet částic/cm2/sec.], budou se v terčíku postupně hromadit atomy
výsledného radionuklidu (B). Za dobu ozařování t bude aktivita A(t)
požadovaného radionuklidu v terčíku přibližně dána produkční
rovnicí
A(t) =
I . N . s . (1 - e-l.t) ,
kde s
[cm2] je
účinný průřez dané jaderné reakce a l [s-1] je rozpadová konstanta vznikajícího radionuklidu (s
poločasem rozpadu souvisí vztahem l = 0,693/T1/2). Množství
vyrobené aktivity je tedy přímo úměrné intenzitě
ozařujícího svazku, množství terčíkové látky a
účinnému průřezu reakce *). Zpočátku je toto množství
přibližně úměrné i ozařovací době t, avšak
vlivem radioaktivního rozpadu vznikajícího radionuklidu,
vyjádřeného saturačním faktorem (1 - e-lt), se přírustek počtu vznikajících jader postupně
zpomaluje a po cca 5-6 poločasech výsledného radionuklidu B je
již dosaženo stavu nasycení (cca 98%),
rychlost produkce a rozpadu se vyrovnává, aktivita při
dalším ozařování již neroste. Výsledná aktivita
vyrobeného radionuklidu B je pak A = I.N.s.
*) Tyto zákonitosti platí za zjednodušených předpokladů
homogenního a časově konstantního svazku záření a tenkého
terčíku obsahujícího mnohonásobně větší počet
výchozích atomů (A) než je počet vznikajících jader (B).

Závislost účinného průřezu jaderných reakcí na energii
ostřelujících neutronů (vlevo) a protonů (vpravo).
Účinný průřez jaderné
reakce, a tím výtěžnost produkce, podstatně
závisí na energii ozařujících částic.
Tato závislost je obecně složitá a různorodá pro různé
druhy produkčních reakcí.
Při
ozařování neutrony je zpravidla vyšší
účinný průřez pro pomalé neutrony (i
když některé reakce probíhají naopak s neutrony vyšších
energií). S rostoucí energií účinnost
monotónně klesá, neboť rychlejší neutrony setrvávají v
poli jaderných sil kratší dobu a pravděpodobnost proběhnutí
jaderné reakce se tím snižuje. V oblasti desítek a stovek eV
energetická závislost jeví složitou strukturu rezonančních
maxim a minim (způsobených
diskrétními hladinami energií nukleonů v jádrech).
Ozařování
protony (jakož i deuterony či těžšími
kladnými částicemi) vede k jaderným reakcím až při
dosažení určité prahové energie, potřebné
k překonání odpudivé elektrické (Coulombovské) bariéry
kolem jádra *), za spolupůsobení tunelového jevu. Účinný
průřez proto zpočátku výrazně roste s energií, dosahuje
maxima a posléze monotónně klesá (neboť
energetické protony rychle proletí oblastí jádra a za tento
krátký čas je menší pravděpodobnost uskutečnění jaderné
reakce). Pro nejjednodušší reakci (p,n)
u středně těžkých jader je prahová energie protonů cca
5MeV a maximální výtěžnost kolem 10MeV. Pro složitější
reakce, alfa-částice a těžší jádra, je křivka
výtěžnosti posunuta k vyšším energiím, 20MeV a výše.
*) Pod touto energií může proton
proniknout do jádra jen kvantovým tunelovým jevem
(§1.1, pasáž "Kvantový
tunelový jev"), s
podstatně menší pravděpodobností.
Tyto zákonitosti
energetické závislosti platí nejen pro požadované
produkční reakce, ale i pro příp. další paralelně
probíhající "parazitní" reakce v terčíkovém
materiálu, při nichž vznikají jiné
radionuklidy než požadované - radionuklidové
nečistoty. Je proto třeba nastavit určitou optimální
energii, zaručující vysokou produkční výtěžnost
s minimálním obsahem radionuklidových nečistot.
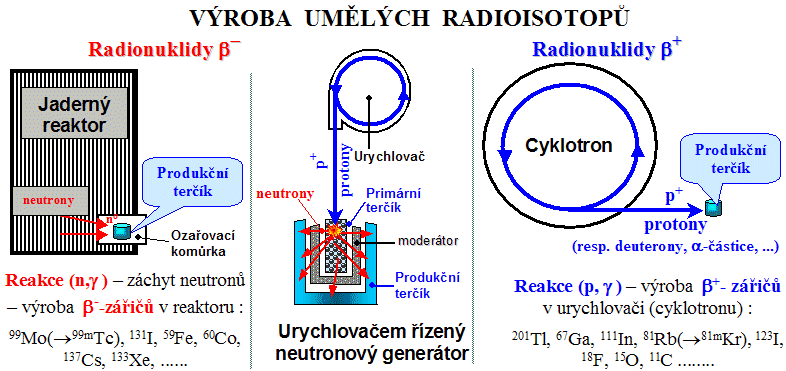
Obr.1.4.5. Výroba radioisotopů
ozařováním terčíkových jader v jaderném reaktoru (vlevo),
neutronovém generátoru (uprostřed) a v cyklotronu (vpravo).
Výroba
radionuklidů v jaderném reaktoru
Nejsnadnější je ozařování jader neutrony -
jelikož neutron nemá elektrický náboj, nepůsobí elektrické
odpudivé síly a i pomalý neutron ochotně vstupuje do jádra.
Nejobvyklejší reakcí je zde prostý neutronový
záchyt (n, g): NAZ + no ® N+1BZ + g *), mohou však nastávat i reakce typu (n,p), (n, a). Ozařováním
neutrony obecně vznikají jádra s přebytkem neutronů, které
obvykle vykazují radioaktivitu b-. Intenzívním zdrojem neutronů je jaderný
reaktor (§1.3, část "Jaderné reaktory"), takže tyto b--radionuklidy
se vyrábějí ozařováním vhodného terčíkového materiálu
v ozařovací komůrce reaktoru - obr.1.4.5 vlevo.
Některé reakce výroby radionuklidů ozařováním neutrony
jsou např.: 6Li(n,a)3H,
14N(n,p)14C, 32S(n,p)32P, 98Mo(n,g)99Mo, .... Konkrétní
způsoby výroby řady důležitých radioisotopů jsou popsány
níže v části "Vlastnosti
některých nejdůležitějších radioaktivních isotopů".
*) Pozn.:
Záchytu neutronů za vzniku radioaktivních jader se vyžívá i
ve velmi citlivé metodě analýzy chemického složení látek -
neutronové aktivační analýze. Ozářením
zkoumaného vzorku neutrony dochází ke vzniku radionuklidů (k
"aktivaci"), načež spektrometrickou analýzou
energií emitovaného záření (především g) aktivovaného
vzorku lze stanovit příslušný radionuklid a
zpětně i jemu odpovídající (neaktivní) výchozí
nuklid, s použitím kalibrace též jeho obsah
ve zkoumaném materiálu. Metoda je podrobněji popsána v kap.3
"Aplikace ionizujícího záření", §3.4, pasáž
"Neutronová aktivační analýza".
Další často používanou
metodou výroby radionuklidů v jaderném reaktoru je
ozařování uranu 235U neutrony,
což vyvolá štěpení jader uranu na menší
jádra, která jsou radioaktivní, např. :
235U + n ® 236U ® 131I + 102Y + 3n
® 137Cs + 97Y + 2n
® 133Xe + 101Sr + 2n
® 99Mo + 135Sn + 2n
® 155Sm + 78Zn + 3n
......... a další
radionuklidy.
Z těchto štěpných produktů se pak izolují
potřebné radionuklidy (např. 131I, 99Mo, 133Xe a další) pomocí radiochemických metod. Jelikož
těžká jádra uranu mají podstatně větší procentuální
zastoupení neutronů než středně težká jádra vzniklá
jejich rozštěpením, mají tyto radionuklidy přebytek
neutronů a vykazují radioaktivitu b-.
Nyní již méně časo
používaným způsobem výroby radionuklidů je jejich chemická
separace ze štěpných produktů uranu jako paliva
v reaktoru. V jaderném reaktoru se jádra uranu 235U (popř. 238U) po vstupu
neutronů rozštěpí na dvě jádra, chemicky
spadající do prostřední části Mendělejevovy periodické
tabulky, která jsou většinou radioaktivní.
Nejčastějšími takto vzniklými jádry jsou např. 131I, 137Cs, 90Sr, .... Vyhořelé palivové
články z reaktoru obsahují velké množství těchto
radionuklidů (řádově TBq). Je však značně obtížné
radiochemicky izolovat jednotlivé radionuklidy z této
různorodé směsi tak, aby získaný radionuklid neobsahoval
stopy ostatních radionuklidů - aby měl vyhovující radionuklidovou
čistotu, nebyl kontaminován.
Urychlovačem
řízený neutronový generátor
Vedle jaderných reaktorů mohou být intenzívními zdroji
neutronů i urychlovače. Protony
urychlené na vysoké energie se nechají dopadat na (primární)
terčík z těžkého kovu (olovo, bismut,
wolfram), kde způsobují tříštivé reakce,
při nichž z terčíkových jader vyrážejí řadu částic a
fragmentů, především velké množství neutronů.
Neutrony se zpomalují v moderátoru (může to být voda, která zároveň chladí terčík) a dopadají na produkční terčíky,
umístěné kolem místa vzniku neutronů, v nichž jadernými
reakcemi jsou produkovány požadované radioisotopy - obr.1.4.5
uprostřed.
Tato metoda je zatím
spíše experimentální, ale jeví se velmi perspektivní.
Kromě výroby radionuklidů umožňuje i likvidaci a
přepracování radioaktivních odpadů s dlouhodobými
radioisotopy a získávání jaderné energie z thoria - je
podrobněji diskutováno v §1.3, část "Jaderné
reaktory", pasáž "Urychlovačem
řízené transmutační technologie ADTT".
Výroba
radionuklidů v urychlovači
Pro výrobu pozitronových b+-radionuklidů je naopak potřeba do jádra dodat protony.
K tomu, aby proton p+ vstoupil do jádra, musí být urychlen na
vysokou energii řádově stovky keV až několika MeV,
aby svou kinetickou energií překonal odpudivou elektrickou
Coulombovskou sílu kladně nabitého jádra. Nejčastějšími
urychlovači protonů jsou cyklotrony (§1.5, pasáž "Cyklotron"), které
elektromagnetickými silami urychlují protony během mnoha
oběhů po kruhové dráze (udržované
magnetickým polem) na vysoké energie.
Protonový svazek je pak magnetickým polem vyveden z kruhové
dráhy a dopadá na vhodný terčíkový materiál - obr.1.4.5
vpravo. Podle energie protonů může probíhat řada reakcí.
Nejjednodušší z nich je radiační záchyt protonu (p, g): NAZ + p+ ® N+1BZ+1 + g, nastávají však i reakce typu (p, p), (p, n), (p,
d), (p, a), zvláště při vyšších energiích a u těžších
jader.
Za účelem jaderné reakce a transmutace lze jádra
ozařovat kromě protonů i jinými rychlými nabitými
částicemi: deuterony d - dochází
především k reakcím (d, n), (d, p), a-částicemi
- nastávají reakce (a, p), (a, n) *), popř. i těžšími jádry
či ionty.
*) Pozn: Jaderných reakcí (a,n) se využívá
též jako zdroje neutronů. Pro tento účel
nepotřebujeme mít jádra hélia urychlené uměle, ale
vystačíme s vhodnými a-radionuklidy, které homogenně
smísíme s vhodným terčíkovým materiálem - některými
lehkými prvky, které dávají velký výtěžek neutronů v
reakci (a,n). Nejvhodnější je berylium v
reakci 9Be(a,n)12C, které smícháme
s vhodným a-zářičem - používá se např. 210Po, 226Ra, 239Pu, 241Am. Tyto směsi se hermeticky uzavírají či zatavují
do kovových nebo skleněných nádobek a slouží jako
přenosné laboratorní zdroje neutronů, tzv. neutronové
generátory, používané např. při neutronové
aktivační analýze (§3.4 "Neutronová
aktivační analýza").
Jádra s přebytkem protonů
jsou většinou beta+-radioaktivní nebo se rozpadají elektronovým
záchytem; podle způsobu své výroby se někdy označují jako cyklotronové
radionuklidy. Některé reakce výroby radionuklidů
ozařováním protony jsou např.: 18O(p,n)18F, 13C(p,n)13N, 11B(p,n)11C, .... ; deuterony
např. 10B(d,n)11C, 56Fe(d,n)57Co, ..... .
Konkrétní způsoby výroby řady důležitých radioisotopů
jsou popsány níže v části "Vlastnosti některých
nejdůležitějších radioaktivních isotopů".
Urychlování
záporných iontů - možnost
zvýšení fluenčního výkonu vnějšího svazku z cyklotronu
V cyklotronu se standardně urychlují těžké kladně
nabité částice - protony, deuterony, alfa částice,
příp. těžší jádra jako je uhlík 12C. U malých cyklotronů používaných pro výrobu
radioisotopů je důležitým požadavkem vysoká
intenzita - fluenční výkon - protonových či
deuteronových svazků. Při energiích kolem 40MeV se daří
dosahovat poměrně značného proudu v paprsku cca 2-5 mA. Tento
maximální výkon lze však plně využít jen při ozařování
interního terčíku, instalovaného uvnitř
vakuové urychlovací trubice. Pro rutinní výrobu radionuklidů
je ale výhodnější vyvedení částicového
svazku k ozařování vnějších terčíků. V
klasických cyklotronech urychlujících kladné částice se
výsledný paprsek extrahuje elektrostatickým deflektorem.
Na přepážce tohoto deflektoru však vzniká značné disipativní
teplo, které je omezujícím faktorem pro dosažení
vysokého fluenčního výkonu extrahovaného svazku.
Tuto
nevýhodu do značné míry odstraňuje technologie urychlování
záporných iontů (§1.5, část
"Cyklotron", pasáž "Urychlování
záporných iontů"). Atomům vodíku nebo deuteria se v iontovém zdroji v
elektrickém výboji dodají dva elektrony, čímž vzniknou
záporné ionty H-
či D- vodíku se dvěma elektrony. Ty se potom urychlují v
cyklotronu. Po potřebném urychlení se do cesty záporných
iontů H- v příslušné dráze vloží tenká uhlíková fólie,
která "strippováním" odstraní jejich oba
lehké elektrony a propustí požadované těžké p+ či d+. Tím se obrátí
směr jejich zakřivení v magnetickém poli, což způsobí
jejich rychlé vyvedení z pole cyklotronu do externího
svazku příslušné energie, s minimální tepelnou
disipací. Dosahuje se tím podstatně vyšších
výkonů produkce radionuklidů ve vnějším terčíku. To je důležité především
pro výrobu větších aktivit radioisotopů pro scintigrafickou
diagnostiku (§4.8 "Radionuklidy a radiofarmaka pro
scintigrafii") a biologicky cílenou radionuklidovou terapii (§3.6 "Radioisotopová terapie") v nukleární medicíně.
Úprava
ozařovaného materiálu v terčíku. Radionuklidová čistota.
Základem pro výrobu požadovaného radionuklidu je :
¨
Volba vhodné
produkční jaderné reakce
- výchozího nuklidu a druhu ostřelujících částic a jejich
energie, což implikuje i požadované ozařovací zařízení
(jaderný reaktor, neutronový generátor, cyklotron) a jeho
vlastnosti.
¨
Příprava
vhodného terčíku
ozařovaného nuklidu, jeho chemické formy a provedení.
Ozařovat můžeme buď přímo výchozí prvek
v elementární formě, nebo jeho vhodnou sloučeninu.
Často je potřebné izotopové obohacení
ozařovaných materiálů v terčíku - zvyšuje to výtěžnost
reakce a usnadňuje následnou radiochemickou separaci.
Isotopové obohacování terčíkových materiálů je
technologicky velmi náročné a drahé. Po ozařování a
separaci vzniklého radionuklidu se proto zbylý obohacený
materiál recykluje k opakovanému ozařování.
Materiál k ozařovaní v terčíku se používá
ve všech třech běžných skupenstvích :
l Terčík v pevném skupenství
je tvořen krystalickou formou (nebo práškovým amorfním
materiálem) výchozího terčíkového prvku či jeho
sloučeniny. Často je to kovová forma daného
těžšího prvku, či jeho slitiny. Po ozážení se
terčíkový materiál použije buď přmo (zapouzdří se a
vznikne uzavřený zářič), nebo se rozpustí
ve vhodné kyselině či hydroxidu a provádí se radiochemická
separace a příprava požadované chemické formy
daného radioisotopu (příp. radioisotopvé označení radiofarmaka
pro nukleární medicínu ).
l Kapalný terčík je
tvořen ampulkou s výchozím prvkem či jeho sloučeninou která
je za normální teploty kapalná, nebo je rozpuštěna
ve vhodném rozpouštědle - nejčastěji je to vodní roztok.
Po ozáření se v kapalném preparátu provede radiochemická
separace a uvedení vzniklého radioisotopu do potřebné
chemické formy či radiofarmaka.
l Plynný terčík je
tvořen stlačeným plynem uzavřeným ve vhodné ampulce či
komůrce (nejčastěji jsou to inertní
plyny xenon, argon, krypton, ...). Po
skončení ozařování se vzniklý radioisotop (obsažený v
objenu komůrky nebo nasorbovaný na stěnách) vymyje vodou nebo
zředěnou kyselinou; další radiochemické úpravy jsou
analogické jako u výše uvedených terčíků. V případě
isotopově obohaceného plynu se provede jeho recyklace
pro opakované použití.
Po
ozáření je v terčíkovém materiálu obsažen nejen
požadovaný radionuklid (aspoň nikdy ne ve 100% koncentraci),
ale i řada dalších atomů a příp. dalších radionuklidů
vzniklých jinými (paralelními "parazitními")
reakcemi. Zpravidla je proto ozářený materiál nutné podrobit
náročné proceduře radiochemické separace
požadovaných radionuklidů.
Radionuklidová
čistota,
udávající procentuální poměr aktivity požadovaného
radionuklidu k celkové aktivitě preparátu, je důležitým parametrem
kvality vyrobeného radionuklidu. Pro technologické a
medicínské aplikace se zpravidla požaduje vysoká
radionuklidová čistota, lepší než 99,9% - neboli
obsah radionuklidových nečistot menší než
0,1%. Radioinuklidové nečistoty mohou působit rušivě při
analytických či zobrazovacích měřeních, příp. způsobovat
zvýšenou radiační zátěž pacienta (je
diskutováno též §4.8, část "Radionuklidy
a radiofarmaka pro scintigrafii",
pasáž "Radionuklidová čistota radiofarmak").
Sekundární radionuklidy z rozpadových
produktů. Radionuklidové generátory.
Některé radionuklidy se přeměňují na dceřinná jádra,
která nejsou stabilní, ale jsou opět radioaktivní - jedná se
o sekundární radioisotopy. Získávání
těchto sekundárních radionuklidů z rozpadových produktů
jiných radionuklidů může být efektivním způsobem jejich
"výroby".
Obzvláštní důležitost má tato metoda u krátkodobých
radionuklidů, které vznikají jako dceřinná jádra
radionuklidů s podstatně delším poločasem rozpadu.
Příslušný mateřský radioisotop, připravený ozářením na
urychlovači nebo reaktoru, může být bez obtíží dopraven do
vzdálené laboratoře, kde z něj lze průběžně či
opakovaně separovat dceřinný krátkodobý
radionuklid, který je tak k dispozici po značně delší dobu (danou poločasem rozpadu mateřského radionuklidu). Zařízení, které umožňuje opakovaně separovat
krátkodobý radionuklid vznikající rozpadem jiného
dlouhodobějšího radionuklidu, se nazývá radionuklidový
generátor. Rozdílné fyzikálně-chemické vlastnosti
umožňují od sebe v generátoru oddělit
mateřský a dceřinný prvek. Generátor je systém obsahující
pevně vázaný mateřský radionuklid s delším
poločasem rozpadu, z něhož vznikající dceřinný radionuklid
s kratším poločasem (který již není
pevně vázán na nosič mateřského radionuklidu) lze oddělit (odseparovat) buď chemicky (v
kapalné fázi), hydrodynamicky (eluce), či
profukováním vzduchem. Výhodou radionuklidových generátorů
je možnost používat příslušné krátkodobé radionuklidy i
na pracovištích vzdálených od jaderného reaktoru nebo
cyklotronu. Kinetika radionuklidových generátorů z hlediska rozpadové
rovnováhy mateřského a dceřinného radionuklidu je
analyzována v §1.2, pasáž "Směsi radionuklidů, rozpadové řady,
radioaktivní rovnovaha".
Typickým příkladem radionuklidového
generátoru je molybden-techneciový generátor 99Mo/99mTc (podrobněji popsaný v §1.2, část "Záření
gama", pasáž "Radionuklidové
generátory", viz též níže
"Molybden-Technecium"), kde beta-rozpadem
molybdenu 99Mo (T1/2=66hod.)
vzniká metastabilní technecium 99mTc
(T1/2=6hodin), které
je čistým zářičem gama (Eg=140keV) a má široké uplatnění ve scintigrafii v
nukleární medicíně - viz kapitola 4
"Radionuklidová scintigrafie",
§4.8 "Radionuklidy a
radiofarmaka pro scintigrafii",
kde je na obr.4.8.1
nakreslen princip činnosti a technické provedení 99Mo-99mTc generátoru. Rubidium-kryptonový
generátor, používaný při ventiční scintigrafii plic, je
popsán níže v pasáži "Rubidium-Krypton". V oblasti PET scintigrafie nachází stále
významnější uplatnění germanium-galiový generátor
68Ge/68Ga (viz níže galium Ga-68).
Uvedeme v tabulce několik častěji
používaných radionuklidových generátorů :
| Mateřský
radionuklid (T1/2) |
Typ rozpadu |
Dceřinný
radionuklid (T1/2) |
Typ rozpadu |
Výsledný nuklid |
| 68Ge
(275 d) |
EC ® |
68Ga
(1,14 hod) |
b+,EC,g ® |
68Zn |
| 81Rb
(4,7 hod) |
b+,EC ® |
81mKr
(13 sec) |
g
® |
81Kr |
| 82Sr
(25 dní) |
EC ® |
82Rb
(75 sec) |
b+,EC,g ® |
82Kr |
| 90Sr
(28 roků) |
b-
® |
90Y
(2,6 dne) |
b-
® |
90Zr |
| 99Mo
(2,78 dne) |
b-
® |
99mTc
(6 hod) |
g
® |
99Tc |
| 113Sn
(115 dní) |
EC ® |
113mIn
(1,66 hod) |
g ® |
113In |
| 188W
(69,4 dní) |
b-
® |
188Re
(16,98 hod) |
b-
® |
188Os |
| 227Ac
(21,77 roků) |
a,b-řada ® |
227Th
(18,7 dne),
223Ra (11,4 dne) |
a,b-
řada® |
207Pb |
| |
|
|
|
|
| |
|
|
|
|
"In vivo generátory" v nukleární
medicíně
V nukleární medicíně se vhodné sloučeniny radionuklidů - radiofarmaka
- aplikují do vnitřního prostředí organismu, kde vstupují
do metabolických procesů a podle své biochemické farmakokinetiky
se mohou akumulovat v určitých cílových
tkáních a orgánech. Jestliže je toto radiofarmakum
značeno radionuklidem, který se přeměňuje nikoli na
stabilní, ale na další radioaktivní isotop s
kratším poločasem, pak po jeho vychytání se v cílové
tkáni in vivo generuje
a hromadí další krátkodobější radionuklid, který spolupůsobí
s primárním mateřským radionuklidem. Pokud tento in vivo generovaný
dceřinný radionuklid emituje g-fotony
nebo pozitrony, může být použit pro scintigrafické
zobrazování (planární, SPECT, PET -
kapitola 4 "Radioisotopová
scintigrafie"); pokud
emituje částice alfa či beta-
(příp. Augerovy elektrony), může
sloužit (či přispívat) k radionuklidové terapii
- §3.6 "Radioisotopová terapie".
Tato situace, kdy do organismu aplikovaný dlohodobější
radionuklid svou radioaktivni přeměnou vytváří v cílové
tkáni dceřinný krátkodobější radionuklid (či celou
rozpadovou řadu), se někdy nazývá in vivo
radionuklidový generátor - v kontextu s výše
uvedenými laboratorními radionuklidovými generátory.
Určitým problémem u in
vivo generátorů je uvolňování - disociace - dceřinných
atomů z molekul radiofarmaka, vedoucí ke zhoršené
stabilitě a redistribuci dceřinných radionuklidů.
Vedle chemických dějů - změna mocenství
(oxidačního čísla) atomů při radioaktivní přeměně - se
na tom podílí i zpětný odraz jader
při radioaktivní emisi kvant alfa, beta, částečně i gama (§1.2, pasáž "Doprovodné jevy při
radioaktivitě", odstavec
"Zpětný odraz jader").
Kinetická energie zpětného odrazu jader zpravidla
mnohonásonmě převyšuje vazbovou energii
příslušných atomů v chemické vazbě *). Vyvíjejí se
radiochemické metody značení biomolekul, které pronikají
dovnitř cílových buněk a jsou v nich internalizovány,
přičemž se dceřinné atomy mohou dostatečně dlouho udržet
v cílových buňkách.
*) Projevuje se to především u
alfa-radioaktivity. Např. při emisi alfa-částice energie 4-7
MeV je dceřinnému jádru s nukleonovým číslem cca 220
zpětným odrazem předána kinetická energie cca 60-100 keV.
Chemická vazbová energie příslušných atomů v
biomolekulách (konjugátech např. s monoklonálními
protilátkami) přitom činí jen cca 2-5 eV.
Typickým příkladem
používaného in vivo generátoru je radium 223Ra
, které se aplikuje jako radiofarmakum ve formě chloridu.
Vychytává se v kostních metastázách, v nichž se pak
223-radium "in vivo" rozpadá s poločasem 11,4 dne
celou kaskádou alfa-přeměn (v kombinaci s
nevýznamnou alfa-beta větví) na další krátkodobé
radionuklidy: 223Ra(11,4d.;
a) ® 219Rn(4s.; a) ® 215Po(1,8ms.; a) ® 211Pb(36,1min.; b-) ® 211Bi(2,2min.; a) ® 207Tl(4,8min.; b-) ® 207Pb(stab.) -
podrobnosti viz níže radium 223Ra.
Při jedné úplné radioaktivní přeměně
jádra 223Ra
v celé rozpadové řadě až na stabilní 207Pb se uvolní celková jaderná energie téměř 30 MeV, především čtyřmi
alfa-částicemi, s vysokým radiobiologickým účinkem;
vznikají též fotony gama, které mohou být využity ke
gamagrafickému monitorování distribuce radiofarmaka. Radium 223Ra však
neumožňuje chelatační vazby na složitější biomolekuly
jako jsou monoklonální protilátky, takže jeho využití je
velmi omezené (223Ra-chlorid pro paliativní terapii kostních metastáz).
Perspektivnějším
radionuklidem typu "in vivo generátor" je thorium 227Th,
které (na rozdíl od radia) umožňuje, s pomocí
makrocyklického ligandu typu DOTA, chelatační navázání 227Th k monoklonálním
protilátkám za vzniku radioimunokonjugátů,
které se cíleně vychytávají v nádorových buňkách.
Vysokoenergetické a-částice, emitované při radioaktivních
přeměnách, pak mohou účinně ničit tyto
nádorové buňky - podrobnosti viz níže thorium 227Th.
Dalším
radionuklidem, který by v cílené alfa-terapii mohl velmi
dobře fungovat jako in vivo generátor, je aktinum
225Ac,
které se s poločasem 10 dní rozpadá kaskádou 4 alfa přeměn
(v kombinaci s nevýznamnou alfa-beta větví)
na další krátkodobé radionuklidy: 225Ac(10d.; a) ® 221Fr(4,8m.; a) ® 217At(32ms.; a) ® 213Bi(46m.; b-) ® 213Po(4ms.; a) ® 209Pb(3,3h.; b-) ® 209Bi(stab.) , uvolňuje se energie asi 27 MeV - podrobnosti viz níže aktinium 225Ac.
I zde vzniká doprovodné záření gama, které může být
použito pro scintigrafické zobrazení. Radiofarmaka značená 225Ac (včetně
monoklonálních protilátek, např. 225Ac-Trastuzumab či 225Ac-PSMA-617) se zkoušejí pro terapii lukemie,
lymfomů, neuroendokrinních nádorů, gliomů, melanomů, velmi
slibné jsou u ca prostaty. Tento "in vivo
generátorový" způsob terapie se ukazuje podstatně
efektivnější, než dříve zkoušená aplikace samotného 213Bi (jehož nevýhodou je i krátký poločas rozpadu 46
min.).
Terapeutické využití in vivo
radionuklidových generátorů je podrobněji diskutováno v
§3.6, pasáži "Alfa a beta radionuklidy pro terapii".
Chemické sloučeniny radionuklidů.
Radioisotopové značení. Radioaktivní preparáty.
Radioaktivní jádra - radionuklidy - jsou za normálních
okolností součástí atomů (které mají stejné chemické vlastnosti jako
neradioaktivní atomy), tvořících radioaktivní
látku. Jen vyjímečně to bývá čistý radioaktivní
prvek, většinou se jedná a radioaktivní
sloučeniny vlastních atomů radioisotopů s jinými
neradioaktivními atomy, často i ve směsi s jinými látkami.
Radioaktivní látka cíleně připravená pro laboratorní,
technické či medicínské použití, se často nazývá radioaktivní
preparát.
Přírodní radionuklidy (popsané výše v části "Přírodní radionuklidy") jsou v přírodním
prostředí rozptýleny s velmi nízkou koncentrací. Těžké
prvky uran-238,235 a thorium-232 jsou obsaženy v zemské kůře v
minerálech ve formě oxidů, křemičitanů, příp.
fosforečnanů. Draslík K-40 se spolu
s normálním neradioaktivním draslíkem hojně vyskytuje
nejčasteji ve formě chloridu, dusičnanu, síranu. Tritium H-3 je ve formě "těžké" vody 3H2O, uhlík C-14 je v
atmosféře ve formě oxidu uhličitého 14CO2. V rostlinách se radiouhlík a tritium zabudovává do
prakticky všech biomolekul v buňkách, posléze i v buňkách
živočichů a člověka.
Chemickými reakcemi s
účastí radioaktivních atomů se zabývá speciální obor radiochemie.
Cílené chemické navázání atomů určitého radionuklidu do
molekul dané látky se nazývá radioisotopové
značení. Takto značená látka - preparát -
se pak používá většinou jako radioindikátor
pro různé analytické a diagnostické postupy (§3.5 "Radioisotopové
stopovací metody" a
§4.8 "Radionuklidy a
radiofarmaka pro scintigrafii"), nebo jako radioterapeutikum v
biologicky cílené radioisotopové terapii (§3.6,
část "Radioisotopová terapie").
Chemické reakce značení požadovaným
radionuklidem zpravidla neprobíhají se stoprocentním
výtěžkem. Proto se ve výsledných přípravcích kromě
vlastní požadované radioaktivní látky vždy vyskytuje i
malé množství nenavázané aktivity a příp. jiných
radioaktivních látek, které mají odlišné radiochemické
vlastnosti a mohou působit rušivě, zhoršují
specificitu vazby značené látky v laboratorních,
diagnostických či terapeutických aplikacích. Vedle výše
diskutované radionuklidové čistoty je proto
důležitým parametrem kvality radiochemická čistota
preparátů. Je to podíl deklarované chemické sloučeniny
daného radionuklidu na celkové aktivitě přípravku.
Část vzniklého
ionizujícího záření se absorbuje již uvnitř
materiálu radioaktivního preparátu, dochází k samoabsorpci
záření ve vzorku. Toto absorbované záření může
způsobovat chemické změny v materiálu (§5.1, část "Účinky záření na látku") - radiolýzu
značené látky vlastním zářením (nejčastěji beta či
alfa). Při tomto radiačním rozkladu ubývá
požadovaná značená látka a místo ní vznikají jiné látky
s odlišnými vlastnostmi. Zhoršuje se tím radiochemická
čistota preparátu. Zvláště radioisotopově značené
složité organické molekuly snadno podléhají radiolýze.
Radiační rozklad probíhá tím rychleji, čím vyšší je specifická
aktivita preparátu.
Rozpadová
(přeměnová) schémata radionuklidů
Pro přehledné a komplexní
znázornění různých druhů radioaktivních přeměn a
energetických hlain u konkrétních atomových jader se
používají tzv. přeměnová schémata
(obr.1.4.6). Mateřská a dceřinná jádra se na těchto
schématech znázorňují pomocí vodorovných čárek
(představujících energetické hladiny jader), jejichž pozice
ve schématu je určena takto: na vodorovné ose je protonové
číslo Z, poloha ve vertikálním směru je dána energií
jádra E *). Základní energetický
stav každého jádra je vyznačen tlustou čárou,
excitované stavy jádra se zakreslují tenkými
čárkami (s údaji o energii a příp. dalších
charakteristikách), v patřičné vertikální výšce nad
základním stavem. U základních stavů radioaktivních jader
je uveden poločas rozpadu, pro speciální
účely popř. i další charakteristity (např. spin).
Základní stav stabilního jádra budeme
vyznačovat kombinací tlusté plné čáry se
šrafováním dole. Metastabilní
energetické hladiny se vyznačují polotučnými
čárkami s údajem o době života (poločasu) tohoto
metastabilního excitovaného stavu.
*) Při praktickém kreslení rozpadových
schémat se přesné proporce hodnot energií a protonových
čísel většinou striktně nedodržují, dodržují se jen
příslušné relace - stavy s vyšší energií jsou zakresleny
více nahoře, jádra s větším protonovým číslem Z
jsou více vpravo od jader s menším Z.
Radioaktivní alfa a beta
přeměna jader je znázorněna šikmou šipkou
vlevo či vpravo, spojující mateřské a dceřinné jádro v
jeho příslušné energetické hladině, která se u daného
procesu realizuje; u této šipky je uveden typ přeměny (a, b, EC) a
příslušná energie kvanta záření. Deexcitace vzbuzených
hladin, tj. izomerní přechody g, jsou vyznačeny kolmými
šipkami spojujícími vyšší hladiny s
příslušnými výslednými nižšími hladinami, či se
základním stavem dceřinného jádra. U šipek
znázorňujících jaderné přeměny a dexcitace se uvádí
jejich relativní zastoupení [%]
(pravděpodobnost, intenzita) - průměrný počet
emitovaných kvant (alfa, elektronů či pozitronů,
fotonů) na 100 přeměn. V dolní části
rozpadového schématu (pod čárou
dceřinného jádra, nebo z důvodu úspory místa v jiném
volném místě obrázku) se uvádí celková
energie přeměny Q [keV nebo MeV].
U vodorovných čárek,
znázorňujících základní a excitované energetické stavy
jader, se v přeměnových schématech uvádějí jejich energie.
Hodnoty této energie jsou vztaženy k základnímu stavu
dceřinného jádra, kterému se přiřadí energie
"0". Základní stav mateřského
jádra pak má energii Q a příp. excitované
stavy dceřinného jádra mají příslušné nižší energie.
Větvená přeměna
Složitější situace nastává v případě větvené
přeměny, kdy se dané mateřské jádro přeměňuje dvěma
různými typy radioaktivity (s určitou
pravděpodobností) na dvě různá dceřinná jádra
s různými energiemi základního stavu - viz
§1.2, pasáž "Smíšená (kombinovaná)
radioaktivita - větvené přeměny". Pak máme dvě různé hodnoty celkové energie
přeměny Q a dvě série energetických hladin dceřinných
jader. U každé větve radioaktivní přeměny se energie
počítají nezávisle. Základnímu stavu
jednoho dceřinného jádra se přiřadí energie "0",
od které se stanovují energie excitovaných hladin, jakož i
energie mateřského jádra. Totéž se udělá pro druhé
dceřinné jádro ve druhé větvi přeměny. Mateřské jádro
pak má dvě různé výchozí hodnoty energie, které k němu
připíšeme z té strany schématu, na který směřuje
příslušný druh přeměny. Typický příklad této situace
můžeme vidět na rozpadovém schématu 186Re, 192Ir, 152Eu a několika dalších.
Na obr.1.4.6 jsou
znázorněna některá nejjednodušší typická rozpadová
schémata :

Obr.1.4.6. Nejjednodušší typická přeměnová schémata
radioaktivity a, b+, b-, b-+ g a větvené přeměny EC+b-.
Úplně vlevo je to čistý rozpad a (mechanismus
podle obr.1.2.2 v §1.2), kde se
vyzářením čásice a (jádra hélia 4He2)
mateřské jádro NAZ přeměňuje na základní stav dceřinného jádra N-4BZ-2 o nižší energii;
jádro B je posunuto doleva o dvě místa, jak
to odpovídá protonovému číslu Z-2 a dolů podle
energetického rozdílu. U šipky (u alfa se používá dvojitá
šipka) znázorňující vlastní přeměnu se uvádí typ
přeměny a příslušná energie kvanta emitovaného záření.
Hned vedle je přeměnové schéma
čisté radioaktivty b+ (NAZ ® NBZ-1 + e+ + n), kde dceřinné jádro B je vůči
mateřskému jádru A posunuto o jedno místo
doleva, což odpovídá snížení protonového čísla o 1.
Dále je na obr.1.4.6 rozpadové schéma čisté
radioaktivity b- (NAZ ® NBZ+1 + e- + n´, podle obr.1.2.3 v §1.2), kde se mateřské jádro A
přeměňuje na základní stav dceřinného jádra B,
posunutého o jedno místo doprava.
Pro jednoduchost jsme zde zatím odhlédli od
skutečnosti, že čistá přeměna a či b na základní hladinu
dceřinného jádra se vyskytuje jen v menším procentu
případů; většinou vzniká dceřinné jádro v excitovaném
stavu, s následnou deexcitací - kombinovaná radioaktivita a+g či b+g. Poslední
rozpadové schéma na obrázku 1.1.5 vpravo představuje ukázku
radioaktivity b konkrétního jádra 137Cs, které se s poločasem T1/2=30 let přeměňuje na dceřinné jádro 137Ba, které je
stabilní. Na základní stav barya jde jen asi 6,5% případů,
zatímco celých 93,5% případů jde na excitovaný stav jádra 137Ba o energii 662keV,
znázorněný vodorovnou čárkou. Svislou šipkou směrem dolů
je znázorněna deexcitace tohoto vzbuzeného stavu za
vyzáření fotonu záření g o této energii 662keV (vlastnosti
tohoto důležitého radionuklidu 137Cs jsou
podrobněji popsány níže v pasáži "Cs-137").
Úplně vpravo na obr.1.4.6 je ukázka výše
zmíněné větvené radioaktivní přeměny
jednoho mateřského jádra dvěma různými typy
radioaktivity na dvě různá dceřinná jádra
(v ukázce se jedná o zjednodušené
schéma radinuklidu 186Re, podrobněji popsaného níže v pasáži 186Re).
Rozpadová schémata některých radionuklidů
jsou značně složitá, s řadou kaskádových přeměn
korpuskulárních a množstvím excitovaných energetických
hladin, mezi nimiž nastávají izomerní přechody doprovázené
kvanty záření gama. Tomu odpovídají i složitá
spektra takových radionuklidů. Spektrometrická
analýza emitovaného záření je pak hlavní metodou
poznávání struktury nuklidů.
V
následující části "Vlastnosti některých
nejdůležitějších radionuklidů" uvedeme
konkrétní rozpadová schémata řady významnějších a
častěji používaných radionuklidů, spolu se spektry jejich
záření a dalšími jejich vlastnostmi, včetně aplikací.
Vlastnosti
některých nejdůležitějších radioaktivních isotopů
Z velkého množství radionuklidů (nyní je jich známo více
než 2000), z nichž některé se vyskytují v přírodě,
většina je však vyráběna uměle, má význam a praktické
uplatnění jen necelá desetina. Zde se seznámíme s
některými radioisotopy obzvlášť zajímavými nebo
důležitými z hlediska přírodovědného či
pro praktické aplikace. Tyto významné
radionuklidy si podrobněji popíšeme s uvedením jejich
vlastností, rozpadových schémat a spekter záření *),
způsobů vzniku či výroby a jejich použití. V úvodu popisu
vlastností jednotlivých radionuklidů uvádíme vždy stručnou
zmínku o fyzikálně-chemických vlastnostech příslušných prvků;
s těmito vlastnostmi sice přímo nesouvisí radiační
chování příslušných radionuklidů (radioaktivita
je vlastností atomového jádra, nikoli elektronového obalu), ale jsou důležité pro radiochemii přípravy
radioisotopů a jejich chování a distribuci v přírodě,
včetně živých organismů. Kromě toho jsou i mnohé
neradioaktivní isotopy důležité v jaderných a radiačních
procesech: ať již jako zdroj ostřelujících částic, jako
terčíkové materiály, součásti detekčních médií,
stínící a kolimační materiály. Všechny tyto souvislosti je
pro komplexní pochopení jaderné a radiační fyziky
užitečné reflektovat...
*) Spektrometrii
záření gama
některých používaných radionuklidů jsme na našem
pracovišti nukleární medicíny v Ostravě-Porubě v rámci
svých skromných možností v 70. a 80. letech prováděli na scintilačním
NaI(Tl) detektoru ( velikosti 5x5cm) a polovodičovém
Ge(Li) detektoru s pomocí 4096-kanálového analyzátoru
ICA-70, později pomocí počítačového analyzátoru
Canberra-Packard. Nyní již Ge(Li) detektor na našem
pracovišti nemáme (dosloužil...) a níže uvedená polovodičová spektra byla
pořízena na HPGe detektoru spektrometrické
laboratoře regionálního centra SÚJB a SÚRO v
Ostravě-Zábřehu za laskavé spolupráce kolegů Ing.J.Lušňáka
a Ing.J.Rady - autor jim moc děkuje. Za
konverzi některých změřených HPGe spekter ze staršího
datového formátu a jejich zobrazení ve formátu MsExcel autor
děkuje kolegovi Ing.M.Koláčkovi z KNM
Ostrava.
Spektra měkkého záření gama a
charakteristického X-záření (o
energiiích nižších než 30keV, pro které je detekční
účinnost koaxiálního velkoobjemového HPGe detektoru již
velmi nízká) byla měřena odděleně na planárním
polovodičovém detektoru s beryliovým vstupním okénkem.
Některá tato měření byla většinou
realizována před řadou let ještě na analogových
spektrometrech, takže do našich spekter jsme je zabudovali
naskenováním a proložením původích grafů spekter -
omlouváme se za příp. zkreslení a zhoršenou kvalitu.
Spektrometrii záření beta
jsme před mnoha lety velmi improvizovaně zkoušeli pomocí plastických
scintilátorů a kapalných scintilátorů, což
rozhodně není optimální (magnetický
spektrometr jsme bohužel nikdy nevlastnili...). Spojitá spektra záření beta u jednotlivých
radionuklidů v našem pojednání neuvádíme i proto, že jsou
celkem "fádní" a nezajímavá - vizuálně jsou si
podobná "jak vejce vejci", jen protažená k vyšším
či smrštěná k nižším maximálním energiím. Relevantní
informace z nich lze získat pouze náročnou počítačovou
analýzou metodou Fermi-Kurie grafu (§2.6 "Měření
záření beta, protonů a neutronů. Kapalné scintilátory."; tedy jsme to počítali ručně a graficky
vynášeli na milimetrovém papíře...). Konverzní
a Augerovy elektrony s diskrétními spektry o
charakteristických energiích by byly sice zajímavé, ale na
našem pracovišti jsme je "neměli na čem" měřit...

Scintilační a polovodičový detektor používaný při gama-spektrometrii
radionuklidů.
Vlevo: Scintilační sonda - scintilační
krystal NaI(Tl) +fotonásobič se stíněním. Uprostřed:
Analogově-digitální konvertor (ADC) a počítačový (CPU)
mnohokanálový analyzátor. Vpravo:
Polovodičový Ge(Li)/HPGe detektor s předzesilovačem a
Dewarovou nádobou s chladícím kapalným dusíkem.
Společné vlastnosti
gama-spekter radionuklidů
Přes veškeré rozdíly mezi energiemi a
intenzitami záření gama emitovaného různými radionuklidy,
mají gama-spektra všech radionuklidů některé podobné rysy:
¨
Na začátku fotonového
spektra, v oblasti nízkých energií, jsou často patrné píky charakteristického
X-záření, emitovaného při přeskocích elektronů
mezi vnitřními slupkami v excitovaných atomových obalech
dceřinného prvku. K těmto excitacím atomů při
radioaktivních přeměnách dochází dvěma způsoby:
1. Vnitřní konverzí
záření gama (§1.2., pasáž
"Vnitřní
konverze záření gama a X"), kdy na uprázdněná místa po konverzních
elektronech přeskakují elektrony z vyšších energetických
hladin v atomovém obalu. Zvláště g-fotony nízkých energií
(jednotky či desítky keV) mívají vysoký koeficient konverze.
Taktéž některé izomerní přechody, vysoce zakázané z
důvodu spinového "nesouladu" mezi excitovaním a
základním stavem jádra (příkladem je izomerní 131mXe), se realizují mechanismem
vnitřní konverze.
2. Elektronovým
záchytem (§1.2, pasáž "Elektronový záchyt (EC)"), při němž na
uprázdněná místa po pohlcených elektronech (většinou ve
slupce K) okamžitě přeskakují elektrony z vyšších hladin
atomu. Právě u radionuklidů přeměňujících se
elektronovým záchytem bývá charakteristické X-záření
vysoce zastoupeno, či je dokonce dominantní (viz např. 125I).
V našich gama-spektrech, měřených
scintilačním NaI(Tl) a polovodičovým HPGe detektorem, se
píky Ka,b charakteristického X-záření zobrazují jen u
středních a těžkých radionuklidů (u
některých lehčích radionuklidů jsme nízkoenergetické píky
charakteristického X-záření měřili separátně na
křemíkovém polovodičovém detektoru, jak bylo zmíněno
výše). Charakteristické X-záření
budeme v našich spektrech uvádět a analyzovat jen tehdy, když
je výrazné - je ve spektrech jasně vidět a má radiační
význam.
¨
Pokud radionuklid emituje
více energií záření gama, bývají zpravidla nejsilnější
gama-linie v oblasti nižších a středních energií (desítky
až stovky keV), zatímco vyšší energie jsou většinou
zastoupeny s podstatně nižší intenzitou (viz níže "Zvětšené
výřezy spekter").
Zvětšené výřezy
spekter
V našich základních spektrech uvedeme
jen nejdůležitější jaderné hladiny a energie záření u
daného radionuklidu, které se uplatňují v aplikacích a jsou
měřitelné běžně dostupnou detekční technikou. Píky
slabě zastoupených radiačních energií gama se ve spektrech
graficky zobrazených v normálním měřítku (daném výškou
nejintenzívnějšího píku) ztrácejí v oblasti kolem
nulových hodnot. Pro jejich zobrazení proto používáme zvětšený
výřez ze spektra, posunutý nad vodorovnou osu;
energie přitom odpovídají základnímu měřítku na
vodorovné ose. Tyto zvětšené výřezy jsou označeny znakem
zvětšení "<", šipkou směřující vzhůru a
udáním násobku zvětšení - např. "<á16 x" - mírné zvětšení, či "<<á256 x" - silné zvětšení. K této situaci často
dochází tehdy, když radioaktivní přeměna nastává na
větší počet excitovaných stavů dceřinného jádra. Pak je
to zpravidla s větší pravděpodobností na hladiny nižších
energií, než na vyšší excitované stavy - v
gama-spektrech jsou s vyšší intenzitou zastoupeny píky
nižších energií, zatímco vysokoenergetické píky bývají
daleko slabší, jsou viditelné často až při velkém
zvětšení a delší akviziční době. Toto právě zobrazují
zvětšené výřezy spekter.
Rozdílnosti ve
scintilačních a polovodičových gama-spektrech
Podíváme-li se na níže uvedené obrázky gama-spekter řady
radionuklidů, můžeme na první pohled vidět některé
výrazné rozdílnosti mezi spektry měřenými scintilačníním
a polovodičovým detektorem:
¨
Fotopíky na scintilačním spektru jsou oblé
a pozvolné, jakoby "rozplizlé" -
energetické rozlišení je zde poměrně nedokonalé (cca 10% pro testovací linii 662keV 137Cs), blízké gama-linie splývají v jeden fotopík. Polovodičové
spektrum je tvořeno velmi ostrými a úzkými píky
- energetické rozlišení je cca 30-krát lepši. Některé
kompaktní píky ze scintilačního spektra jsou na
polovodičovém spektru rozloženy do několika gama-linií...
¨
Ve scintilačním spektru je vidět
výrazně zastoupenou spojitou složku
Comptonovsky rozptýleného záření, především v oblasti
nižších energií. Toto spojité pozadí působí rušivě (zvláště v oblasti "píku" zpětného
rozptylu, který může interferovat se skutečným gama-píkem
měřeného radionuklidu). V polodičových
spektrech je spojitá složka silně potlačena,
neboť lepší energetické rozlišení vede k úzkým a vysokým
píkům (při zachování stejné
plochy pod píkem), což na grafickém
zobrazení spektra, normalizovaném k maximu v píku, automaticky
vede ke snížení relativní výšky spojitého pozadí.
¨
Můžeme pozorovat některé rozdíly v relativní
intenzitě píků, které jsou způsobeny rozdílnou
energetickou závislostí detekční účinnosti. Scintilační
NaI(Tl) detektor měří s vyskou účinností i gama-linie s
energiemi cca 20-40keV, pro které má (námi použitý)
koaxiální HPGe detektor již velmi malou (či konce nulovou)
citlivost. Proto např. charakteristické X-záření vykazuje na
polovodičovém spektru většinou podstatně nižší
zastoupení než na scintilačním. Pro lehčí radionuklidy se
na tomto detektoru píky X-záření nezobrazují vůbec. K
jejich změření byl u některých spekter použit planární
Ge(Li) nebo Si detektor.
Omluva autora - zkreslení v zobrazení spekter
Původní změřená spektra radionuklidů z mnohokanálového
analyzátoru (s vysokým energetickým rozlišením a řadou
detailů) jsme pro zobrazení v našem pojednání museli z
kapacitních důvodů podstatně graficky zmenšit.
Vedlo to často ke geometrickému zkreslení spekter,
zvláště z polovodičových detektorů - např. ke
"smrsknutí" čar fotopíků, ztrátě některých
bodů v křivkách a jejich rozpojení, splynutí blízkých
linií. V rámci možností jsem se pokusil tato zkreslení
"vyretušovat" a připodobnit zobrazené grafy
originálnímu spektru. Ne vždy se to však zcela podařilo,
omlouvám se a uvítám připomínky kolegů - znalců
spekter...
Totéž se týká zobrazení složitějších rozpadových
schémat některých radionuklidů, kde zakreslení
blízkých energetických hladin a šipek přeměn a přechodů
se může rovněž překrývat a splývat... Z podobných
důvodů jsou energetické škály pod vodorovnými
osami spekter jen přibližné (jsme
schopni zajistit přesnost zobrazení poloh číselných hodnot
ne lepší než cca ±10%). Pro naše účely to však
nevadí, neboť přesné hodnoty energií jednotlivých píků,
odečtené z originálních spekter (nekomprimovaných, v
digitálním tvaru na spektrometru), jsou explicitně uvedeny u
šipek označujících příslušné fotopíky.
Měřítko na svislých osách naměřeného počtu
impulsů je relativní, normalizované k hodnotě 100.103 impulsů.
Jednotlivé radionuklidy
uvádíme v zásadě v pořadí protonových a
nukleonových čísel, avšak s řadou drobných
výjimek - jednak podle návaznosti radioaktivních přeměn (např radium-223 je uveno za radiem-226, z něhož se
připravuje), jednak podle důležitosti a
způsobu použití příslušných radioaktivních isotopů (např. kobalt 57-Co je uveden až po daleko
významnějším 60-Co). Pokud u určitého
prvku jeho radioaktivní isotopy svým počtem nebo významem
"nevydají" na samostatný oddíl, jsou spojeny dva či
tři blízké prvky do jedné pasáže (např.
dusík+kyslík+fluor, chrom+železo, měď+galium+germanium,
transurany) a jejich isotopy jsou
diskutovány ve vzájemné souvislosti. Toto je logické
zvláště v případě návaznosti vztahů mateřský-dceřinný
radionuklid (např. rubidium-krypton,
molybden-technecium, rozpadové řady těžkých
alfa-radionuklidů).
Různorodost
radionuklidů
Každý radionuklid je jistě něčím zajímavý. Avšak
popisovat podrobně vlastnosti všech známých
radioisotopů by bylo příliš zdlouhavé a nepřehledné *) (a jistě by to i přesahovalo síly autora...). Neuvádíme zde proto ty
radioisotopy, které byly jednou či několikrát, víceméně
náhodně, v dobovém kontextu, použity při výzkumu
některých přírodních dějů, materiálových a
biologických, či v nukleární medicíně, a pak se již
nepoužívaly - buď proto, že svou jednorázovou úlohu
již splnily, nebo byly v praxi nahrazeny
výhodnějšími radionuklidy (které samozřejmě
uvádíme). Podrobněji rozebíráme radionuklidy obzvlášť
zajímavé z jaderného a obecně přírodovědného hlediska,
či široce používané ve vědecko-technických aplikacích, v
medicíně, průmyslu (zvláště pak ty,
které autor osobně používá v analytických a měřících
metodách, nebo jako kalibrační etalony).
Tento výběr může být snad poněkud subjektivní
- uvítám připomínky a návrhy kolegů..!..
*) Nemá význam se zde zabývat např. extrémně
krátkodobými radionuklidy, které nelze nijak použít
- mohou být zajímavé nanejvýš z hlediska jaderné fyziky,
studia silně nerovnovážných jaderných konfigurací.
U
jednotlivých radionuklidů uvádíme a ve spektrech zobrazujeme
především relevantní energetické hladiny a
radiaci, kterou je možno detekovat dostupnou radiometrickou
technikou. Intenzitu záření číselně
uvádíme v procentech (např.
"gama 320keV (10%)" znamená, že "na 100 přeměn
příslušného radionuklidu se emituje 10 fotonů gama o energii
320keV"). Velké množství dalších,
málo saturovaných hladin a velmi slabě zastoupených
radiačních energií, jakož i další jejich charakteristiky (jako je spin, multipolarita, parita, které jsou
důležité pouze pro jaderný výzkum) je
možno nalézt v podrobných rozpadových tabulkách isotopů. Na
našem pracovišti jsme používali především knižní
vydání "Table of isotopes" autorů Lederer,
Hollander, Perlman (nová
elektronická verze je "http://ie.lbl.gov/toipdf/toi20.pdf"). Další
nové podrobné tabulky v elektronické verzi jsou "http://ie.lbl.gov/toi/nucSearch.asp" ("Lund univ.") a "http://www.nucleide.org" z "Laboratoře Henri Becquerel".
Krátkodobé a
hlouhodobé radionuklidy
Jedním z hlavních faktorů, rozhodujícím o významu a
použití radionuklidů, je poločas rozpadu.
Jak bylo uvedeno výše v části "Přírodní
radionuklidy" mají tyto
přírodní radionuklidy (primordiální a kosmogenní) velmi
dlouhé poločasy rozpadu. Rovněž naprostá většina
významných umělých radionuklidů používaných ve vědě a
technice či průmyslu, mají dostatečně dlouhý
poločas rozpadu - měsíce, roky, desítky let i více,
což umožňuje jejich dlouhodobé používání především ve
formě uzavřených zářičů.
Výjimkou jsou některé krátkodobé
radionuklidy používané v nukleární
medicíně, které díky svým chemickým a
farmakokinetickým vlastnostem nacházejí uplatnění v
radionuklidové diagnostice či terapii ve formě otevřených
zářičů - značených radiofarmak,
aplikovaných přímo do organismu (většinou
intravenózně či perorálně, viz kap.4 "Scintigrafie", §4.9 "Klinická
scintigrafická diagnostika v nukleární medicíně"). V tomto případě může
být krátký poločas rozpadu naopak výhodou z
hlediska radiační zátěže organismu.
Takovými krátkodobými radionuklidy jsou
především technecium 99mTc (T1/2=6hod.) a dále lehké pozitronové
radionuklidy: uhlík 11C (T1/2=20,4min.), dusík 13N (T1/2=10min.), kyslík 15O (T1/2=122sec.) a především fluor 18F
(T1/2=110min.),
který se ve formě 18F-deoxyglukózy vychytá a hromadí zvláště v
nádorových tkáních, které se pak na základě koincidenční
detece anihilačního záření gama 511keV
zobrazují pomocí pozitronové emisní tomografie
(viz §4.3 "Tomografické
kamery" a §4.8 "Radionuklidy
a radiofarmaka pro scintigrafii",
část "Pozitronové radionuklidy"). Jejich vlastnosti, rozpadová schémata a spektrum
511keV budou uvedena níže (pasáž "Dusík,
kyslík, fluor"). Nejkrátkodobějším radionuklidem používaným v
nukleární medicíně je metastabilní krypton
81mKr s
poločasem pouhých 13,1 sekundy.
 Vodík
Vodík 
Nejlehčí a nejrozšířenější prvek v přírodě (vesmíru)
je vodík H1 (hydrogenum
- vodu tvořící),
jehož jádra protony vznikly těsně po velkém
třesku v hadronové éře vesmíru (§1.1, část "Kosmická
nukleogeneze"); podílí se 75% na celkové hmotě ve
vesmíru. Je hlavním "palivem" termonukleární fúze
v nitru hvězd ("Gravitace a evoluce hvězd", část "Termonukleární reakce v nitru
hvězd"). Je
velmi reaktivní, takže v pozemské přírodě se vyskytuje
prakticky pouze ve sloučeninách (elementární
vodík se vyskytuje pouze v zemním plynu a sopečných plynech), z nichž nejdůležitější je
voda H2O. Spolu s uhlíkem je vodík
nejdůležitějším biogenním
prvkem. Má
tři důležité isotopy (celkově jsou
známy isotopy 1H1
až 7H1). Základní "lehký" vodík 1H1 (zvaný někdy
též protium) - relativní zastoupení 99,9885%, "těžký" vodík deuterium 2H1
(0,0115%) a "supertěžký" vodík tritium 3H1
(kosmogenní nuklid se stopovým zastoupením), který je již
radioaktivní.
Vodík 1H
je, jak již bylo
zmíněno, hlavním "palivem" termonukleární fúze v
nitru hvězd. V jaderných technologiích jsou jádra vodíku protony hlavními ostřelujícími částicemi v
jaderném výzkumu, při přípravě umělých radioisotopů (viz výše "Výroba umělých radionuklidů"), v
protonové radioterapii (§3.6, část
"Hadronová
radioterapie").
Deuterium 2H
- těžší isotop
vodíku, vzniklo těsně po začátku vesmíru při primordiální nukleosyntéze (je
podrobněji analyzováno v části "Leptonová
éra. Prvotní kosmologická nukleosyntéza" §5.4 monografie "Gravitace,
černé díry a fyzika prostoročasu"). Deuterium je dalším neradioaktivním
isotopem důležitým v jaderné a radiační fyzice. Jádra
deuteria deuterony d=2H se často používají jako ostřelující částice v
cyklotronech. Těžká voda se používá někdy jako moderátor
a chladicí médium ve štěpných jaderných reaktorech (§1.3, část "Jaderné reaktory"). Spolu s tritiem
představuje deuterium nejperspektivnější palivo pro
řízenou termonukleární fúzi (§1.3,
část "Slučování atomových jader");
přímou termonukleární fúzi vodíkových jader 1H=protonů v
pozemských podmínkách zatím nedovedeme uskutečnit.
Tritium
3H
Pomineme-li volný neutron (který je b--radioaktivní no®p++e-+n´ s poločasem »13min., max.
energie beta 782keV), je nejlehčím radionuklidem isotop vodíku
tritium 3H, který se s poločasem 12,3roku
přeměňuje b--radioaktivitou na základní stav
isotopu hélia 3He: 3H1®3He2+e-+n´(jeho jednoduché rozpadové
schéma je na obr.1.4.7 vlevo). Tritium je čistý
beta-zářič s poměrně nízkou maximální energií
emitovaných elektronů 18,6 keV (červená
křivka na obr.1.4.7 vpravo).

Obr.1.4.7. Beta- - radioaktivita některých nejjednodušších
isotopů.
Vlevo: Přeměnová schémata tritia 3H, uhlíku 14C a fosforu 32P. Vpravo:
Spojitá spektra záření beta těchto radionuklidů.
Pozn.1:
Energetická osa je nelineární a nepravidelná (jen
ilustrativní), aby do jednoho grafu bylo možno zakreslit
energeticky velmi rozdílná spektra.
Pozn.2: Spektra byla měřena
přístrojem MarkIII Nuclear Chicago s toluenovým kapalným
scintilátorem (§.2.6, část "Kapalné scintilátory", obr.2.6.2), vynesena graficky a (s úpravami)
proložena.
Pozn.3: Tvar nízkoenergetické části
spektra (plynulý růst od nulových hodnot - což se poněkud
liší od skutečného tvaru počáteční části spektra b- - srov. §1.2, pasáž "Rozdíl energetického spektra b- a b+", spektrum v levé části obrázku) je ovlivněn
nízkou citlivostí přístroje pro nízké energie beta a
elektronickou filtrací signálu pro omezení šumových
impulsů.
V pozemské přírodě se tritium stopově
vyskytuje jako kosmogenní radionuklid (viz výše část "Přírodní
radionuklidy", nebo §1.6, část
"Kosmické záření", pasáž "Sekundární kosmické
záření"). Vzniká dále při
tzv. ternárním štěpení těžkých jader,
především uranu (§1.3, část "Štěpení
atomových jader"). Obsah tritia v přírodě byl v posledních několika
desítiletích výrazně ovlivněn lidskou činností. K velkému
zvýšení obsahu 3H v životním prostředí došlo v 60.letech v
důsledku zkoušek termonukleárních zbraní v atmosféře (při termonukleárním výbuchu deuteridu lithného 6Li2H vzniká tritium
reakcí 6Li(n,a)3H - viz §1.3, část
"Slučování atomových jader",
pasáž "Explozívní termonukleární reakce"). Ve štěpných jaderných reaktorech tritium vzniká v
cirkulující chladící vodě reakcí neutronů s deuteriem 2H(n,g)3H; v malé míře s
deuteriem obsaženým v běžné vodě, účinněji pak při
použití těžké vody jako moderátoru a chladiva. Dále, v
chladicí vodě obsahující kyselinu boritou pro regulaci
reaktivity štěpného reaktoru vzniká tritium reakcí 10B(n,2a)3H. Při provozu
jaderných elektráren se tedy do vodních a plynných výpustí
dostává určité menší množství 3H (řádově setiny kosmogenního
tritia).
Tritium
je vhodným budícím radionuklidem v malých elektrických
zdrojích - betavoltaických článcích
- viz §1.3, pasáž "Radionuklidové voltaické články ("atomové" baterie)".
Pro řadu aplikací v jaderné fyzice (především pro termonukleární fúzi,
v budoucnu pravděpodobně pro energetické využití - §1.3
"Jaderné reakce a jaderná energie", část "Slučování
atomových jader"), v biologii a medicíně, se tritium vyrábí uměle
pomocí reakce neutronů s lithiem: 6Li(n,a)3H,
nebo se získává z těžké vody v reaktorech.
 Hélium
Hélium 
Druhý nejlehčí a nejrozšířenější prvek ve vesmíru hélium
He2 ("prvek boha Slunce") vzniklo v leptonové
éře po velkém třesku (primordiální nukleosyntéza je
podrobněji analyzována v části "Leptonová
éra. Prvotní kosmologická nukleosyntéza" §5.4 monografie "Gravitace,
černé díry a fyzika prostoročasu").
Na Zemi je však vzácné - důvody jsou uvedeny v §1.1, část
"Kosmická nukleogeneze". Veškeré hélium v pozemské přírodě je
produktem radioaktivního alfa-rozpadu uranu a thoria. Za
normálních podmínek je hélium chemicky inertní plyn,
který vzhledem k vemi nízké teplotě zkapalnění (-269,9oC=4,2oK) má důležité
uplatnění v kryogenní technice, především
v supravodivých elektromagnetech. Má dva stabilní
isotopy: 4He (98,999863%) a 3He (0,000137%). Hélium-4 je velmi
silně vázané jádro, neboť má zaplněné obě slupky
protonů a neutronů, které jsou nejnižší. Radioaktivní
isotopy hélia nemají žádný praktický význam, neboť jsou velmi
krátkodobé *). Ze 7 známých radioisotopů hélia je
"nejstabilnější" 5He (vznikající ozařováním berylia neutrony: 9Be4+1n0®6He2+4He2), které má poločas
jen 0,81sec! V jaderné fyzikce je však hélium (4He) důležité jako účinné
chladící médium (supravodivé elektromagnety
urychlovačů a tokamaků, chlazení citlivých detektorů) a
též jako produkt termonukleární fúze
vodíku (§1.3 "Jaderné reakce a
jaderná energie", část "Slučování
atomových jader"). Jádra hélia - částice alfa - jsou
podstatou alfa-radioaktivity.
*) Diproton:
pro jadernou fyziku má určitou
zajímavost nejkrátkodobější isotop hélia 2He2,
zvaný též diproton 2p - skládá se ze dvou
protonů, bez neutronů. Tento stav je velice nestabilní a
prakticky okamžitě se rozpadá emisí protonů nebo beta+-rozpadem. Samostatný
diproton nebyl pozorován, jen u vysoce excitovaných stavů
např. 18Ne
byla pozorována současná emise dvou protonů, která se
interpretovala jako pocházející z krátkodobého vázaného
stavu 2p.
 Lithium,
Berylium, Bór
Lithium,
Berylium, Bór 
Prvky této skupiny, navzdory tomu že patří k velmi
lehkým, jsou z astrofyzikálních důvodů v přírodě
poměrně málo zastoupené. Vznikly totiž, jako primordiální
prvky, v malém množství v prudce expandujícím
vesmíru na konci leptonové éry ("Leptonová éra. Prvotní kosmologická
nukleosyntéza") a v pozdější hvězdné nukleosyntéze se již
nevytvářejí, ale naopak se spalují (§1.1,
část "Kosmická alchymie - jsme potomky
hvězd!", pasáž "Zastoupení prvků v
přírodě" a §4.1 "Úloha gravitace
při vzniku a evoluci hvězd", část "Evoluce
hvězd" knihy "Gravitace,
černé díry a fyzika prostoročasu").
 Lithium
Li3 je velmi měkký lehký kov z alkalické skupiny (je to nejlehčí kov a zároveň nejlehčí prvek v
pevném skupenství za pokojové teploty),
chemicky značně reaktivní, takže se v přírodě vyskytuje
jen ve sloučaninách. Má dva stabilní isotopy 6Li (7,5%) a 7Li (92,5%). I když
lithium nemá žádné významné dlouhodobější radionuklidy (nejdelší poločas 0,84s. má 8Li), je tento prvek v jaderné
fyzice důležitý. 6Li slouží jako neutronový absorbátor a zdrojový
materiál pro produkci tritia v řízené
termonukleární fúzi (§1.3, část
"Tokamak"). Směs lithia a deuteria -
lithium-6 deuterid 6Li2H byl zneužit jako palivo "vodíkové" termonukleární
bomby (§1.3, část "Slučování
atomových jader",
pasáž "Termojaderný výbuch").
Lithium
Li3 je velmi měkký lehký kov z alkalické skupiny (je to nejlehčí kov a zároveň nejlehčí prvek v
pevném skupenství za pokojové teploty),
chemicky značně reaktivní, takže se v přírodě vyskytuje
jen ve sloučaninách. Má dva stabilní isotopy 6Li (7,5%) a 7Li (92,5%). I když
lithium nemá žádné významné dlouhodobější radionuklidy (nejdelší poločas 0,84s. má 8Li), je tento prvek v jaderné
fyzice důležitý. 6Li slouží jako neutronový absorbátor a zdrojový
materiál pro produkci tritia v řízené
termonukleární fúzi (§1.3, část
"Tokamak"). Směs lithia a deuteria -
lithium-6 deuterid 6Li2H byl zneužit jako palivo "vodíkové" termonukleární
bomby (§1.3, část "Slučování
atomových jader",
pasáž "Termojaderný výbuch").
 Berylium
Be4 je tvrdý šedý kov, který ve vlhku snadno oxiduje, v
přírodě se vyskytuje vzácně (cca 3-10mg/kg v zemské kůře)
ve sloučeninách, např. ve smaragdu. Využívá se ve
speciálních slitinách v metalurgii. V jaderné fyzice se
využívá jeho nízká absorpce (vysoká propustnost)
pro nízkoenergetické X a gama záření - beryliová vstupní okénka
citlivých detektorů. Z berylia se též zhotovují některé
úseky trubic v urychlovačích, ve kterých dochází k
interakcím částic - aby vylétající částice snadněji (bez větší absorpce) pronikly k
detektorům.Ve směsi s a-radionuklidy slouží berylium jako laboratorní zdroj
neutronů (viz např. pasáž "Neutronové
záření a jeho interakce" v
§1.6). Berylium má jediný stabilní
isotop 9Be. Z radioaktivních isotopů berylia
mají určitou přírodovědnou důležitost dva kosmogenní
radionuklidy :
Berylium
Be4 je tvrdý šedý kov, který ve vlhku snadno oxiduje, v
přírodě se vyskytuje vzácně (cca 3-10mg/kg v zemské kůře)
ve sloučeninách, např. ve smaragdu. Využívá se ve
speciálních slitinách v metalurgii. V jaderné fyzice se
využívá jeho nízká absorpce (vysoká propustnost)
pro nízkoenergetické X a gama záření - beryliová vstupní okénka
citlivých detektorů. Z berylia se též zhotovují některé
úseky trubic v urychlovačích, ve kterých dochází k
interakcím částic - aby vylétající částice snadněji (bez větší absorpce) pronikly k
detektorům.Ve směsi s a-radionuklidy slouží berylium jako laboratorní zdroj
neutronů (viz např. pasáž "Neutronové
záření a jeho interakce" v
§1.6). Berylium má jediný stabilní
isotop 9Be. Z radioaktivních isotopů berylia
mají určitou přírodovědnou důležitost dva kosmogenní
radionuklidy :
Berylium 7Be se s poločasem 53,3 dne
přeměňuje elektronovým záchytem na
stabilní isotop 7Li - v 89,5% na základní stav, v 10,5% na excitovanou
hladinu 478keV, při jejíž deexcitaci je emitováno záření
gama o této energii. Isotop 7Be vzniká v přírodě působením kosmického
záření v atmosféře. Jsou to hlavně tříštivé reakce
vysokoenergetických protonů s jádry dusíku 14N(p,2a)7Be nebo kyslíku 16O(p,10B)7Be, dále jadernými
reakcemi neutronů s jádry dusíku 14N(n,8Li)7Be a kyslíku 16O(n,10B)7Be. Jeho detekce se využívá ke zkoumání
transportních dějů v atmosféře. Pro výzkumné účely v
jaderné fyzice se isotop 7Be uměle připravuje ozařováním lithia urychlenými
protony v cyklotronu reakcí 7Li(p,n)7Be. Pro jadernou fyziku je isotop 7Be zajímavý tím, že se u něj poprve prokázala
závislost rychlosti radioaktivní přeměny elektronovým
záchytem na chemickém stavu isotopu - viz §1.2, část "Elektronový záchyt",
pasáž "Dvě zvláštnosti EC".
Berylium 10Be se s poločasem 1,6.106roků přeměňuje b--radioaktivitou
na stabilní isotop 10B v základním stavu. V atmosféře vzniká působením
kosmického záření reakcí s uvolněnými neutrony: 14N(n,pa)10Be. Atomy 10Be se v atmosféře
zachytávají na aerosolových částicích a se srážkovou
vodou se dostávají na zemský povrch, kde se usazují v půdě,
oceánech a ledovcích. Měření této depozice 10Be (pomocí
hmotnostní spektrometrie), vzhledem k jeho dlouhému poločasu,
se využívá ke sledování některých geologických a
oceánografických procesů.
Velmi skrytou (hluboko v nitru masívních
hvězd) přírodní důležitost má jeden
velmi krátkodobý isotop berylia :
Berylium 8Be, vzhledem ke svému extrémně
krátkému poločasu 6,7.10-17sekundy, je z hlediska "pozemské" jaderné
fyziky zcela bezvýznamné. Prakticky okamžitě po svém vzniku
se berylium-8 rozpadá na 2 částice alfa (jádra hélia). Je
však velmi důležité z hlediska jaderné astrofyziky:
přes Be-8 probíhá jaderné "hoření" hélia na
uhlík v pozdních stádiích vývoje masívních hvězd. Ve
specifických podmínkách vysokých teplot a tlaků v nitru
hmotných hvězd bohatých na hélium (po "vyhoření"
vodíku) i tak krátká doba života 8Be stačí k tomu, aby záchytem jader 4He v 8Be mohlo vznikat
velké množství uhlíku 12C - je diskutováno v §4.1 "Úloha gravitace
při vzniku a evoluci hvězd", část "Evoluce
hvězd", pasáž "Spalování
hélia" knihy "Gravitace,
černé díry a fyzika prostoročasu".
 Bór
B5 je polokovový prvek, který se v pozemské přírodě
vyskytuje pouze ve sloučeninách. Má dva stabilní isotopy: 10B
(19,9%) a 11B (80,1%). I když bór nemá žádné
použitelné radionuklidy (všechny jsou
velmi krátkodobé, nejdelší 0,77s. má 8B), je tento prvek velmi
důležitý v jaderných technologiích. Vysoký
účinný průřez isotopu 10B pro absorpci pomalých neutronů jej činí velmi
vhodným materiálem pro řídící tyče v jaderných
reaktorech, nebo přidávání kyseliny borité do
chladicí vody pro řízení reaktivity (§1.3,
část "Jaderné reaktory").
Bór
B5 je polokovový prvek, který se v pozemské přírodě
vyskytuje pouze ve sloučeninách. Má dva stabilní isotopy: 10B
(19,9%) a 11B (80,1%). I když bór nemá žádné
použitelné radionuklidy (všechny jsou
velmi krátkodobé, nejdelší 0,77s. má 8B), je tento prvek velmi
důležitý v jaderných technologiích. Vysoký
účinný průřez isotopu 10B pro absorpci pomalých neutronů jej činí velmi
vhodným materiálem pro řídící tyče v jaderných
reaktorech, nebo přidávání kyseliny borité do
chladicí vody pro řízení reaktivity (§1.3,
část "Jaderné reaktory").
 Uhlík
Uhlík 
Uhlík C6 (Carboneum) je velmi důležitý prvek ve vesmíru, kde vzniká
termonukleární fúzí hélia v nitru masívních hvězd (§1.1, pasáž "Jsme potomky
hvězd!", podrobněji
"Termonukleární syntéza v nitru hvězd"). U masivních hvězd 2. a následujících generací se
uhlík též účastní termonukleární fúze vodíku na hélium
(jako "katalyzátor" - CNO
cyklus). C6 je čtvrtým nejrozšířenějším prvkem ve vesmíru.
Atomárně je uhlík nekovový prvek, který se kromě amorfní
formy vyskytuje v několika krystalických strukturách: grafit
(tuha - šestiúhelníková struktura), diamant (krychlová struktura, tvořící
velmi tvrdé, opticky průzračné krystaly), fulleren
(sférické "molekuly" ze sítí uhlíkových atomů,
např. C60).
Mimořádně důležitý je uhlík v pozemské
přírodě (obsah v zemské kůře cca
200-800 mg/kg), kde se vyskytuje
převážně ve sloučeninách, z nichž nejdůležitější je
plynný oxid uhličitý CO2 (cca 0,04% v zemské atmosféře
- je důležitý pro fotosyntézu v rostlinách), z nerostů pak uhličitan vápenatý CaCO3. CO2 a některé další
uhlíkové plyny (např. metan) vykazují značně vysokou reflexní schopnost pro
tepelné infračervené záření ("skleníkový
efekt") a působí tak jako
termoregulační složka v atmosféře Země i jiných planet.
Díky specifické konfiguraci atomového obalu je
uhlík schopen tvořit obrovské množství druhů tzv. "organických"
sloučenin s vodíkem, kyslíkem, dusíkem,
fosforem a dalšími prvky, často za vzniku velmi dlouhých,
rozvětvených a cyklických molekul. Díky těmto velmi
rozmanitým kombinacím, které spolu mohou vzájemně opět
reagovat za vzniku dalších složitých specifických látek, se
sloučeniny uhlíku staly základním stavebním kamenem živé
hmoty - uhlík je základní biogenní prvek.
Uhlík má řadu isotopů (8C - 22C), z nichž stabilní jsou jen dva isotopy 12C
(98,93%) a 13C (1,07%). Důležité jsou dva
radioisotopy uhlíku :
Uhlík 14C
Z radioaktivních isotopů uhlíku je nejdůležitější radiouhlík
14C6, který se s poločasem rozpadu 5730 let
přeměňuje b--radioaktivitou 14C ® 14N + e- + n´ na základní
stav dusíku 14N7.
14C je čistý
beta-zářič s maximální energií emitovaných
elektronů 156,5 keV (modrá křivka v
pravé části obr.1.4.7 uvedeného výše v pasáži 3H). V přírodě se vyskytuje jako významný kosmogenní
radionuklid, který vzniká účinkem neutronů,
vyrážených kosmickým zářením z jader atomů, na dusík ve
vyšších vrstvých zemské atmosféry: no + 14N7 ® 14C6 + p+ (viz
§1.6, část "Kosmické záření", obr.1.6.7). Je na něm založena radikarbonová
metoda určování stáří archeologických předmětů
(popsaná výše v části "Radioisotopové
(radiometrické) datování",
pasáž "Radiouhlíková datovací metoda").
Obsah radiouhlíku-14 v
přírodě je ovlivňován i lidskou činností. V menší míře
dochází ke snižování obsahu 14C v životním prostředí spalováním fosilních
paliv, ze kterých v průběhu miliónů let původní obsah
14C již
vymizel radioaktivním rozpadem; CO2 vznikající spalováním fosilního paliva tedy 14C neobsahuje a
zastoupení přírodního radioaktivního 14CO2 se tak zřeďuje. Jaderné technologie obsah
radiouhlíku-14 naopak zvyšují. Obsah 14C značně vzrostl v
60.letech při zkouškách jaderných zbraní v důsledku
jaderné reakce 14N(n,p)14C účinkem neutronů, uvolněných při explozi, na
dusík. Menší množství radiouhlíku 14C vzniká dále při provozu štěpných jaderných
reaktorů jadernou reakcí 17O(n,a)14C na kyslíku v chladící vodě a reakcí 14N(n,p)14C na dusíku
rozpuštěném v chladící vodě; z chladící vody se
odvětráváním toto malé množství 14CO2 dostává přes ventilační komíny elektrárny do
ovzduší.
Podobně
jako tritium, i radiouhlík 14C se vyrábí uměle neutronovou aktivací 14N(n,p)14C v jaderném
reaktoru pro mnohé aplikace, zvláště biologické,
především stopovací metody (§3.5
"Radioisotopové
stopovací metody").
Uhlík 11C
Dalším poněkud významným radioisotopem uhlíku je
krátkodobý pozitronový 11C, který se s poločasem 20,36
min. přeměňuje převážně beta+-radioaktivitou
(99,75%) a v malé míře elektronovým záchytem (0,25%) na
základní stav boru 11B. Používá se (poměrně zřídka) v pozitronové
emisní tomografii (§4.3 "Kamery PET", §4.8 "Radionuklidy
a radiofarmaka pro scintigrafii"). Isotop 11C se připravuje v cyklotronu buď ozařováním bóru
urychlenými deuterony v reakcích 10B(d,n)11C, 11B(d,2n)11C (probíhajících současně s
oběma stabilními isotopy přírodního bóru), nebo ozařováním dusíku protony: 14N(p,a)11C.
Zmíníme v této
souvislosti další tři lehké pozitronové radionuklidy,
používané v pozitronové emisní tomografii :
 Dusík,
Kyslík, Fluor
Dusík,
Kyslík, Fluor 
 Dusík
N7 (Nitrogenium) je za normální teploty inertní plynný prvek,
tvořící hlavní část zemské atmosféry (78% objemových).
Při -195°C přechází do kapalného skupenství; kapalný
dusík je velmi důležité kryogenní médium.
Spolu s uhlíkem, vodíkem a kyslíkem patří dusík mezi
důležité biogenní prvky, jakožto součást aminokyselin
tvořících bílkoviny. Dusík má dva stabilní
isotopy 14N
(99,64%) a 15N (0,36%). Radioaktivní isotopy dusíku mají poměrně
krátké poločasy, kratší než 10 minut. Za zmínku stojí dva
z nich :
Dusík
N7 (Nitrogenium) je za normální teploty inertní plynný prvek,
tvořící hlavní část zemské atmosféry (78% objemových).
Při -195°C přechází do kapalného skupenství; kapalný
dusík je velmi důležité kryogenní médium.
Spolu s uhlíkem, vodíkem a kyslíkem patří dusík mezi
důležité biogenní prvky, jakožto součást aminokyselin
tvořících bílkoviny. Dusík má dva stabilní
isotopy 14N
(99,64%) a 15N (0,36%). Radioaktivní isotopy dusíku mají poměrně
krátké poločasy, kratší než 10 minut. Za zmínku stojí dva
z nich :
Dusík 13N
se s poločasem T1/2=9,96 min. přeměňuje beta+-radioaktivitou (99,82%) a v malé
míře elektronovým záchytem (0,18%) na základní stav uhlíku
13C.
Isotop 13N
se připravuje v cyklotronu buď ozařováním kyslíku (ve
vodě) urychlenými protony jadernou reakcí 16O(p,a)13N, nebo ozařováním
uhlíku deuterony v reakci 12C(d,n)13N. Dusík 13N se občas používá v pozitronové emisní
tomografii ve formě amoniaku a aminokyselin značených
isotopem 13N.
Pozn.: Isotop 13N sehrál důležitou
úlohu v procesu zkoumání radioaktivity: byl prvním uměle
připraveným radioaktivním isotopem. V r.1934 jej v pokusech
ozařování bóru alfa-částicemi (z polonia) objevili F.Joliot
a I.Curie; vznikal zde reakcí 10B(a,n)13N.
Dusík 16N
se s poločasem T1/2=7,13 sec. přeměňuje beta--radioaktivitou (Ebmax=4290keV a 10420keV) na základní stav (28%) a na
vysoce excitované stavy 6130keV (67%) a 7115keV (5%) kyslíku 16O. Při deexcitaci
jsou emitovány vysokoenergetické fotony 6,13MeV a 7,1MeV.
Isotop 16N
vzniká reakcí 16O(n,p)16N rychlých neutronů se základním isotopem kyslíku 16O, především v
chladící vodě primárního okruhu jaderných reaktorů
chlazených vodou. Aktivita isotopu 16N v cirkulující chladící vodě je úměrná počtu
neutronů v aktivní zóně reaktoru, tedy intenzitě řetězové
štěpné reakce (počtu probíhajících štěpení za sekundu)
a tepelnému výkonu reaktoru. Měření aktivity 16N pomocí
gama-detektorů, přiložených z vnější strany k
cirkulačnímu potrubí chladící vody primárního okruhu,
proto může monitorovat správnou funkci reaktoru.
 Kyslík O8 (Oxygenium) je za normální teploty reaktivní plynný prvek,
tvořící 21% (objemových) zemské atmosféry. Spolu s uhlíkem
a vodíkem je nejdůležitějším biogenním
prvkem. Má tři stabilní isotopy: 16O (99,76%), 17O (0,04%), 18O (0,2%). Radioaktivní isotop 15O se někdy používá v pozitronové emisní tomografii
:
Kyslík O8 (Oxygenium) je za normální teploty reaktivní plynný prvek,
tvořící 21% (objemových) zemské atmosféry. Spolu s uhlíkem
a vodíkem je nejdůležitějším biogenním
prvkem. Má tři stabilní isotopy: 16O (99,76%), 17O (0,04%), 18O (0,2%). Radioaktivní isotop 15O se někdy používá v pozitronové emisní tomografii
:
Kyslík 15O
se s poločasem T1/2=122sec. přeměňuje beta+-radioaktivitou (99,82%) a v malé
míře elektronovým záchytem (0,12%) na základní stav dusíku
15N.
Isotop 15O
se připravuje v cyklotronu buď ozařováním dusíku
(obohaceného isotopem 15N) urychlenými deuterony jadernou reakcí 15N(d,2n)15O, nebo ozařováním
kyslíku protony v reakci 16O(p,pn)15O. Jeho použití v PET je poměrně ojedinělé,
vzhledem ke krátkému poločasu.
 Fluor F9 je za normální teploty zelenožlutý plyn, velmi
reaktivní, takže se na Zemi vyskytuje pouze ve sloučeninách.
Patří do skupiny halogenů - prvků
tvořících soli (řec. halos=sůl). Je poměrně hojně rozšířený (540mg/kg v zemské kůře). Má
jediný stabilní isotop 19F. Radioaktivní isotop 18F je velmi hojně využíván v
pozitronové emisní tomografii :
Fluor F9 je za normální teploty zelenožlutý plyn, velmi
reaktivní, takže se na Zemi vyskytuje pouze ve sloučeninách.
Patří do skupiny halogenů - prvků
tvořících soli (řec. halos=sůl). Je poměrně hojně rozšířený (540mg/kg v zemské kůře). Má
jediný stabilní isotop 19F. Radioaktivní isotop 18F je velmi hojně využíván v
pozitronové emisní tomografii :
Fluor
18F
se s poločasem T1/2=110min. přeměňuje beta+-radioaktivitou (96,86%) a elektronovým
záchytem (3,14%) na základní stav kyslíku 18O. Isotop 18F se připravuje v
cyklotronu nejčastěji ozařováním kyslíku (ve vodě obohacené isotopem 18O) urychlenými protony v reakci 18O(p,n)18F, méně často
ozařováním stlačeného neonu urychlenými deuterony jadernou
reakcí 20Ne(d,a)18F. V pozitronové
emisní tomografii PET se používá většinou
ve formě 18F-fluor-deoxyglukózy (FDG - §4.8 "Radionuklidy a radiofarmaka
pro scintigrafii", část "Pozitronové radionuklidy").
Pozitronové
radionuklidy
Všechny pozitronové radionuklidy, pokud jsou obsažené v
látkovém prostředí (což je prakticky
vždy), při anihilaci
emitovaných pozitronů s elektrony e++e-®2g vysílají
gama-záření o energii 511keV (§1.2, část "Radioaktivita b+" a §1.6, část "Interakce nabitých částic -
přímo ionizující záření ", obr.1.6.1 dole). Gama-spektrum "čistých" pozitronových
radionuklidů, lehkých o kterých jsme zatím pojednali, je
tvořeno jediným anihilačním e+e- píkem 511keV *) o intenzitě blízké
200% - u 11C (199,5%), 13N (199,6%), 15O (199,7%), 18F (193,7%). U některých dalších (těžších) pozitronových
radionuklidů je zastoupení pozitronů nižší než 100% a tím
pádem i intenzita anihilačního záření je často podstatně nižší
než 200% - viz např. 22Na (180,7%), 58Co (29,8%), 64Cu (35%), 68Ga (177,8%), 89Zr (45,6%); bývají
přítomné i další gama-píky.
*) Stojí za zajímavost, že anihilační gama pík 511keV je ve
spektru ve srovnání s okolními "jadernými"
fotopíky o něco širší v důsledku Dopplerovského
rozšíření způsobeného různou rychlostí zabrzdění
pozitronů v látce před anihilací s elektrony (je diskutováno v §1.2, pasáž "Spektrum záření gama"). Toto rozšíření činí
jen cca 1,2keV a projevuje se pouze na polovodičových spektrech
(v našich podrobných spektrometrických
měřeních jsme je jasně pozorovali, avšak na níže
zobrazených silně zmenšených a kontrahovaných spektrech tyto
rozdíly viditelné nejsou...).
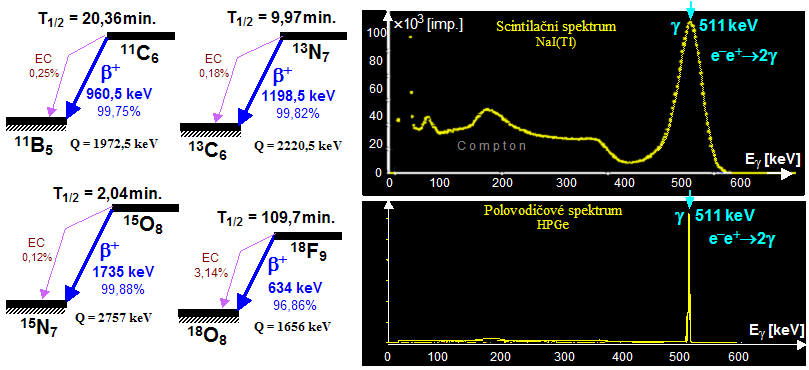
Přeměnová schémata pozitronových radionuklidů 11C,
13N, 15O, 18F a gama-spektrum
jejich anihilačního záření 511keV.
Pozitronové radionuklidy se používají
především v nukleární medicíně ve formě
vhodných radiofarmak, které se vychytávají a hromadí
zvláště v nádorových tkáních, jejichž ditribuce se pak na
základě koincidenční detece dvojic fotonů
anihilačního záření gama 511keV zobrazuje pomocí pozitronové
emisní tomografie PET (viz §4.3
"Tomografické kamery" a §4.8 "Radionuklidy a radiofarmaka
pro scintigrafii", část "Pozitronové radionuklidy"). Z výše zmíněných
lehkých pozitronových radionuklidů se široce používá pouze
fluor 18F, další pozitronové radionuklidy
(C-11, N-13, O-15) jen ojediněle, vzhledem k jejich krátkému
poločasu.
V
našem pojednání uvedeme řadu dalších důležitých
lehčích, středně těžkých a nakonec i těžkých nuklidů :
 Fosfor ,
Síra
Fosfor ,
Síra 
Jsou to důležité biogenní prvky, hojně zastoupené v zemské
kůře, mořské vodě i v živých organismech.
 Fosfor P15 (lat. Phosphorus) je poměrně rozšířený
nekovový prvek - obsah v zemské kůře cca 1g/kg. Čistý
fosfor se vystykuje v několika alotropních modifikacích, z
nichž nejznámější jsou tři nazývané podle barevného
vzhedu: Bílý (nažloutlý) fosfor tvořený molekulami P4,
který je měkký a vysoce reaktivní, zvláště s kyslíkem (může dojít k samovznícení). Červený fosfor s polymerní
strukturou, který je relativně stabilní. Černý fosfor s
vrstevnatou polymerní strukturou je nejstabilnější a vykazuje
i kovové elektrické, tepelné a optické vlastnosti. V
přírodě se však fosfor vyskytuje pouze ve sloučeninách.
Fosfor P15 (lat. Phosphorus) je poměrně rozšířený
nekovový prvek - obsah v zemské kůře cca 1g/kg. Čistý
fosfor se vystykuje v několika alotropních modifikacích, z
nichž nejznámější jsou tři nazývané podle barevného
vzhedu: Bílý (nažloutlý) fosfor tvořený molekulami P4,
který je měkký a vysoce reaktivní, zvláště s kyslíkem (může dojít k samovznícení). Červený fosfor s polymerní
strukturou, který je relativně stabilní. Černý fosfor s
vrstevnatou polymerní strukturou je nejstabilnější a vykazuje
i kovové elektrické, tepelné a optické vlastnosti. V
přírodě se však fosfor vyskytuje pouze ve sloučeninách.
Fosfor je velmi důležitý biogenní prvek nacházející se ve všech buňkách
rostlinných a živočišných. Je vazebnou fosfátovou složkou
genetických biomolekul DNA a RNA, energetických molekul
adenozintrifosfát, fosfolipidové buněčné membrány (§5.2, část "Buňky - základní jednotky živých
organismů"). V kostech je uložen ve fosforečnanu
vápenatém, hydroxiapatitu.
Fosfor má jediný
stabilní isotop 31P. Z řady radioaktivních isotopů 24-46P má většina
krátké poločasy (minuty, sekundy,
milisekundy). Díky delšímu poločasu
mají význam jen dva radioisotopy fosforu :
Fosfor
32P
se s poločasem 14,27 dní přeměňuje beta--radioaktivitou (Ebmax= 1710 keV)
na síru 32S
v základním stavu, je to čistý beta zářič. V
přírodě isotop 32P v nepatrném množství vzniká jako kosmogenní
radionuklid v atmosféře jadernými reakcemi sekundárních
neutronů z kosmického záření. Uměle se vyrábí v jaderném
reaktoru ozařováním fosforu v reakci 31P(n,g)32P, nebo ozažováním síry-32 rychlými neutrony
reakcí 32S(n,p)32P .
Radioaktivní 32P se používá jako radioindikátor v
laboratorních metodách molekulární biologie a genetiky pro
radioaktivní značkování. 32P-fosfátové skupiny se vestaví do geneticky
důležitých molekul nukleotidů, DNA, RNA, které pak mohou
být sekvenovány a radiometricky (autoradiograficky) detekovány
- §2.2, pasáž "Autoradiografie". 32P může být též využíván pro diagnostiku a
terapii nádorových onemocnění - nádorové buňky mají
tendenci vychytávat více sloučenin fosforu než normální
buňky.
Radiofosfor 32P, jakožto čistý beta-radionuklid, se používal pro
léčbu hematologických maligních onemocnění ( i.v. aplikace cca 200-500MBq ve formě fosfátu), především polycytemie - §3.6
"Radioisotopová terapie", pasáž "Léčba hematologických
onemocnění radiofosforem 32P".
Fosfor
33P
se s poločasem 32,97 dní přeměňuje beta--radioaktivitou (Ebmax= 248 keV) na síru 33S v základním stavu.
Radioaktivní 33P se používá v podobných laboratorních aplikacích
jako fosfor-32, v metodách kde je výhodná nižší energie
elektronů beta (např. lepší
rozlišovací schopnost u Autoradiografie).

Přeměnová schémata radionuklidů 32P,
33P, 35S
a jejich beta-spektra (na spektrum beta se
vztahuje tatáž poznámka jako u obr.1.4.7).
 Síra S16 (lat. Sulphur) je rovněž
značně reaktivní nekovový prvek a proto se v přírodě
vyskytuje především ve sloučeninách, hlavně v sulfidech. Obsah v zemské kůře cca
0,03-0,09 %, koncentrace v mořské vodě cca 880
mg/litr. Jako čistý prvek se vyskytuje
při vulkanické činnosti, kde krystalizuje z horkých
sopečných plynů obsahujících sirné výpary. Teplota tání
115°C, teplota varu 445°C. I síra je důležitým biogenním prvkem, je součástí aminokyselin
(cystein, methionin) tvořících bílkoviny.
Síra S16 (lat. Sulphur) je rovněž
značně reaktivní nekovový prvek a proto se v přírodě
vyskytuje především ve sloučeninách, hlavně v sulfidech. Obsah v zemské kůře cca
0,03-0,09 %, koncentrace v mořské vodě cca 880
mg/litr. Jako čistý prvek se vyskytuje
při vulkanické činnosti, kde krystalizuje z horkých
sopečných plynů obsahujících sirné výpary. Teplota tání
115°C, teplota varu 445°C. I síra je důležitým biogenním prvkem, je součástí aminokyselin
(cystein, methionin) tvořících bílkoviny.
Má
čtyři stabilní isotopy: 32S (94,99%), 33S (0,75%), 34S (4,25%) a 36S (0,019%). Z radioaktivních isotopů síry má
praktické uplatnění jeden :
Síra
35S
se s poločasem 87,25 dní přeměňuje beta--radioaktivitou (Ebmax= 167,3 keV) na chlór 35Cl v základním stavu. Podobně jako 32P, i síra 35S vzniká v
nepatrném množství v atmosféře jako kosmogenní radionuklid.
Isotop 35S
se uměle připravuje v jaderném reaktoru ozařováním chlóru (chloridu draselného) neutrony
reakcí 35Cl(n,p)35S.
Radioaktivní sírou značené aminokyseliny 35S-cystein a 35S-methionin se v
biochemickém výzkumu používají ke studiu metabolismu
aminokyselin.
 Sodík ,
Draslík
Sodík ,
Draslík 
Sodík a draslík jsou nejběžnější prvky z řady alkalických
kovů, hojně zastoupené v zemské kůře, mořské
vodě i v živých organismech. Jsou to měkké (lze je
krájet nožem),
lehké (plavou na vodě), stříbřitě lesklé kovy,
snadno tavitelné (sodík má teplotu
tání 97,7°C, draslík 63,4°C). Jsou velmi reaktivní (zvlášť bouřlivě reagují s vodou), takže se v přírodě
vyskytují jen ve sloučeninách.
 Sodík Na11 (lat. Natrium) je nejrozšířenější
alkalický prvek - obsah v zemské kůře 2,4-2,6 %,
koncentrace v mořské vodě 10,5 g/litr. Sodík patří mezi biogenní prvky a nachází se ve všech buňkách
rostlinných a živočišných tkání, jakož i v
extracelulární tekutině...
Sodík Na11 (lat. Natrium) je nejrozšířenější
alkalický prvek - obsah v zemské kůře 2,4-2,6 %,
koncentrace v mořské vodě 10,5 g/litr. Sodík patří mezi biogenní prvky a nachází se ve všech buňkách
rostlinných a živočišných tkání, jakož i v
extracelulární tekutině...
Má jediný stabilní isotop 23Na. Z radioaktivních
isotopů má význam především sodík-22 :
Sodík
22Na
se s poločasem 2,6 roků přeměňuje
dominantně beta+-radioaktivitou
(90%, Ebmax=500keV) a
částečně elektronovým záchytem (10%) na 22Ne v excitovaném
stavu 1275keV; při deexcitaci jsou emitovány fotony gama o
téže energii 1275keV. Jen v 0,056% probíhá přeměna na
základní stav 22Ne. Isotop 22Na se připravuje v cyklotronu buď ozařováním
kovového hořčíku deuterony v jaderné reakci 24Mg(d,a)22Na, nebo
ozařováním fluoru alfa-částicemi v reakci 19F(a,n)22Na.
V gama spektru sodíku-22 dominuje anihilační
pík 511keV (180%), v oblasti vyšších energií je
výrazný pík 1274keV (100%).

Přeměnové schéma a gama-spektrum sodíku 22Na .
Radionuklid 22Na se používá především jako laboratorní zdroj
pozitronů pro atomovou a jadernou fyziku (viz např. §1.5, část "Antičástice - antiatomy - antihmota -
antisvěty", pasáž
"Umělá výroba antihmoty") a pro materiálovou analýzu vzorků *). U některých
PET kamer uzavřené zářiče Na-22 slouží jako kalibrační a
adjustační zdroje anihilačního gama záření 511 keV (vedle 18F vzorků a Ge68-Ga68 etalonů ) - viz §4.3, část "Pozitronová
emisní tomografie PET".
*) Analýza materiálů pomocí pozitronů,
tzv. pozitronová anihilační spektrometrie (stručně popsaná v §3.3, pasáž "Pozitronová anihilační spektrometrie"), je založena na chování
pozitronů při průchodu zkoumanou látkou. Vyšetřuje se doba
života pozitronu, t.j. časový úsek mezi jeho vznikem v
beta+-radioaktivitě 22Na (indikovaný emisí fotonu
1275keV) a zánikem (doprovázeným
vyzářením anihilačních fotonů 511keV),
čímž lze získat informace o strukturních nepravidelnostech -
dislokace, vakance, nečistoty v krystalové struktuře.
 Alkalický kov draslík K19 (lat. Kalium) je rovněž velmi
reaktivní a proto se v přírodě vyskytuje pouze ve
sloučeninách. Obsah
v zemské kůře cca 2,0-2,4 %, koncentrace v mořské vodě
cca 380 mg/litr. I draslík je biogenním
prvkem.......
Alkalický kov draslík K19 (lat. Kalium) je rovněž velmi
reaktivní a proto se v přírodě vyskytuje pouze ve
sloučeninách. Obsah
v zemské kůře cca 2,0-2,4 %, koncentrace v mořské vodě
cca 380 mg/litr. I draslík je biogenním
prvkem.......
Má dva stabilní isotopy 39K (93,3%) a 41K (6,73%). Přírodní draslík obsahuje též 0,0017%
dlouhodobého radioaktivního isotopu 40K:
Draslík
40K
je všeobecně rozšířeným přírodním
(primárním) radionuklidem s velice dlouhým poločasem rozpadu 1,25.109roků.
Přeměňuje se rozvětveně beta--radioaktivitou (89%) na
základní stav vápníku 40Ca a elektronovým záchytem
(11%) na argon 40Ar - na jeho excitovaný stav 1460 keV. Oba tyto
dceřinné isotopy jsou stabilní, další rozpad již
nepokračuje. Charakteristický pík gama 1460 keV
(10,5%) draslíku je dobře patrný při všech
spektrometrických měřeních přírodních vzorků s
akviziční dobou několika hodin (srov.
výše uvedený obr.1.4.2 v
části "Přírodní radionuklidy").

Přeměnové schéma a gama-spektrum
draslíku 40K.
 Skandium
Skandium 
Skandium Sc21 (název pochází z jeho objevu ve Skandinávii -
L.F.Nilson, r.1879, Švédsko) je stříbřitě bílý měkký a lehký
kov poněkud podobný hliníku, jeho zastoupení v zemské kůře
je asi 5-2mg/kg. Má poměrně malé
využití, používá se ve slitinách s hliníkem. Má jediný stabilní isotop 45Sc. Z asi 25 známých
radioaktivních isotopů scandia má perspektivní uplatnění v
nukleární medicíně 44Sc a 47Sc :
Scandium
44Sc
Přeměňuje se s poločasem 3,97 hodin
dominantně beta+-radioaktivitou
(94%, Eb+max=1474keV) a částečně elektronovým záchytem
(5,7%) na 44Ca v excitovaném stavu 1157keV (vyšší
excitované hladiny 2656 a 3301 keV jsou zastoupeny jen slabě); při deexcitaci jsou emitovány fotony gama
především o této energii 1157keV. V gama spektru skandia-44
dominuje anihilační pík 511keV (188%), v
oblasti vyšších energií je výrazný pík 1157keV (99,8%); slabé vyšší g-píky 1499, 2144, 2556 a 3301 keV jsou vidět až při
silném zvětšení.
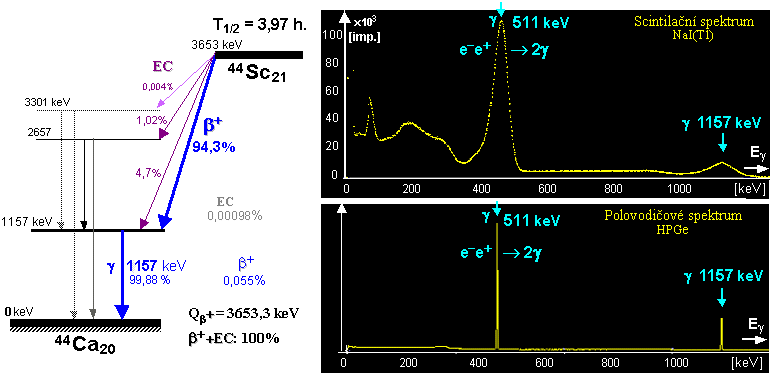
Přeměnové schéma a gama-spektrum skandia 44Sc .
Pozitronový radionuklid 44Sc má perspektivní
použití v nukleární medicíně pro scintigrafické zobrazení
metodou pozitronové emisní tomografie PET (viz §4.3 "Tomografické
kamery" a §4.8 "Radionuklidy a radiofarmaka
pro scintigrafii", část "Pozitronové radionuklidy"). Trojmocné skanium se
dobře navazuje, pomocí osvědčených bifunkčních
chelatačních činidel typu DOTA, na vektorové
biomolekuly, hlavně monoklnální protilátky. Oproti 18F a hlavně 68Ga je výhodný též
delší poločas téměř 4 hodiny, umožňující zobrazovat i
pomocí těžších biomolekul s pomalejší farmakokinetikou.
Může být též použit teranosticky v kombinaci s
analogickými terapeutickými radiofarmaky značenými 90Y, 177Lu, nebo ideálně 47Sc.
Jeho velkou výhodou je způsob výroby:
Může být sice produkován jadernou reakcí 44Ca(p,n)44Sc na malém
cyklotronu, avšak na pracovištích nukleární medicíny může
být (bez nutnosti cyklotronu) 44Sc průběžně a dlouhodobě získáváno elucí z 44Ti/44Sc
generátoru :
Mateřský titan 44Ti pro generátor se získává na
cyklotronu jadernou reakcí 45Sc(p,2n)44Ti. V kolonce generátoru se mateřský 44Ti s dlouhým poločasem
60,4 let přeměňuje elektronovým záchytem na
dceřinné 44Sc, které se vhodným roztokem (H2C2O4+HCl) vymývá - eluuje. Vzhledem k dlouhému poločasu
mateřského 44Ti (cca 130 000-krát delší než
dceřinný 44Sc) se v generátoru udržuje sekulární
rovnováha (viz pasáž "Radionuklidové
generátory"), takže se dlouhodobě, po mnoho let, může každý
den eluovat potřebné 44Sc o stejné aktivitě, dané aktivitou výchozího 44Ti (......... ....)
.......
Vzhledem k těmto výhodným
vlastnostem lze očekávat, že skandium 44Sc možná postupně nahradí dosavadní
hlavní PET radionuklidy 18F a 68Ga ..?..
Určitou nevýhodou 44Sc je souběžná emise vysokoenergetického záření
gama 1157keV, které zvyšuje radiační dávku pacientů a
pracovníků PET. Objevují se proto úvahy o použití
sousedního radionuclidu scandia 43Sc (T1/2 3,89hod., beta+ 88%, gama 373keV (23%)), který má vlastnosti podobné
jako 44Sc,
ale vykazuje mnohem nižší energii a intenzitu doprovodného
záření gama ...
Scandium
47Sc
S poločasem 3,35 dní se přeměňuje beta--radioaktivitou na 47Ti (což je stabilní nuklid), v
31,6% na základní stav a v 68,4% na excitovanou hladinu 159keV.
Max. energie elektronů beta pro oba tyto případy činí 600keV
a 441keV, střední energie beta je 162keV. Gama spektrum 47Sc je tvořeno
jediným píkem 159keV (68%).

Přeměnové schéma a gama-spektrum skandia 47Sc .
Isotop 47Sc lze připravovat neutronovými reakcemi 47Ti(n,p)47Sc, 46Ca(n,p)47Ca.. ... 47Sc .... ... v
jaderném reaktoru, nebo v cyklotronu reakcemi 48Ca(p,2n)47Sc, 46Ca(p,g)47Sc, ........
Skandium 47Sc je perspektivním beta- radionuklidem
pro terapii v nukleární medicíně. Přitom
gama záření 159 keV lze s výhodou použít pro scintigrafické
zobrazení (planární/SPECT) a monitorování
radionuklidové terapie. Sekvence 44Sc/47Sc může být výbornou teranostickou
dvojicí isotopů pro PET zobrazování + radionuklidovou
terapii.
 Chrom ,
Železo
Chrom ,
Železo 
 Chrom Cr24 je světle bílý tvrdý kov, odolný
vůči korozi. Je poměrně hojně zastoupený v pozemské
přírodě (v zemské kůře cca 0,1-0,2
g/kg). Používá se
především v metalurgii jako legující přísada či k
pokovování. Má 4 stabilní isotopy: 50Cr (4,35%), 52Cr (85,8%), 53Cr (9,5%), 52Cr (85,8%), 54Cr (2,37%). Z radioaktivních isotopů
našel praktické uplatnění jeden:
Chrom Cr24 je světle bílý tvrdý kov, odolný
vůči korozi. Je poměrně hojně zastoupený v pozemské
přírodě (v zemské kůře cca 0,1-0,2
g/kg). Používá se
především v metalurgii jako legující přísada či k
pokovování. Má 4 stabilní isotopy: 50Cr (4,35%), 52Cr (85,8%), 53Cr (9,5%), 52Cr (85,8%), 54Cr (2,37%). Z radioaktivních isotopů
našel praktické uplatnění jeden:
Chrom
51Cr
Přeměňuje se s poločasem 27,7 dní elektronovým
záchytem na stabilní isotop 51V - v 90% přeměn je to na základní a v 10% na
vzbuzený stav 320keV, při jehož deexcitaci se emitují fotony
gama o téže energii. Velmi jednoduché gama-spektrum chromu-51
je tvořeno jediným fotopíkem 320keV (10%). Ve
srovnání s většinou ostatních beta(EC)-gama radionuklidů
je, v přepočtu na aktivitu, 51-chrom poměrně slabým
gama-zářičem, cca 10-x slabším než třebas cesium 137Cs, kobalt 60Co či radiojód 131I. Isotop 51Cr se připravuje
jadernou reakcí 50Cr(n,g)51Cr ozařováním chrómu (obohaceného
na cca 80% isotopem 50Cr) neutrony v jaderném reaktoru.
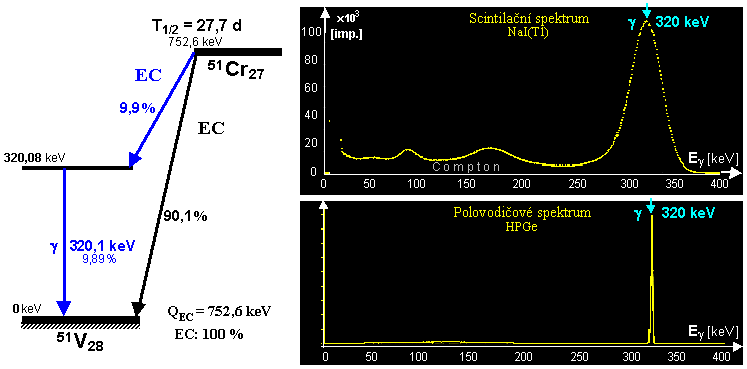
Rozpadové schéma a gama-spektrum chromu 51Cr.
Radionuklid 51Cr se používá jako stopovací radioindikátor
v některých aplikacích v průmyslu, geologii a v nukleární
medicíně. V nukleární hematologii se 51Cr-chromanovými ionty značí červené krvinky,
příp. i bílé krvinky. Pomocí takto značených autologních
erytrocytů se stanovuje doba života (resp. poločas
přežití) krvinek a příp. místo jejich destrukce (§4.9 "Přežívání a
sekvestrace erytrocytů.").
Použití 51Cr v nukleární medicíně je již téměř opuštěno.
Radionuklid 51Cr
byl též. několikrát použit pro sledování cest podzemní
vody. Do ponorného pramene se nalil roztok radiochrómu, načež
se z několika blízkých vodních toků odebíraly vzorky vody a
měřily se na citlivém studnovém scintilačním detektoru -
zda se v nich objeví, za jak dlouho a v jakém množství,
radioaktivita 51Cr.
 Železo
Fe26 (Ferrum) je feromagnetický
kovový prvek, poměrně hojně zastoupený v přírodě (4-6% v
zemské kůře). Tento všeobecně známý kov je základním
konstrukčním materiálem ve strojírenství, stavebnictví,
elektrotechnice a řadě dalších technických oborů, jakož i
v domácnosti a běžném životě. Má čtyři stabilní
isotopy: 54Fe
(5,8%), 56Fe
(91,7%), 57Fe
(2,2%) a 58Fe
(0,28%). Z mnoha radioaktivních isotopů železa mají
praktický význam dva:
Železo
Fe26 (Ferrum) je feromagnetický
kovový prvek, poměrně hojně zastoupený v přírodě (4-6% v
zemské kůře). Tento všeobecně známý kov je základním
konstrukčním materiálem ve strojírenství, stavebnictví,
elektrotechnice a řadě dalších technických oborů, jakož i
v domácnosti a běžném životě. Má čtyři stabilní
isotopy: 54Fe
(5,8%), 56Fe
(91,7%), 57Fe
(2,2%) a 58Fe
(0,28%). Z mnoha radioaktivních isotopů železa mají
praktický význam dva:
Železo 55Fe
se přeměňuje s poločasem 2,74 roků elektronovým
záchytem na základní stav manganu 55Mn. Emituje se
přitom chrakteristické X-záření Ka,b o
energiích kolem 6keV. Zářiče 55Fe o dostatečně vysoké aktivitě se používají jako
zdroje měkkého X-záření pro rentgen-fluorescenční
analýzu lehkých prvků (lehčích než mangan), např.
v geologickém průzkumu hornin.
Železo 59Fe
Přeměňuje se s poločasem 44,5 dní beta--radioaktivitou
na stabilní kobalt 59Co, převážně na excitované stavy 1099keV (53%) a
1292keV (45%). Při deexcitaci je emitováno g záření
především o těchto dvou energiích (s
nízkým zastoupením pak 142, 192, 335, 1482 keV). Používalo se při ferokinetických testech
v hematologii v nukleární medicíně ke studiu
metabolismu železa v souvislosti s procesy tvorby červených
krvinek při anemii či leukemii (§4.9.9., pasáž "Vyšetření
kinetiky železa pomocí 59Fe"). V rostlinné biologii se
isotop 59Fe
používal pro sledování příjmu železa z půdy a živných
roztoků a jeho ukládání v různých částech rostlin.
 Kobalt
Kobalt 
Kobalt Co27 je feromagnetický kovový prvek
poměrně podobný železu, jeho zastoupení v zemské kůře je
asi 25mg/kg. Jeho hlavní využití je v
metalurgii. Má
jediný stabilní isotop 59Co. Nejdůležitějšími radioisotopy
kobaltu jsou 60Co a 57Co:
Kobalt
60Co
Ze středně těžkých radionuklidů je široce využíván
zvláště kobalt 60Co jako zdroj tvrdého záření gama
energií 1173+1332keV pro radioterapii
(§3.6, část "Isocentrická radioterapie"), defektoskopii
(§3.3, část "Radiační defektoskopie") a další technické
aplikace. 60Co se s poločasem 5,27 let
přeměňuje beta--radioaktivitou
na excitované stavy niklu 60Ni (což je stabilní nuklid). Je to především, v
99,88%, hladina 2506keV, která se kaskádově deexcituje nejprve
na hladinu 1332,5keV, ta pak na základní stav 60Ni. Spektrum
záření gama je tvořeno dvěma píky 1173 a 1332 keV, ve
scintilačním spektru se výrazně zobrazuje též spojité
Comptonovsky rozptýlené záření.
Isotop
60Co se
připravuje neutronovým ozařováním kovového kobaltu v
jaderném reaktoru reakcí 59Co(n,g)60Co.
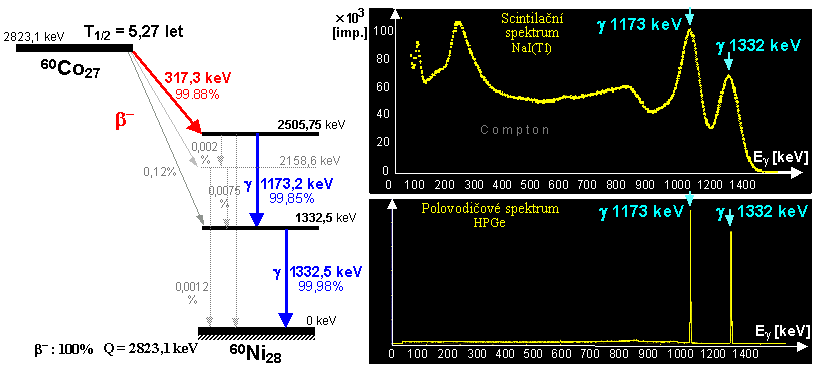
Přeměnové schéma a gama-spektrum
kobaltu 60Co.
Kobalt
57Co
Dalším důležitým radioisotopem kobaltu je 57Co,
který se používá jako zdroj měkčího záření gama 122+136 keV. 57Co se s poločasem 271,8 dní
přeměňuje elektronovýn záchytem na
excitované hladiny 706,4keV (0,18%) a především 136,5keV
(99,82%) železa 57Fe. Nejvíce saturovaná hladina 136,5keV se v 10%
deexcituje na základní stav 57Fe a v 85,5% na hladinu 14,4keV za emise hlavní energie
gama 122keV. Po elektronovém záchytu jsou při
přeskocích elektronů mezi L a K slupkou emitovány fotony
charakteristického X-záření Ka,b železa o
energiích 6,4-7,1 keV,
dále konverzní a Augerovy elektrony. Gama-spektrum 57Co je tvořeno
především hlavním píkem 122keV (85,5%), s nižším
sousedním píkem 136keV (11%); v oblasti
vyšších energií je až po velkém zvětšení vidět velmi
slabý pík 692keV (0,16%).
Isotop
57Co se
připravuje deuteronovým ozařováním kovového železa v
cyklotronu jadernou reakcí 56Fe(d,n)57Co.

Přeměnové schéma a gama-spektrum kobaltu 57Co.
57Co se
používá jako zdroj gama záření pro Mösbauerovu
spektrometrii železa a jeho sloučenin (§3.4, část "Mössbauerovská
spektroskopie"). V nukleárné medicíně se používal vitamin B12 značený 57Co pro stanovení příjmu tohoto vitaminu střevní
resorpcí (§4.9.9, pasáž "Schillingův
test").
Oba
zmíněné radionuklidy kobaltu 57,60Co se též využívají jako etalonové
zářiče gama. Pro blízkost energie záření gama
122keV s energií 140keV 99mTc se bodové zdroje 57Co používají jako pointery
při scintigrafii a plošné homogenní zdroje 57Co se používají
pro seřizování a testování homogenity zorného pole
scintilačních gamakamer (viz "Fantomy
a fantomová měření v nukleární medicíně").
Kobalt 58Co
Pro radioisotopovou diagnostiku v nukleární medicíně se v
60.-80.letech používal kobalt 58Co, který se s poločasem 70,8 dní elektronovým
záchytem (84%) a b+-radioaktivitou (15%) přeměňuje na excitované stavy
železa 58Fe - 811keV (84+15%) a 1675keV (1,2%). Při
deexcitaci se emitují fotony gama převážně o energii 811keV
(99,4%), s mnohem menší intenzitou 864keV (0,7%) a 1675keV
(0,5%). V jaderné fyzice se někdy používá jako zdroj
pozitronů. V nukleární medicíně se v 70.-80.letech
používal vitamin B12
značený 58Co, podobně jako výše uvedeným 57Co.
Všechny tyto metody jsou nyní již opuštěny.
 Nikl 56Ni
--> Kobalt 56Co
Nikl 56Ni
--> Kobalt 56Co
Poněkud atypickým způsobem zde uvádíme tyto dva vzájemně
navazující radionuklidy, které jsou důležité v jaderné
astrofyzice při výbuchu supernov :
Nikl 56Ni
podle astrofyzikálních analýz vzniká v kolosálním
množství (řádově hmotnosti naší
zeměkoule..!..) při výbuchu supernov,
především termonukleárních supernov typu Ia
- je popsáno v §4.2, části "Výbuch supernovy. Neutronová hvězda.
Pulsary." monografie
"Gravitace, černé díry a fyzika prostoročasu".
56Ni se s poločasem 6,1 dní přeměňuje
elektronovým záchytem na excitovanou hladinu
1,72 MeV kobaltu 56Co. Při deexcitaci přes tři nižší hladiny je
emitováno gama záření o energiích 158keV (99%), 269keV
(37%), 480keV (36%), 750keV (49%), 812keV (86%), 1562keV (15%).
Dceřinný 56Co je také radioaktivní :
Kobalt 56Co
se s poločasem 77,27 dní přeměňuje beta+-radioaktivitou (20%, Eb+max=1,49 MeV) a elektronovým
záchytem (80%) na poměrně vysoké excitované stavy
železa 56Fe (2085keV
(20%), 3120keV (15%), 3451keV (21%), 3830keV (15%), 4050keV
(24%), 4300keV (1,4%)), které je
stabilní. Při deexcitaci se emituje tvrdé gama záření o
mnoha energiích, z nichž výraznější jsou 847keV (100%),
977keV (1,4%), 1038keV (14%), 1175keV (2,3%), 1238keV (67%),
1360keV (4,3%), 1771keV (15%), 2015keV (3,1%), 2035keV (8%),
2598keV (17%), 3009keV (1%), 3202keV (3,2%), 3253keV (8%),
3451keV (1%).

Přeměnové schéma a gama spektrum 56Ni a 56Co (spektrum přijde změřit a
rozpadové schéma upřesnit až získám vzorek 56Ni...).
Oba tyto radionuklidy 56Ni a 56Co svým
radioaktivním rozpadem v supernovách emitují obrovské
množství energie, díky němuž supernova může mnoho
dní zářit jasností miliard Sluncí (pasáž
"Záření supernov.
Světelná křivka. Spektrum záření") ..!..
Pro technické ani laboratorní aplikace nemají
tyto radionuklidy žádný význam.
 Měď ,
Galium , Germanium , Selen
Měď ,
Galium , Germanium , Selen 
 Měď Cu29 (Cuprum) je všeobecně známý
žlutočerveně lesklý kov s velmi dobrou elektrickou a tepelnou
vodivostí. Obsah v zemské kůře činí cca 50-70mg/kg,
čistá kovová měď se vyskytuje jen ojediněle, většinou se
nachází ve sloučeninách - sulfidech, oxidech, v kombinaci se
sloučeninami železa a dalších. Vedle metalurgie (slitiny s cínem - bronz, nebo zinkem - mosaz), strojírenství a
stavebnictví, je hlavní použití mědi v elektrotechnice, díky výborné elektrické
vodivosti a též odolnosti vůči korozi. Měď má dva
stabilní isotopy 63Cu (69,15%) a 65Cu (30,85%). Některé radioaktivní
isotopy mědi se sporadicky používají nebo zkoušejí v
nukleární medicíně (především PET scintigrafii) a
biochemických studiích: 61Cu (T1/2=3,3hod.,
b+,EC), 62Cu (T1/2=9,7min., b+,EC), 64Cu(T1/2=12,7hod.,
b+,EC), 67Cu (T1/2=61,8hod., b-,g) . Perspektivní se jeví dva radionuklidy mědi :
Měď Cu29 (Cuprum) je všeobecně známý
žlutočerveně lesklý kov s velmi dobrou elektrickou a tepelnou
vodivostí. Obsah v zemské kůře činí cca 50-70mg/kg,
čistá kovová měď se vyskytuje jen ojediněle, většinou se
nachází ve sloučeninách - sulfidech, oxidech, v kombinaci se
sloučeninami železa a dalších. Vedle metalurgie (slitiny s cínem - bronz, nebo zinkem - mosaz), strojírenství a
stavebnictví, je hlavní použití mědi v elektrotechnice, díky výborné elektrické
vodivosti a též odolnosti vůči korozi. Měď má dva
stabilní isotopy 63Cu (69,15%) a 65Cu (30,85%). Některé radioaktivní
isotopy mědi se sporadicky používají nebo zkoušejí v
nukleární medicíně (především PET scintigrafii) a
biochemických studiích: 61Cu (T1/2=3,3hod.,
b+,EC), 62Cu (T1/2=9,7min., b+,EC), 64Cu(T1/2=12,7hod.,
b+,EC), 67Cu (T1/2=61,8hod., b-,g) . Perspektivní se jeví dva radionuklidy mědi :
Měď
64Cu ,
která se s poločasem 12,7 hod. přeměňuje beta+ radioaktivitou (17,5%) a elektronovým
záchytem (44%) na základní (53%) a excitovaný (0,5%)
stav 64Ni
; dále beta- radioaktivitou (38,5%) na základní
stav 64Zn.
....... V gama spektru 64Cu dominuje (jako u každého
pozitronového radionuklidu) e-e+
anihiliční pík 511keV (35%), v oblasti
vyšších energií je až při výrazném zvětšení vidět
slabý pík 1345,7keV (0,47%).

Přeměnové schéma a gama spektrum mědi 64Cu (vzorek Cu-64 pro
spektrometrické měření laskavě poskytli Mgr.A.Čepa a
Ing.J.Červenák z ÚJV Řež)
Pozitronový radionuklid Cu-64 se občas
používá v pozitronové emisní tomografii ("§4.3 "Pozitronová
emisní tomografie PET",
§4.8 "Radionuklidy a
radiofarmaka pro scintigrafii",
pasáž "Radionuklidy a
radiofarmaka pro PET"). Komplex 64Cu-ATSM (acetyl-methyl-thiosemikarbazon) se rychle a
selektivně vychytává v hypoxických tkáních, používá se
pro diagnostiku hypoxie myokardu a mozku, jakž i nádorové
hypoxie. 64Cu-TETA-octreotid
umožňuje PET zobrazení neuroendokrinních nádorů. Zkouší
se též pro značení monoklonálních protilátek, např. 64Cu-DOTA-cetuximab,
peptidu bombesin.........
Měď
67Cu
se s poločasem 61,8 hod. přeměňuje beta- radioaktivitou na základní (20%) a
excitované stavy stavy zinku 64Zn, při jejich deexcitacích je emitováno gama
záření o energiích 91keV (7%), 93keV (16%), 185keV (49%);
tři další vyšší energie do 393keV jsou slabé, <1%.
.......
....... obrázek - rozpadové schéma +gama
spektrum ..........
Kombinace označení téhož biochemického nosiče isotopem Cu-64
pro diagnostiku PET a Cu-67 pro terapii
beta-zářením jsou slibné pro teranostiku v
nukleární medicíně....
 Galium Ga36 je měkký velmi lehce tavitelný kov (taje již při 30°C) světlé modrošedé barvy. Vyskytuje se
poměrně vzácně (zastoupení v zemské
kůře cca 15 mg/kg).
Jeho hlavní použití je v elektronice jako složka řady
polovodičových materiálů při výrobě tranzistorů a světlo
emitujících diod (LED). Má dva stabilní isotopy 69Ga
(60,1%) a 71Ga (39,9%). Z radioaktivních isotopů
se používají dva:
Galium Ga36 je měkký velmi lehce tavitelný kov (taje již při 30°C) světlé modrošedé barvy. Vyskytuje se
poměrně vzácně (zastoupení v zemské
kůře cca 15 mg/kg).
Jeho hlavní použití je v elektronice jako složka řady
polovodičových materiálů při výrobě tranzistorů a světlo
emitujících diod (LED). Má dva stabilní isotopy 69Ga
(60,1%) a 71Ga (39,9%). Z radioaktivních isotopů
se používají dva:
Galium
67Ga
se s poločasem 3,26 dní přeměňuje elektronovým
záchytem na excitované stavy 67Zn o energiích především 93keV (52,5%), 184keV
(22,7%) a 393keV (23,6%), na základní stav jde jen 3%. Při
deexcitacích dceřinného 67Zn jsou emitovány fotony záření gama o energiích
především 93, 184 a 393 keV. Spektrum záření gama
radionuklidu 67Ga sestává především ze tří hlavních linií
93keV (38%), 184kev (21%) a 300keV (17%), slabší je linie
394keV (5%). V oblasti vyšších energií
jsou slabé píky 494, 794 a 887 keV (zastoupení kolem 0,1%),
viditelné ve spektru jen při silném zvětšení.
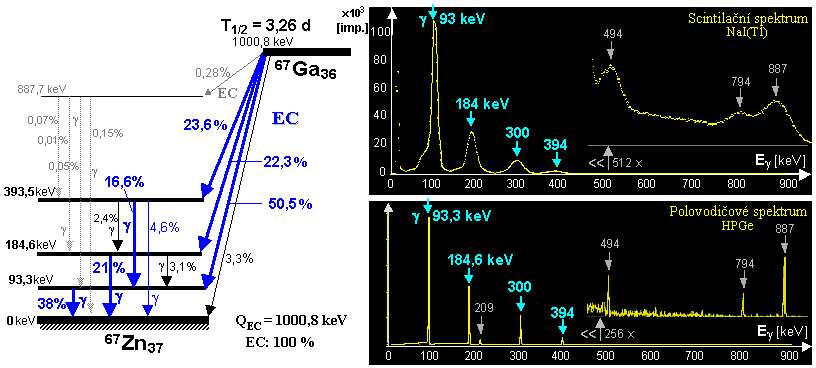
Rozpadové schéma a gama-spektrum galia 67Ga.
Isotop 67Ga se připravuje ozařováním zinku nebo mědi v
cyklotronu urychlenými protony, deterony nebo jádry hélia (a-částicemi) jadernými reakcemi:
67Zn(p,n)67Ga, 68Zn(p,2n)67Ga, 67Zn(d,2n)67Ga, 65Cu(a,2n)67Ga.
67Ga
se používá v nukleární medicíně (ve formě komplexu galium-citrát)
pro zobrazení míst v tkáních a orgánech, postižených zánětlivými
procesy nebo nádorovými ložisky (§4.8 "Radionuklidy a radiofarmaka pro
scintigrafii").
Galium
68Ga
se s poločasem 67,7 minut přeměňuje elektronovým záchytem
(8,7%) a především b+-radioaktivitou (87,9%) na 68Zn, nejčastěji na
základní stav (jen něco přes 1%
přeměn je do excitovaných stavů 67Zn, hlavně na hladinu 1077keV). V
gama spektru galia-68 dominuje (jako u
každého pozitronového radionuklidu) e-e+ anihiliční
pík 511keV (178%), v oblasti vyšších energií jsou
až při velkém zvětšení vidět slabé píky 1077 (3%), 1261 (0,1%) a 1883 (0,14%) keV.

Přeměnové schéma a gama-spektrum galia 68Ga .
Radiofarmaka značená 68Ga se používají v
nukleární medicíně pro zobrazení metodou PET
("§4.3 "Pozitronová emisní tomografie PET", §4.8 "Radionuklidy a radiofarmaka pro
scintigrafii", pasáž "Radionuklidy a radiofarmaka pro PET"). Isotop 68Ga se na
pracovištích nejčastěji získává z germanium-galiových generátorů
68Ge/68Ga (zmíněných
kousek níže v pasáži "Germanium 68Ge", včetně germaniového fantomu
pro PET kamery). Galium 68Ga je do určité
míry "PET analog" obvyklého technecia 99mTc u planární a
SPECT scintigrafie. Umožňuje chelatační navázání na celou
řadu radiofarmak, včetně lehčích monoklonálních
protilátek (jejich Fab fragmentů). Zatím se
nejčastěji používá pro zobrazení neuroendokrinních
nádorů (somatostatinové receptory -
značené octreotidy typu 68Ga-DOTATOC a jeho derivátů).
Velmi perspektivní se jeví PET zobrazování nádorů prostaty
pomocí značeného prostatického membránového antigenu
68Ga-PSMA (J591,
617, I&T, ...), s následnou biologicky
cílenou radionuklidovou terapií pomocí téže
monoklonální protilátky antiPSMA, značené beta či alfa
radionuklidy.
Zkouší se též
zobrazování peptidových receptorů exprimujících gastrin - bombesinových
receptorů, pomocí např. 68Ga-DOTA-PEG2-bombesin,
68Ga-BZH3. Dále receptorů
epidermálního růstového faktoru HER pomocí
značeného fragmentu Fab trastuzumabu, též receptorů vaskulárního
endotelového růstového faktoru VEGF. 68Ga-Annexin může sloužit pro PET pro
zobrazování apoptózy.
Galium-68 je velmi perspektivní diagnostický PET
radionuklid, který má - v kombinaci s terapeutickými
radionuklidy 90Y, 177Lu, 225Ac, 227Th - vysoký teranostický potenciál (je diskutováno v §4.9, pasáž "Kombinace
diagnostiky a terapie - teranostika").
 Germanium
Ge36 je šedobílý pevný polokovový prvek,
který se v přírodě vyskytuje poměrně vzácně (zastoupení v zemské kůře cca 5-7 mg/kg). Jeho hlavní použití je v elektronice jako složka řady polovodičových
materiálů při výrobě tranzistorů, diod, integrovaných
obvodů; pro náš obor jaderné fyziky jsou důležité germaniové polovodičové detektory (Ge(Li), HPGe - §2.5 "Polovodičové detektory"). Germanium má 4 stabilní isotopy: 70Ge (20,4%), 72Ge (27,3%),
73Ge (7,8%) a 74Ge (36,7%).
Přírodní germanium obsahuje též 7,83% velmi dlouhodobého
radioaktivního isotopu 76Ge (T1/2=1,7.1021 roků; jeho radioaktivita je nepatrná, lze jej
považovat za téměř stabilní - viz níže). Z radioaktivních isotopů zmíníme tři - jeden
prakticky vyžívaný, druhý použitý v zajímavém experimentu
a třetí pozoruhodný svým "exotickým" způsobem
rozpadu :
Germanium
Ge36 je šedobílý pevný polokovový prvek,
který se v přírodě vyskytuje poměrně vzácně (zastoupení v zemské kůře cca 5-7 mg/kg). Jeho hlavní použití je v elektronice jako složka řady polovodičových
materiálů při výrobě tranzistorů, diod, integrovaných
obvodů; pro náš obor jaderné fyziky jsou důležité germaniové polovodičové detektory (Ge(Li), HPGe - §2.5 "Polovodičové detektory"). Germanium má 4 stabilní isotopy: 70Ge (20,4%), 72Ge (27,3%),
73Ge (7,8%) a 74Ge (36,7%).
Přírodní germanium obsahuje též 7,83% velmi dlouhodobého
radioaktivního isotopu 76Ge (T1/2=1,7.1021 roků; jeho radioaktivita je nepatrná, lze jej
považovat za téměř stabilní - viz níže). Z radioaktivních isotopů zmíníme tři - jeden
prakticky vyžívaný, druhý použitý v zajímavém experimentu
a třetí pozoruhodný svým "exotickým" způsobem
rozpadu :
Germanium
68Ge
se s poločasem 270,9 dní přeměňuje elektronovým
záchytem na základní stav pozitronového radionuklidu
68Ga. Na
této radioaktivní přeměně je založen 68Ge/68Ga radionuklidový generátor, z
něhož lze na pracovištích nukleární medicíny průběžně
získávat krátkodobý radioisotop galium 68Ga
(poločas 68 minut - obtížná doprava do
míst mimo cyklotron) pro použití v PET
scintigrafii (zmíněný výše 68Ga). Generátor Ge/Ga na principu iontové
chromatografie je podobného typu jako známý Mo/Tc
generátor (popsaný níže - 99mTc). Je to skleněná chromatografická kolonka, v níž je
mateřské 68Ge v nerozpustné formě nasorbováno na oxidu titanu,
hliníku nebo cínu. Zkoušejí se i "bezkovové"
nosiče na organické bázi, jako je trihydrohybenzen
(pyrogalol)-formaldehydová pryskyřice, slibné by mohly být
porézní sorbenty na bázi nanomateriálů (zkoušejí
se nanomateriály se zirkoniem a cerem). Po
radioaktivní přeměně jáder 68Ge na dceřinná jádra 68Ga se vzniklé atomy galia vyvážou z nerozpustné
vazby a mohou být z kolonky eluovány slabým
roztokem kyseliny chlorovodíkové (0,1M). Eluce se dá
provádět opakovaně (několik set krát), s příslušně
klesající aktivitou může generátor sloužit cca 1-3 roky.
Pozitronové galium-68 je tak na pracovišti nukleární
medicíny operativně a dlouhodobě k dispozici pro klinické
použití v PET.
Posloupnost 68Ge--> 68Ga se též využívá v uzavřených
"germaniových" fantomech pro
kalibraci a testování gamakamer PET (viz
"Fantomy
a fantomová měření v nukleární medicíně", pasáž "Tomografické fantomy"). Zdrojem anihilačního
záření 511keV, detekovaného PET kamerou, je zde dceřinné
galium-68 (vzniká při interakci
pozitronů emitovaných 68Ga s elektrony materiálu),
mateřské germanium se na radiaci nepodílí.
Vlastní mateřský isotop 68Ge se připravuje ozařováním isotopů galia v
cyklotronu v jaderných reakcích 69Ga(p,2n)68Ge, 72Ga(p,4n)68Ge, nebo 66Zn(a,2n)68Ge, popř. tříštivými strip-reakcemi (p,p-xn)
vyrážením "x" neutronů z isotopů brómu nebo
germania.
Germanium 71Ge
se s poločasem 11,4 dní přeměňuje elektronovým
záchytem na základní stav 71Ga, je emitováno charakteristické X-záření galia.
Tento isotop se použil v experimentech s radiochemickou detekcí
slunečních neutrin s využitím reakce 71Ga(n,e-)71Ge. Po radiochemickém odsepování vznikajícího
germania se měří charakteristické X-záření a Augerovy
elektrony emitované z atomů galia po přeměně 71Ge elektronovým
záchytem (§1.2, část "Neutrina - "duchové"
mezi částicemi",
pasáž "Detece neutrin").
Germanium 76Ge
se dříve považovalo za stabilní isotop.
Pozdější experimenty prokázaly, že se s obrovsky dlouhým
poločasem 1,7.1021 roků přeměňuje dvojným beta rozpadem b-b- na selen 75Se (§1.2, část "Radioaktivita beta-", pasáž "Dvojný rozpad beta"). .........
 Selen
Se34 je šedobílý polokovový prvek, který
se v přírodě vyskytuje poměrně vzácně (zastoupení v zemské kůře cca 0,005-0,17 mg/kg). Jeho hlavní použití je v elektronice díky jeho význačným fotoelektrickým
vlastnostem - fotoelektrické
články -
a jako složka některých polovodičových materiálů. Selen
má 5 stabilních isotopů: 74Se (0,89%),
76Se (9,37%), 77Se (7,63%),
78Se (23,77%) a 80Se
(49,61%). Přírodní selen obsahuje též 8,73% velmi
dlouhodobého radioaktivního isotopu 82Se (T1/2=1,087.1020 roků; jeho radioaktivita je nepatrná, lze jej
považovat za prakticky stabilní). Z
radioaktivních isotopů našel praktické uplatnění jeden :
Selen
Se34 je šedobílý polokovový prvek, který
se v přírodě vyskytuje poměrně vzácně (zastoupení v zemské kůře cca 0,005-0,17 mg/kg). Jeho hlavní použití je v elektronice díky jeho význačným fotoelektrickým
vlastnostem - fotoelektrické
články -
a jako složka některých polovodičových materiálů. Selen
má 5 stabilních isotopů: 74Se (0,89%),
76Se (9,37%), 77Se (7,63%),
78Se (23,77%) a 80Se
(49,61%). Přírodní selen obsahuje též 8,73% velmi
dlouhodobého radioaktivního isotopu 82Se (T1/2=1,087.1020 roků; jeho radioaktivita je nepatrná, lze jej
považovat za prakticky stabilní). Z
radioaktivních isotopů našel praktické uplatnění jeden :
Selen
75Se
se s poločasem 119,8 dní přeměňuje elektronovým
záchytem (EC) na řadu excitovaných stavů arsenu 75As, převážně na
excitovaný stav s energií 401keV (95,9%); přeměny
na další vyšší excitované stavy mají velmi nízkou
intenzitu (<0,01%). Při kaskádových
deexcitacích se emituje cca 20 energií fotonů gama, z nichž
významnější intenzitu mají energie 121, 136, 264, 279 a 401
keV.

Přeměnové schéma a gama-spektrum selenu 75Se. Omluva:
Polovodičové spektrum bylo měřeno na starším detektoru
Ge(Li) se zhoršenými vlastnostmi.
V gama-spektru 75Se dominují
gama-píky 121 (17%),
136 (58%), 264 (58%), 279 (25%) a 401 (11%) [keV].
Řada dalších vyšších píků v rozmezí 400-822keV je
natolik nízká (<0,01%), že u našeho slabého vzorku (cca 3kBq) se ve spektru
nezobrazily.
Isotop 75Se se připravuje v cyklotronu ozařováním selenu (obohaceného isotopem 74Se) neutrony reakci 74Se(n,g)75Se v jaderném
reaktoru. Používá se jako zdroj záření gama
v průmyslových radiografických aplikacích (§3.3, část "Radiační
defektoskopie") jako alternativa k níže popsanému iridiu 192Ir. 75Se má ve srovnání s iridiem delší poločas rozpadu
a poskytuje měkčí spektrum gama záření (může být vhodné pro defektoskopické testování
tenších kovových vrstev cca 2-3mm, kde nižší gama energie
poskytuje lepší radiografický kontrast).
Selen-75 se ojediněle používá v nukleární
medicíně ve formě 75Se-selenomethioninu, ve kterém je atom
síry v aminokyselině methionin nahrazen atomem
selenu-75. Po intravenózní aplikaci se provádí vyšetření metabolismu
aminokyseliny methioninu a proteosyntézy. V
60.-80.letech se toto radiofarmakum používalo pro
scintigrafickou diagnostiku pankreatu (příjem aminokyselin v pankreatu je odrazem rychlosti
syntézy trávicích enzymů - §4.9.3, pasáž "Scintigrafie
pankreatu"). Též se ojediněle používá 75Se- kyselina tauroselcholová k
diagnostice malabsorpce žlučových kyselin, při hodnocení
snížení absorpční funkce ilea (např. u Crohnovy choroby,
zánětlivého, toxického či radiačního poškození).
Pro použití v nukleární medicíně je nevýhodou
75Se jeho
příliš dlouhý poločas rozpadu (120 dní) ...
 Rubidium
- Krypton -Xenon
Rubidium
- Krypton -Xenon 
 Rubidium Rb37 je lehký měkký lesklý kov ze skupiny
alkalických kovů. Je velmi reaktivní, takže se v přírodě
vyskytuje jen ve sloučeninách (zastoupení
v zemské kůře cca 100-300 mg/kg). Má jediný stabilní isotop 85Rb
(72,17%), v přírodním rubidiu zbylých 27,83% tvoří primordiální
radioaktivní isotop 87Rb (viz níže). Z radioisotopů rubidia mají význam
tři isotopy s diametrálně rozdílnými poločasy:
Rubidium Rb37 je lehký měkký lesklý kov ze skupiny
alkalických kovů. Je velmi reaktivní, takže se v přírodě
vyskytuje jen ve sloučeninách (zastoupení
v zemské kůře cca 100-300 mg/kg). Má jediný stabilní isotop 85Rb
(72,17%), v přírodním rubidiu zbylých 27,83% tvoří primordiální
radioaktivní isotop 87Rb (viz níže). Z radioisotopů rubidia mají význam
tři isotopy s diametrálně rozdílnými poločasy:
Rubidium 81Rb
S poloočasem 4,57 hod. se přeměňuje elektronovým
záchytem (39%) a b+-radioaktivitou (25%) na excitované
stavy kryptonu 81Kr. Nejvíce zastoupená je přeměna za vzniku
metastabilního izomeru 81mKr s energií 191keV a krátkým poločasem 13 sekund.
Uměle vyráběný isotop 81Rb se používá jako mateřský generátorový
nuklid pro přípravu krátkodobého metastabilního
izomeru 81mKr pro scintigrafii plicní ventilace v
nukleární medicíně (viz níže 81mKr). 81Rb se připravuje nejčastěji reakcí 82Kr(p,2n)81Rb ozařováním
kryptonu (příp. obohaceného isotopem 82Kr) protony urychlenými v cyklotronu.
Rubidium
82Rb
S poloočasem 1,27 minut se přeměňuje b+-radioaktivitou
(96%) a elektronovým záchytem (4%) na
základní (87%) a na excitované stavy (především
na hladinu 776keV - 8%) kryptonu 82Kr. Při deexcitaci
se emituje více energií fotonů gama, významnější je pouze
energie 776keV. V gama spektru rubidia-82 dominuje (jako u každého pozitronového radionuklidu) e-e+
anihiliční pík 511keV (191%), patrný je
dále gama pík 776keV (13%) a slabší 1395keV (0,5%); až při
velkém zvětšení jsou vidět další velmi slabé píky až do
3900keV.
.......obrázek.........
..................Spektrum ......
Krátkodobý isotop 82Rb se získává elucí z generátoru 82Sr/82Rb,
jehož mateřský isotop 82Sr má poločas 25,4 dní - viz pasáž "Sr-82". Rubidium-82 se používá experimentálně pro
PET scintigrafii perfuze myokardu (§4.9.4., pasáž "Scintigrafie perfuze myokardu"). Aplikuje se ve formě
chloridu 82RbCl,
chová se jako analog draslíku (podobně
jako thalium 201Tl).
Rubidium 87Rb
je primordiální radioisotop rubidia (obsah 27,83% v
přírodním rubidiu). S velmi dlouhým poločasem 4,81.1010 roků
se b--radioaktivitou přeměňuje na
stroncium 87Sr v základním stavu. 85Rb se využívá v isotopové geochronologii
pro určování stáří minerálů a hornin - rubidium-stronciové
datování (viz výše "Radioisotopové
datování").
 Krypton
Kr36 je chemicky inertní vzácný plyn, v
zemské atmosféře se nachází v koncentraci cca 0,0001%, odkud se získává frakční destilací
zkapalněného vzduchu. Používá se k plnění žárovek a
výbojek. Má 6 stabilních isotopů 78Kr (0,36%), 80Kr (2,29%), 82Kr (11,6%), 83Kr (11,5%), 84Kr (56,99%), 86Kr (17,28%).
Z řady radioaktivních isotopů má praktické uplatnění
zvláště 81mKr v nukleární medicíně a 85Kr v průmyslových aplikacích.
Krypton
Kr36 je chemicky inertní vzácný plyn, v
zemské atmosféře se nachází v koncentraci cca 0,0001%, odkud se získává frakční destilací
zkapalněného vzduchu. Používá se k plnění žárovek a
výbojek. Má 6 stabilních isotopů 78Kr (0,36%), 80Kr (2,29%), 82Kr (11,6%), 83Kr (11,5%), 84Kr (56,99%), 86Kr (17,28%).
Z řady radioaktivních isotopů má praktické uplatnění
zvláště 81mKr v nukleární medicíně a 85Kr v průmyslových aplikacích.
Krypton
81mKr
je metastabilní jaderný izomer kryptonu-81,
který s krátkým poločasem 13,1 sekundy
deexcituje do základního stavu, z 65% emisí fotonu gama 191keV,
z 35% vnitřní konverzí za emise obalového elektronu. 81mKr se získává z generátoru
81Rb/81mKr. Princip tohoto generátoru je v
levé části obr.... Mateřské rubidium 81Rb je fixováno v pevné fázi v malé kolonce, přes
kterou se pomocí ventilátoru (vzduchového
čerpadla s regulovatelným výkonem) vede proud elučního
vzduchu. Radioaktivním rozpadem rubidia-81 průběžně
uvolňovaný dceřinný plynný krypton 81mKr je unášený procházejícím vzduchem a vedený do dýchací
masky, z níž pacient vdechuje směs vzduchu a
radioaktivního 81mKr. Do obvodu dýchací masky jsou zařazeny jednocestné
ventily, dále je předřazen směšovací ventil
vnějšího vzduchu pro zajištění volného dýchání.
Vydechovaný vzduch se vede do vymírací nádoby (objemu cca 30 litrů), z níž
vzhledem k velmi krátkému poločasu rozpadu 81mKr vychází již
prakticky neradioaktivní vzduch (na
rozdíl od níže uvedeného xenonu 133Xe, který bylo třeba odvádět potrubím mimo budovu).
Pozn.: Jak je vidět z rozpadového
schématu v pravé části obrázku, po rychlé deexcitaci 81mKr vznikající
krypton 81Kr
v základním stavi není stabilní, ale je slabě
radioaktivní (viz níže 81Kr), avšak vzhledem k dlouhému poločasu se to v dané
aplikaci nijak neprojevuje (hluboko pod úrovní přírodního
radiačního pozadí).
Při tomto vyšetření plicní
ventilace se vdechovaný vzduch se stopovým obsahem
radioaktivního 81mKr dostává do plicních alveol, přičemž
emitované záření gama 191keV je snímáno gamakamerou.
Na scintigrafickém obraze místa se sníženou aktivitou
ukazují oblasti plic se zhoršenou ventilací,
kam se krypton-81m, a tím pádem ani vzduch, nedostává (buď
vůbec, nebo sníženě) - viz §4.9.5 "Scintigrafie plic
(nukleární pneumologie)".

Generátor 81Rb/81mKr.
Vlevo: Princip činnosti generátoru a
scintigrafického vyšetření plicní ventilace. Uprostřed:
Jedno z konstrukčních uspořádání Rb-Kr generátoru. Vpravo:
Přeměnové schéma 81Rb a 81mKr; v
černém poli je scintilační spektrum záření gama 81mKr.
Krypton 81Kr
se s dlouhým poločasem 2,29.105 roků přeměňuje elektronovým záchytem na stabilní
81Br.
Přitom v 99,7% vzniká 81Br v základním stavu, v 0,3% v excitovaném stavu
276keV. V přírodě se vyskytuje ve velmi nízkých stopových
množstvích jako kosmogenní radionuklid.
Krypton
85Kr
se s poločasem 10,75 let přeměňuje beta- -radioaktivitou (Ebmax=687keV) na stabilní 85Rb, v 99,7% na základním stav, v 0,44% na excitovaný
stav 514keV. Při deexcitaci se emitují fotony gama o téže
energii 514keV (0,43%), ve stopovém množství (0,0000022%) pak
ještě při kaskádové deexcitaci gama 362,8keV a 151,2keV. V
přírodě 85Kr vzniká ve velmi nízkých stopových množstvích
jako kosmogenní radionuklid, avšak v současné době
je daleko větší množství produkováno v jaderných
reaktorech (beta přeměnami z primárního štěpného
produktu 85As).
Vzhledem k delšímu poločasu se 85Kr během provozu reaktoru v palivu hromadí. Malá
část tohoto kryptonu uniká přímo z reaktoru, většina pak
při přepracování jaderného paliva, odkud se uvolňuje do
atmosféry.

Přeměnové schéma a gama-spektrum kryptonu 85Kr
Omlouvám se za horší kvalitu gama spekter (statistické
fluktuace, vysoké pozadí). Spektrum bylo měřeno na výbojce s
velmi malým obsahem Kr-85 v plynové náplni. Slabé píky 151 a
363 keV nejsou téměř patrné v přírodním pozadí (pokud se
mi podaří opatřit silnější vzorek Kr-85, měření by se
zopakovalo)...
Krypton 85Kr se může vyrábět v jaderném reaktoru neutronovou
fúzí přírodního kryptonu-84: 84Kr(n,g)85Kr; vzniká přitom převážně metastabilní 85mKr, který s
poločasem 4,48 hod. deexcituje na základní stav 85Kr. Většinou se
však 85Kr
izoluje ze štěpných produktů jaderného paliva metodou PUREX.
Krypton 85Kr se v technické praxi používá jako přísada do plynové
náplně výbojek (cca 10kBq/m3), kde ionizace beta-elektrony usnadňuje zapálení
elektrického výboje při nižším napětí (§3.7, pasáž "Radioaktivita ve výbojkách"). Další použití je jako
stopovací plynný radionuklid pro odhalování netěsností
v hermetických nádobách a potrubích. Též v různých
dalších laboratorních aplikacích...(doplnit..?..)
 Xenon
Xenon
je do tohoto oddílu začleněn poněkud atypicky, jeho protonové číslo a
pozice v periodické tabulce prvků jej řadí až za jód (a
před cesium). Z našeho hlediska jsou pro toto atypické
zařazení dva důvody: 1. Xenon je inertní vzácný plyn
podobný kryptonu; 2. Nejdůležitější radioisotopy
kryptonu (81mKr) a xenonu (133Xe) mají své hlavní použití v
nukleární medicíně stejné: pro scintigrafické vyšetření plicní ventilace.
Xenon Xe54
je chemicky
inertní vzácný plyn, v zemské atmosféře se nachází v
koncentraci cca 5.10-6 %, odkud se získává frakční destilací
zkapalněného vzduchu. Používá se k plnění žárovek a
hlavně výbojek. Má 8 stabilních isotopů: 124Xe (0,1%), 136Xe (0,09%), 128Xe (1,9%), 129Xe (26,4%), 130Xe (4,07%), 131Xe (21,23%), 132Xe (26,91%), 134Xe (10,44%), 136Xe (8,86%).
Pozn.: Za
zajímavost stojí zmíněný stabilní isotop 129Xe,
který je dceřinným produktem radioisotopu 129I a jehož
zvýšený obsah v některých meteoritech se používá v tzv. jód-xenonové
chronometrii pro určování doby jejich vzniku - viz výše
část "Radioisotopové (radiometrické) datování", pasáž "Datování
pomocí rozpadlých radionuklidů".
Z radioaktivních isotopů xenonu se občas používá 133Xe:
Xenon
133Xe
se s poločasem 5,25 dne přeměňuje b--radioaktivitou
na 133Cs,
v 99,1% na excitovanou hladinu 81keV, 0,87% probíhá na vyšší
hladinu 160,6keV a jen 0,0092% na ještě vyšší hladinu
383,8keV. Při deexcitaci jsou vyzařovány především fotony
gama o energii 81keV (37%), dále 79,6keV
(0,29%), s velmi nízkou intenzitou pak vyšší energie 160,6keV
(0,068%), 302,9keV (0,0058%) a 383,8keV (0,0028%).
Isotop 133Xe
se nejčastěji získává štěpením uranu (obohaceného
isotopem 235U) neutrony v jaderném reaktoru. Další možností je
neutronové ozařování přírodního xenonu v jaderném
reaktoru za použití reakce 132Xe(n,g)133Xe (vzniká zde rovněž
metastabilní 133mXe, který s poločasem 2,2 dne emisí fotonu gama
233keV izomerně deexcituje na základní stav 133Xe), nebo neutronové ozařování cesia pomocí reakce 133Cs(n,p)133Xe.
Plynný xenon 133Xe se používá *) v nukleární medicíně pro diagnostiku
ventilační funkce plic - je podrobněji popsáno v
§3.11b "Dynamická scintigrafie plic (ventilace
133-Xenon)" knihy "Komplexní vyhodnocování
scintigrafie".
*) 133Xe se často používal především v 80.letech. Jeho
nevýhodou byla obtížná dostupnost, složitá manipulace s
plynným xenonem a potřeba speciální spirometrické
dýchací aparatury. Za tuto cenu však umožňoval
velmi komplexní vyšetření dýchací funkce.
Nyní je ventilační scintigrafie plic prováděna většinou
generátorovým kryptonem 81mKr popsaným výše.
Metastabilní xenon 131mXe
je popsán níže v části "Radiojód 131I", pasáž "Metastabilní xenon 131mXe".
 S t r o n c i u m , Y t r
i u m
S t r o n c i u m , Y t r
i u m 
 Stroncium
Sr38 je poměrně měkký šedobílý lesklý kov z
alkalické skupiny. Je značně reaktivní, v přírodě se
vyskytuje pouze ve sloučeninách, v zemské kůře v množství
0,03-0,04%. Stroncium se v přírodě vyskytuje v podobě 4
stabilních isotopů: 84Sr (0,56%), 86Sr (9,86%), 87Sr (7%), 88Sr (82,58%).
Stroncium
Sr38 je poměrně měkký šedobílý lesklý kov z
alkalické skupiny. Je značně reaktivní, v přírodě se
vyskytuje pouze ve sloučeninách, v zemské kůře v množství
0,03-0,04%. Stroncium se v přírodě vyskytuje v podobě 4
stabilních isotopů: 84Sr (0,56%), 86Sr (9,86%), 87Sr (7%), 88Sr (82,58%).
Pozn.: Isotop 87Sr v přírodě
vzniká beta-radioaktivitou isotopu rubidia 87Rb - je radiogenní; pomocí poměrů isotopů 87Sr, 86Sr a 87Rb se provádí
dlouhodobé radiometrické datování (viz
výše "Radioisotopové
(radiometrické) datování").
Z radioaktivních isotopů stroncia jsou
důležité především dva:
Stroncium
89Sr,
se s poločasem 50,5 dní přeměňuje b--radioaktivitou
z 99,99% na základní stav ytria 89Y (Ebmax=1488keV) a z 0,01% na
excitovaný stav 909keV (při deexcitaci je
emitováno velmi slabé záření gama této energie). Je tedy prakticky čistým zářičem beta.

Přeměnové schéma a gama-spektrum
stroncia 89Sr.
Pozn.: Gama pík 514 keV uprostřed spektra nepatří
89Sr, ale pochází z drobné (cca 0,01%)
radionuklidové nečistoty 85Sr v měřeném vzorku.
V gama-spektru 89Sr vidíme především brzdné záření
se spojitým spektrem, vznikající při interakci rychlých
elektronů beta s atomy v materiálu vzorku; s klesající
tendencí se táhne až k energii cca 1000keV. Při delší
spektrometrické akvizici je zde při zvětšení vidět i slabý
fotopík gama-záření o energii 909keV.
Při měření našeho konkrétního vzorku
("Metastron", dodaného
laskavostí kolegů prim.MUDr.A.Chodackého a vrchní sestry
H.Mixové z ONM Chomutov) se zobrazil i
pík 514 keV, pocházející z radionuklidové nečistoty 85Sr (její vznik je zmíněný v poznámce níže).
Isotop 89Sr se připravuje buď ozařováním stroncia (obohaceného isotopem 88Sr) pomalými neutrony reakcí 88Sr(n,g)89Sr v jaderném
reaktoru, nebo ozařováním ytria rychlými neutrony v reakci 89Y(n,p)89Sr. Lze jej
radiochemicky separovat i ze štěpných produktů uranu.
Pozn.: Typickými
radionuklidovými nečistotami v preparátech 89Sr jsou zde 85Sr
(vznikající reakcí n,g s isotopem 84Sr obsaženým v terčíku) a 90Sr, vznikající z isotopu 88Sr, nebo hojně
obsažený ve štěpných produktech.
Radioisotop 89Sr ve formě chloridu
("Metastron") se používá v nukleární
medicíně pro paliativní terapii kostních metastáz
ca prostaty a prsu (§3.6, část "Radioisotopová
terapie").
Stroncium 90Sr
se s poločasem 27,78 roků přeměňuje b--radioaktivitou
na radioaktivní ytrium 90Y (Ebmax=546keV) v základním stavu.
Isotop 90Sr
vzniká při jaderném štěpení uranu-235 a plutonia-239 (s
výtěžkem 5,7%) a izoluje se ze štěpných produktů z
vyhořelého jaderného paliva. Používá se v
termoelektrických radioisotopvých bateriích (spolu s plutoniem-238).
Důležité použití stroncia-90 je v 90Sr/90Y generátorech pro přípravu ytria
90Y v nukleární medicíně (viz níže Y-90).
Stroncium
82Sr -
Sr/Rb generátor
se s poločasem 25,4 dní přeměňuje elektronovým
záchytem na radioaktivní rubidium 82Rb
v základním stavu.
Isotop stroncium-82 slouží jako mateřský isotop v generátoru
82Sr/82Rb pro získávání krátkodobého
pozitronového radionuklidu rubidia 82Rb pro použití v pozitronové emisní
tomografii PET (výše uvedená pasáž
"82Rb").
 Ytrium Y39 je
stříbřitě šedý kov podobný skupině lantanoidů. V
pozemské přírodě se vyskytuje pouze ve sloučeninách, v
zemské kůře v množství cca 2-4mg/kg. Ytrium se používá k
výrobě luminoforů. Má jediný stabilní isotop 89Y. Důležitým
radioaktivním isotopem ytria je:
Ytrium Y39 je
stříbřitě šedý kov podobný skupině lantanoidů. V
pozemské přírodě se vyskytuje pouze ve sloučeninách, v
zemské kůře v množství cca 2-4mg/kg. Ytrium se používá k
výrobě luminoforů. Má jediný stabilní isotop 89Y. Důležitým
radioaktivním isotopem ytria je:
Ytrium
90Y,
které se s poločasem 64,1 hodin přeměňuje b--radioaktivitou
z 99,9885% na základní stav 90Zr (Ebmax=2300keV) - je tedy prakticky čistým
b-zářičem.
Jen v nepatrném zastoupení
0,017% dochází k přeměnám na dva excitované stavy 90Zr 1760 (0,017%) a 2190 keV (mizivé
zastoupení 0,0000014%). Hladina 2190keV přechází
gama-deexcitací na základní stav (emise
gama na hranicích měřitelnosti). Hladina
1760keV se na základní stav nemůže deexcitovat přímo,
neboť se jedná o monopólový E0 přechod 0+®0+
(je diskutováno v §1.2, část "Záření gama",
pasáž "Jaderná metastabilita a
izomerie"); může docházet k 2-g emisi, vnitřní konverzi,
nebo emisi e--e+ páru - 90Y je tedy i slabým pozitronovým zářičem.
Ve spektru záření gama 90Y dominuje především spojitá křivka
intenzívního brzdného záření,
vznikajícího při interakci vysokoenergetických elektronů
beta s materiálem vzorku (s klesající
tendencí se táhne až k energii téměř 2MeV). Při podrobnějším měření s delším expozičním
časem se dále ve spektru objevuje pík slabého
anihilačního záření 511keV(0,006%) od emitovaných
pozitronů. Velmi slabě zastoupeny jsou vyšší píky 1761keV
*) a 2186keV.
*) Pík 1761keV vzniká především
současnou detekcí obou emitovaných gama kvant při 2-g deexcitaci hladiny
1761keV (přímá gama deexcitace je zakázána - E0); proto je
slabý.

Přeměnové schéma a gama-spektrum ytria 90Y.
Při měření spektra velmi slabého záření gama byl vzorek
ytria obklopen vrstvou 2,5cm plastu pro odstínění tvrdých
elektronů beta.
Isotop Y-90 se získává především z generátoru
90Sr/90Y zmíněného výše. Alternativními
způsoby výroby je ozařování ytria neutrony v jaderném
reaktoru 89Y(n,g)90Y (má však nízký účinný průřez), nebo pomocí cyklotronu ozařováním ytria deuterony 89Y(d,p)90mY(I.T.,T1/2=3,2h.)®90Y, či rubidia alfa-částicemi 87Rb(a,n)90mY(I.T)®90Y.
Hlavní využití isotopu 90Y, jakožto čistého b-zářiče, je v terapeutické
nukleární medicíně (§3.6,
část "Radioisotopová
terapie"), kde se využívají vysoce energetické beta-částice
v radioimunoterapii, paliativní terapii metastáz
či radiační synovektomii u větších kloubů.
Relativně delší dosah těchto beta elektronů v tkáni
umožňuje (díky efektu "křížové palby")
rovnoměrné prozáření větších nádorů, vykazujících
často heterogenní prokrvení a hypoxii.
Slabé pozitronové a
anihilační záření nemá přímý radiační význam, je
naprosto přezářené intenzívním brzdným zářením. V
principu však lze využít i tak slabé anihilační záření
511keV pro zobrazení biodistribuce
teraputických radiofarmak značených 90Y pomocí pozitronové emisní tomografie PET
*) s lepším rozlišením, než jednofotonová scintigrafie
(planární, SPECT) s použitím brzdného záření. Další
možností zobrazení biodistribuce ytria je PET scintigrafie s
použitím níže uvedeného pozitronového ytria 86Y.
*) Koincidenčním režimem detekce je
brzdné záření silně potlačeno, takže i slabé anihilační
záření může být úspěšně detekováno. Princip PET je
popsán v §4.3, část "Kamery PET".
Ytrium
86Y
se s poločasem 14,7 hodin přeměňuje b+-radioaktivitou
(26%) a elektronovým záchytem (74%) na
stroncium 86Sr ve více než 20 vysoce excitovaných hladinách. V
gama spektru ytria-86 kromě e-e+
anihiličního píku 511keV (35%) je obsaženo
velké množství gama-píků z deexcitací hladin 86Sr - výraznější zastoupení mají 443 (16%), 515+580
(5%), 628 (33%), 703 (15%), 777 (22%), 836 (5%), 1026 (10%), 1077
(83%), 1115 (31%), 1854 (17%), 1921 (21%) keV; při velkém
zvětšení je vidět řada dalších slabých píků
převážně vysokých energií, až do 3800keV.
.................obrázek...........
....................přeměnové schéma , spektrum ........
Isotop 86Y se připravuje protonovým ostřelováním
stronciového terčíku (vysoce obohaceného isotopem 86Sr) v cyklotronu
reakcí 86Sr(p,n)86Y.
Ytriem-86 se zatím experimentálně značí diagnostická
radiofarmaka pro použití v pozitronové emisní
tomografii PET jako radioindikátory
pro farmakokinetiku a akumulaci terapeutických
radiofarmak značených 90Y v organismu (isotop Y-90 je
čistý beta, jeho biodistribuci lze obtížně scintigraficky
zobrazit - přes brzdné záření). Je to
speciální příklad teranostiky (srov. §4.9, pasáž "Kombinace
diagnostiky a terapie - teranostika"), kdy v tomto případě
jeden isotop (86Y) téhož prvku slouží jako diagnostický indikátor
biodistribuce jiného isotopu (90Y) použitého v terapeutickém radiofarmaku - např. v 90Y-konjugátu
monoklonálních protilátek.
 Zirkonium
Zr40 je stříbřitě šedý kov ze skupiny přechodných
kovů, chemicky velmi odolný. V pozemské přírodě se
vyskytuje pouze ve sloučeninách, v zemské kůře v množství
cca 160-200mg/kg. Křemičitan zirkon ZrSiO4 je tvrdostí a krystalickou
strukturou podobný diamantu. Zirkonium se používá
především v jaderných reaktorech (zapouzdření
palivových článků), vzhledem ke své
chermické i mechanické odolnosti a nízkému účinnému
průřezu pro záchyt neutronů (§1.3,
část "Jaderné reaktory"). Slitiny zirkonia s niobem
vykazují supravodivé vlastnosti a používají se v některých
supravodivých elektromagnetech.
Zirkonium
Zr40 je stříbřitě šedý kov ze skupiny přechodných
kovů, chemicky velmi odolný. V pozemské přírodě se
vyskytuje pouze ve sloučeninách, v zemské kůře v množství
cca 160-200mg/kg. Křemičitan zirkon ZrSiO4 je tvrdostí a krystalickou
strukturou podobný diamantu. Zirkonium se používá
především v jaderných reaktorech (zapouzdření
palivových článků), vzhledem ke své
chermické i mechanické odolnosti a nízkému účinnému
průřezu pro záchyt neutronů (§1.3,
část "Jaderné reaktory"). Slitiny zirkonia s niobem
vykazují supravodivé vlastnosti a používají se v některých
supravodivých elektromagnetech.
Zirkonium má 4 stabilní isotopy 90Zr (51,5%), 91Zr (11,2%), 92Zr (17,1%) a 94Zr (17,4%). Přírodní zirkonium obsahuje též 2,8%
radioaktivního isotopu primárního původu 96Zr, který se
přeměňuje dvojitým beta rozpadem s obrovsky dlouhým
poločasem 3,9.1019roků. Z radioaktivních isotopů zirkonia našel
platnění jeden :
Zirkonium
89Zr,
které se s poločasem 78,4 hodin přeměňuje elektronovým
záchytem (76,2%) a pozitronovou radioaktivitou (22,8%) na
stabilní 89Y v excitovaném stavu, především o energii 909 keV (ve zlomcích procenta probíhá elektronový záchyt i
na vyšší hladiny 1744, 2530, 2567 a 2622 keV). V gama spektru zirkonia-89 je výrazný e-e+ anihiliční
pík 511keV (46%) (jako u
každého pozitronového radionuklidu) a
ještě silnější je gama pík 909keV (99%); v oblasti vyšších energií jsou až při velkém
zvětšení vidět slabé píky 1621, 1658, 1713 a 1745 keV.

Přeměnové schéma a gama spektrum zirkonia 89Zr.
Pozitronový radionuklid Zr-89 se používá v pozitronové
emisní tomografii ("§4.3
"Pozitronová emisní tomografie
PET", §4.8 "Radionuklidy a radiofarmaka pro
scintigrafii", pasáž "Radionuklidy a radiofarmaka pro PET"). Díky poněkud delšímu
poločasu je 89Zr vhodný pro PET zobrazování pomalejších
biologických a fyziologických procesů sloučenin s vysokou
molekulovou hmotností. Je to zvláště radioimunodiagnostika s
biokonjugáty těžších monoklonálních protolátek
(struktura a vlastnosti monoklonálních
protilátek jsou podrobněji rozebírány v §3.6, část "Cílená biologická léčba - monoklonální protilátky"), které mají pomalejší
farmakokinetiku, takže při označení krátkodobým fluorem-18
nebo galiem-68 by se radionuklidy nestačily v nádorových
ložiscích vychytat.
Zkouší se značený 89Zr-cetuximab,
který blokuje aktivaci epidermálního růstového faktoru EGFR,
který hraje důležitou roli v proliferaci, diferenciaci a
přežívání nádorových buněk. 89Zr-cetuximab může sloužit pro PET diagnostické
zobrazení vychytávání cetuximabu v nádorových a
normálních tkáních před biologickou imunoterapií. Může
též teranosticky sloužit pro zjišťování
biodistribuce 90Y- či 177Lu-cetuximabu v radioimunoterapii.
Dále se zkouší značený 89Zr-trastuzumab, proti epidermálního
růstového faktoru HER2, podílejícím se na
proliferaci, angiogenezi a metastázování nádorových buněk. 89Zr-bevacizumab,
anti VGEF protilátka, může zobrazovat
nádorovou angiogenezi způsobovanou vaskulárním
endoteliálním růstovým faktorem VGEF. Značená
89Zr-J591
anti-PSMA monoklonální protilátka může být
použita k zobrazení PSMA pozitivních nádorů prostaty.
Pozn.: Určitým
problémem zde může být silný gama-pík 909keV, jehož
spodní okraj a Compton. rozptýlené záření zasahuje do
poměrně širokého pracovního okna analyzátoru měřeného
anihilačního záření 511keV (může tím docházet ke
zhoršování kontrastu obrazu vlivem nepravých
koincidencí)..?..
 Molybden , Technecium
Molybden , Technecium 
 Molybden
Mo42 je kovový prvek v pozemské
přírodě poměrně vzácný (cca 1-7mg/kg
v zemské kůře).
Má řadu aplikací především v metalurgii. Vyskytuje se v
řadě stabilních isotopů: 92Mo (11,8%), 924Mo (9,3%), 95Mo (16%), 97Mo (9,5%), 98Mo (24,1%), 100Mo (9,6%) *).
Molybden
Mo42 je kovový prvek v pozemské
přírodě poměrně vzácný (cca 1-7mg/kg
v zemské kůře).
Má řadu aplikací především v metalurgii. Vyskytuje se v
řadě stabilních isotopů: 92Mo (11,8%), 924Mo (9,3%), 95Mo (16%), 97Mo (9,5%), 98Mo (24,1%), 100Mo (9,6%) *).
*) Pomocí koincidenčních měření s
polovodičovými Ge detektory se ukázalo, že isotop 100Mo není zcela
stabilní, ale s obrovsky dlouhým poločasem cca 8.1018let se dvojitým
beta-rozpadem přeměňuje na ruthenium 100Ru.
Z radioaktivních isotopů molybdenu je
nejdůležitější 99Mo :
Molybden 99Mo
se s poločasem rozpadu 66 hodin přeměňuje b--radioaktivitou
na excitované hladiny dceřinného nuklidu technecium 99Tc
(levá část rozpadového schématu). V 82% přeměna probíhá na metastabilní
excitovanou hladinu 142keV 99mTc o poločasu 6 hod., v 17% na
vyšší hladinu 921keV, která při deexcitaci (přes hladinu
181keV) emituje záření g 740keV.
Molybden-99 se připravuje v jaderném reaktoru
dvěma způsoby. První metoda spočívá v neutronovém
ozařování molybdenu (obohaceného
isotopem 98Mo) v reakci 98Mo(n,g)99Mo. Častěji se však 99Mo vyrábí štěpením uranu (obohaceného isotopem 235U) pomalými neutrony, kde jedním
ze štěpných produktů je 99Zr, z něhož požadovaný molybden-99 vzniká dvěma
následnými b--přeměnami:
99Zr(b-, T1/2=2,1s.)®99Nb(b-, T1/2=15s.)®99Mo.
Molybden
99Mo
slouží jako mateřský radionuklid pro získávání technecia 99mTc v Mo-Tc
generátoru (viz níže).
 Technecium
Technecium
Chemický prvek technecium Tc43 se
v přírodě prakticky nevyskytuje *), neboť nemá
žádný stabilní isotop (přičemž
poločasy rozpadu nejstabilnějších radioisotopů technecia 97,98,99Tc - 2,6.106let, 4,2.106let, 2,1.105let - nejsou
dostatečně dlouhé na to, aby se do dnešní doby zachovalo
primordiální technecium z výbuchu supernovy, tak jak je tomu u
thoria, uranu či draslíku-40). Naprosto
stopové množství technecia vzniká při spontánním
štěpení uranu-235. V posledních několika desítiletích
však poměrně značné množství technecia vzniká při
provozu jaderných reaktorů (§1.3 "Štěpení
atomových jader",
pasáž "Štěpné produkty").
*) V Mendělejevově periodické tabulce
zůstávalo místo pro atomové číslo 43 dlouho prázdné.
První isotop tohoto prvku byl objeven v r.1937 při ozařování
molybdenu urychlenými deuterony v cyklotronu 99Mo(d,n)97Tc.
Z toho vznikl název "technecium" jako prvek, jehož isotopy lze připravit jen umělou -
technickou - cestou.
Technecium
99mTc
Pro nukleární medicínu je vůbec
nejdůležitějším radionuklidem metastabilní technecium
99mTc (T1/2=6hodin), které je čistým zářičem gama
o energii Eg=140keV (88,5%). Se zanedbatelně
slabou intenzitou jsou emitovány g fotony 2,2keV, 90keV,
142keV, 233keV a 322keV (viz níže). Poměrně hojně jsou však
zastoupeny konverzní a Augerovy elektrony,
produkované z atomového obalu při vnitřní konverzi
deexcitačních přechodů (mechanismus je
popsán v §1.2, pasáž "Vnitřní konverze záření gama a
X").
Jsou to především nízkoenergetické elektrony 1,6-2,9keV
(210%), 14-21keV (2,2%) a též elektrony středních energií
120-140keV (21%). Při vnitřní konverzi vzniká též přeskoky
mezi elektronovými hladinami v obalu měkké charakteristické
X-záření 18-21keV (8%).
99mTc se získává téměř výhradně shora uvedeným
beta-rozpadem molybdenu 99Mo (T1/2=66hod.) v tzv. Mo-Tc generátoru.
Lze jej však vyrobit i přímo ("instantní" technecium)
protonovým ostřelováním přírodního molybdenu (obohaceného isotopem 100Mo) v cyklotronu pomocí reakce 100Mo(p,2n)99mTc - používá se
jen ojediněle.
Mo-Tc generátory jsou
většinou elučního typu. Molybdem 99Mo je v
"chromatografické" kolonce nasorbován na nosiči
(většinou Al2O3)
v nerozpustné formě oxidu. Po radioaktivní
přeměně jádra 99Mo na dceřinné jádro 99mTc se vzniklý atom technecia vyváže z nerozpustné
vazby; spojí se se 4 atomy kyslíku za vzniku aniontu 99mTcO4- pertechnetátu. Tento dceřinný
produkt je rozpustný ve vodě, čímž může
být promýváním vodou - elucí - odseparován
od výchozího molybdenu (na obr. vlevo). Jelikož se eluce
provádí fyziologickým roztokem obsahujícím sůl
NaCl, anionty pertechnetátu se okamžitě vážou iontovou
vazbou se sodíkem za vzniku technecistanu sodného
Na99mTcO4-. V této chemické formě získáváme technecium z
elučního generátoru.

Eluční 99Mo/99mTc generátor.
Vlevo: Principiální funkční schéma
elučního generátoru. Uprostřed: Technické
provedení sterilního generátoru s evakuovanou eluční
lahvičkou.
Vpravo: Přeměnové schéma molybdenu 99Mo na technecium 99mTc, deexcitace na 99Tc a pomalé
přeměny na stabilní ruthenium 99Ru.
Nové typy sterilních elučních
generátorů používají evakuovanou eluční lahvičku,
do níž se po "napíchnutí" vlivem atmosférického
podtlaku automaticky nasaje fyziologický roztok hadičkou
vedoucí ze zásobní lahvičky přes sorbční kolonku
generátoru s 99Mo (na obr. uprostřed). Během několika desítek
sekund se lahvička naplní eluátem 99mTc.
Podrobné
rozpadové schéma 99mTc
je níže v pravé části obrázku. Výchozí metastabilní
hladina 142keV (vzniklá po beta-přeměně 99Mo) izomerně
přechází nejdříve na hladinu 140,5 keV, odkud se vyzařuje
základní záření gama o energii 140,5keV.
S velmi malým zastoupením 0,02% dochází k přímé deexcitaci
na základní stav, při němž je emitována energie 142,7keV.
Fotony velmi měkkého záření gama 2,17keV prakticky
nepozorujeme, neboť téměř ve 100% podléhají vnitřní
konverzi. Jádro technecia 99Tc v základním
stavu (po izomerním přechodu z 99mTc) je beta-radioaktivní a s velmi dlouhým poločasem 200
000 let se pomalu přeměňuje na stabilní ruthenium 99Ru.
Ve zcela nepatrném procentu dochází k přímé
beta-přeměně 99mTc
z metastabilní hladiny *) na 99Ru (základní stav jádra 99Tc je
"bypassován") - především na
excitované hladiny 322 a 90 keV 99Ru. Jejich
deexcitací vzniká g-záření o energiích 322, 232 a 90 keV, ovšem zcela
nepatrného zastoupení. Při radioaktivitě 99mTc je
dále emitováno měkké charakteristické X-záření
o energiích » 2-3keV (L-série) a »18-22keV (K-série), jakož i větší počet
nízkoenergetických konverzních a Augerových
elektronů (až 4 elektrony/1přeměnu), většinou o
energiích »1,6-3 keV, menší množství »120-140 keV (bylo uvedeno
výše).
*) Při tomto procesu se neuplatňuje
běžně uváděná energie 142keV této metastabilní hladiny
vzhledem k základnímu stavu 99Tc, ale energie 436keV
měřená vzhledem k základnímu stavu dceřinného 99Ru.
Je to speciální případ větvené přeměny,
shora diskutované v části "Přeměnová schémata".

Podrobné přeměnové schéma technecia 99mTc -
důležitého radionuklidu v nukleární medicíně.
Vlevo: Vznik metastabilního 99mTc
beta-radioaktivitou molybdenu 99Mo. Vpravo: Metastabilní hladina 142 keV,
vedle dominantní deexcitace na základní stav technecia 99Tc,
se může s nepatrnou pravděpodobností beta--radioaktivitou
přeměňovat přímo na excitované hladiny ruthenia-99.
Ve standardním scintilačním gama-spektru 99mTc
(na scintilačním spektrometru nebo gamakameře) pozorujeme
pouze jeden výrazný fotopík energie 140keV -
na obr. vlevo (na polovodičovém
spektrometru můžeme při pečlivém dlouhodobém měření
rozlišit i slabou linii 142,7keV). Slabé
píky z excitovaných hladin 99Ru, vznikajících z 99mTc
"bypassováním" 99Tc, především 322keV,
můžeme spektrometricky vidět až po odfiltrování silné
přezařující linie 140keV vrstvou cca 4-5mm olova; na tomto
filtrovaném spektru je dále patrná i linie 740keV kontaminantu
99Mo -
pravá část obrázku.
Pozn.:
Linii 90keV, která je silnější než 322keV,
v tomto filtrovaném spektru nevidíme, neboť je zcela pohlcena
olověnou vrstvou.

Gama-spektrometrické měření eluátu 99mTc (nahoře - scintilační spektrum, dole
- polovodičové spektrum).
Vlevo: Základní spektrum záření gama 99mTc. Vpravo:
Filtrované spektrum záření gama měřené přes stínící
vrstvu 5mm olověného kontejnerku, v němž je možno pozorovat
velmi slabou g-linii 322keV 99mTc a gama-linie 740 a 778 keV kontaminantu 99Mo.
Techneciem značená radiofarmaka (§4.8 "Radionuklidy a
radiofarmaka pro scintigrafii") nacházejí široké uplatnění při
statické i dynamické scintigrafii ledvin,
jater, plic, srdce, mozku a dalších orgánů, jakož i v
nádorové diagnostice (§4.9 "Klinická
scintigrafická diagnostika v nukleární medicíně").
 I n d i u m , C í n
I n d i u m , C í n 
 Indium In49 je
měkký snadno tavitelný kov (157°C) světlé barvy, v přírodě poměrně vzácně
zastoupený (cca 0,1mg/kg v zemské kůře). Využívá se pro přípravu nízkotavitelných
slitin, pokovování zrcadel, v elektronice při výrobě
zvláště optoelektronických součástek. Má dva stabilní
isotopy 113In
(4,3%) a 115In (95,7%).
Indium In49 je
měkký snadno tavitelný kov (157°C) světlé barvy, v přírodě poměrně vzácně
zastoupený (cca 0,1mg/kg v zemské kůře). Využívá se pro přípravu nízkotavitelných
slitin, pokovování zrcadel, v elektronice při výrobě
zvláště optoelektronických součástek. Má dva stabilní
isotopy 113In
(4,3%) a 115In (95,7%).
 Cín Sn50 je
rovněž měkký snadno tavitelný kov (232oC) světlé barvy, poněkud více zastoupený (cca 2-4 mg/kg v zemské kůře).
Má řadu stabilních isotopů: ........
Cín Sn50 je
rovněž měkký snadno tavitelný kov (232oC) světlé barvy, poněkud více zastoupený (cca 2-4 mg/kg v zemské kůře).
Má řadu stabilních isotopů: ........
Z radioaktivních isotopů india a cínu mají určitou
důležitost tři radionuklidy:
Indium
111In
Přeměňuje se s poločasem 67,4 hodin elektronovým
záchytem na kadmium 111Cd v excitovaném stavu 416keV, při jehož kaskádové
deexcitaci je emitováno záření gama o energiích 171 a 245keV
(rozpadové schéma v levé části
obr....). Gama spektrum 111In sestává ze dvou
výrazných fotopíků zmíněných energií (spektrum v pravé části obrázku), při měření s vysokou detekční účinností je ve
spektru patrný i slabší sumační pík kolem energie
416keV. Vyrábí se ozařováním kadmia (obohaceného
isotopem 111Cd) urychlenými protony v
cyklotronu reakcí 111Cd(p,n)111In.
V
nukleární medicíně se 111In poměrně často používá pro scintigrafii nádorů
a zánětlivých ložisek, pro imunoscintigrafii a scintigrafii
likvorových cest (§4.9 "Klinická
scintigrafická diagnostika v nukleární medicíně", "Scintigrafie likvorových cest"...).
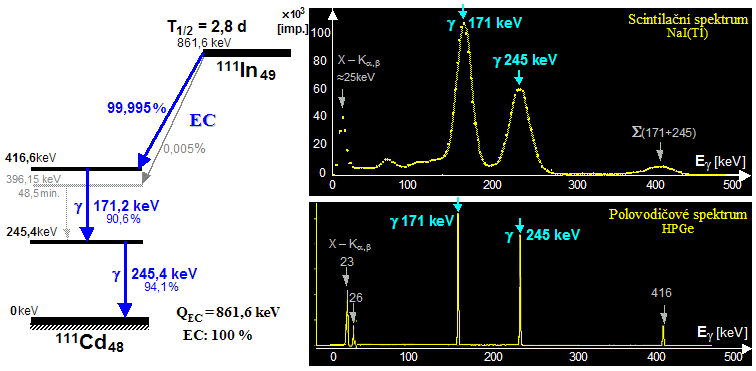
Přeměnové schéma a gama-spektrum india 111In.
Cín 113Sn
S poločasem 115 dní se přeměňuje elektronovým záchytem na
dva excitované stavy india 113In: v 98,2% vzniká excitovaný stav india 113mIn,
v 1,8% hladina 647keV, která emisí fotonu gama 255keV
přechází rovněž na hladinu 113mIn. Radionuklid 113Sn se vyrábí ozařováním cínu (obohaceného
isotopem 112Sn) neutrony v jaderném reaktoru pomocí reakce 112Sn(n,g)113Sn. Tento
radionuklid slouží jako mateřský isotop pro získávání
india 113mIn
v generátoru 113Sn/113mIn:
Indium 113mIn
Metastabilní 113mIn s poločasem 1,66hod. deexcituje na základní stav
emisí fotonů gama o energii 392keV. Získává se z výše
uvedeného generátoru 113Sn/113mIn. V nukleární medicíně se používal v
60.-80.letech pro podobné scintigrafické metody jako nyní 111In, jakož i pro
vyšetření skeletu, mozku či ledvin. Později byl postupně
vytlačen radiofarmaky značenými 111In a 99mTc, jejichž delší poločas a nižší energie gama
záření jsou vhodnější pro scintigrafii.
 J ó d
J ó d 
Prvek jód I53
ze skupiny
halogenů je vysoce reaktivní a v přírodě se vyskytuje pouze
ve sloučeninách; je poměrně vzácně
zastoupený (cca 0,1-5 mg/kg v zemské
kůře, v mořské vodě cca 0,6mg/l). V pevném skupenství tvoří
tmavě fialové lístkové krystalky, které za atmosférického
tlaku sublimují přímo do plynné fáze. Jód
patří mezi biogenní prvky, využívá ho
především štítná žláza pro tvorbu
hormonů, především thyroxinu.
Ortografická poznámka :
Ve starší československé literatuře bylo někdy zvykem
obvyklou chemickou značku jódu "I" (Iodine)
foneticky přepisovat jako "J" (Jód). Takže
místo např. 131I či 125I se někdy psalo 131J nebo 125J. Tato zvyklost se u nás udržela zhruba do 60-70 let.
Jód má řadu isotopů v rozmezí 108I - 144I, z nichž
stabilní je pouze jeden 127I. Jód je prvek s největším počtem
v praxi využívaných radioisotopů, především pro aplikace v
nukleární medicíně; zmíníme si je zde v
pořadí podle důležitosti :
Radiojód
131I
Nejdůležitějším radioisotopem jódu je radiojód 131I
(T1/2=8 dnů, b- s max. energií 606keV, hlavní energie g 364keV).
Radionuklid 131I se (podle
rozpadového schématu na obr. vlevo) b--radioaktivitou
přeměňuje na excitované stavy dceřinného nuklidu xenonu 131Xe, který je již
stabilní (neradioaktivní). Dominantní "kanál" beta-přeměny je na
excitovanou hladinu 364,5 keV (89%), která v
81% deexcituje na základní stav 131Xe a v 6% deexcituje na hladinu 80keV (která vzápětí
deexcituje na základní stav). Ve 2% nastává přeměna na
excitovanou hladinu 722keV, v 7% na hladinu 637keV, ve zlomcích
procenta na některé další excitované hladiny (včetně zajímavé metastabilní
hladiny 164keV dceřinného izomeru 131mXe - viz níže "Metastabilní 131mXe").

Přeměnové schéma a gama-spektrum radiojódu 131I .
Pozn.: Toto spektrum bylo měřeno s
"čerstvým" vzorkem jódu, v němž se ještě
nestačil nahromadit metastabilní xenon 131mXe.
Ve scintilačním a
polovodičovém spektru záření gama 131I dominuje hlavní fotopík zachycující energii
záření g 364keV. Směrem k vyšším energiím
jsou patrné dva slabší píky 637 a 723 keV. V oblasti
nižších energií pak vidíme rovněž slabší píky 284 a 80
keV, úplně na začátku spektra pak charakteristické
X-záření Ka,b xenonu 30keV (nízkoenergetické
linie La,b 4-5keV na běžném gama detektoru nevidíme).
Metastabilní
131mXe
Při beta-radioaktivitě radiojódu 131I je jednou z excitovaných hladin dceřinného 131Xe i metastabilní
131mXe hladina o energii 164keV,
která se s poločasem T1/2=12 dní deeexcituje na základní stav jádra 131Xe; tento vzbuzený
metastabilní stav můžeme tedy považovat za samostatný radionuklid
131mXe. Na tuto metastabilní hladinu
probíhá jen 0,38% rozpadů 131I a navíc její deexcitace silně podléhá vnitřní
konverzi (z 98%),
takže jen cca 0,021% je emitováno jako záření gama 164keV
(viz níže). V hermeticky uzavřeném preparátu 131I je po cca 14 dnech
od výroby isotopu 131I dosažena radioaktivní rovnováha mezi
dynamikou přeměny 131I a 131mXe (z otevřeného vzorku však
plynný dceřinný xenon průběžně uniká). Lze říci, že každý preparát radiojódu-131 je směsí
dvou radioisotopů: mateřského beta-gama-radionuklidu 131I s poločasem 8dní
a dceřinného metastabilního gama-radionuklidu 131mXe s poločasem
12dní.
Slabý fotopík 164keV z metastabilního 131mXe není ve
scintilačním spektru vzorku 131I viditelný, protože leží v oblasti Comptonova
rozptylu hlavní energie 364keV (interferuje
s píkem zpětného rozptylu). Ani na
polovodičovém spektru není na první pohled patrný, je vidět
až po silném zvětšení úseku spektra mezi 100-200 keV. Pro
přesnější spektrometrické změření metastabilního 131mXe jsme vymysleli
drobnou "fintu", spočívající v následujícím
jednoduchém experimentu (snadno
proveditelném na pracovišti nukleární medicíny) :
Použili jsme kapalný vzorek 131I
ve formě jodidu NaI o aktivitě cca 100MBq (radiojód
běžně používaný k terapii štítné žlázy), hermeticky uzavřený v penicilince
po dobu asi 14 dní. Do injekční stříkačky s jehlou jsme pak
odsáli vzduch nad hladinou vzorku s obsahem
dceřinného plynného xenonu; tuto stříkačku jsme okamžitě
uzavřeli. V takto získané plynné náplni ve stříkačce
bude, kromě vzduchu, i dceřinný xenon-131 s obsahem
metastabilního 131mXe, jehož gama-záření můžeme
měřit ve spektrometru - zbavili jsme se tím rušivého
mateřského isotopu 131I *), od něhož jsme odseparovali dceřinný
131mXe.
Výsledný vzorek (o aktivitě zhruba 3kBq) pro spektrometrické měření jsme potom připravili
tak, že z odsáté plynné náplně ve stříkačce jsme cca 1/2
mililitru přepustili do malé měřící kyvety.
*) Pokud by v plynné náplni byl obsažen
vypařený plynný jód, můžeme se ho zbavit protřepáním
roztokem neaktivního jodidu draselného nebo hydroxidu sodného.
Při našem měření toto však nebylo potřeba, odsátý vzorek
byl naprosto čistý, bez sebemenší stopy
jódu 131.
Toto
měření zároveň ukazuje, že z roztoku jodidu sodného se jód
neodpařuje, neboť atomy jódu jsou vázány pevnou
iontovou vazbou s atomy sodíku. Není tedy pravda vžité
paradigma, že při práci s otevřeným jodidem Na131I
se do vzduchu uvolňuje ("sublimuje") radionuklid
jód-131. Uvolňovat se může jedině plynný radionuklid xenon
131mXe. Jiná je situace u složitějších sloučenin
radiojódu, např. 131I-MIBG, kde vazba není tak
silná a určté menší množství jódu se ze sloučeniny
uvolňuje. V parách nad vzorkem pak vedle xenonu-131m můžeme
pozorovat i radiojód-131 (spektrometricky jsme prokázali).
 |
Přeměnové schéma a
gama-spektrum metastabilního xenonu 131mXe.
Plynný vzorek 131mXe byl získán
separací z preparátu radiojódu 131I
odsátím plynu nad hladinou roztoku 131I-jodidu
sodného. |
Podle přeměnového schématu na
obrázku vlevo metastabilní 131mXe s poločasem 11,96 dní deexcituje izomerním
přechodem (IT) na základní stav 131Xe. Jen v necelých 2% je to přímou emisí fotonů
gama o energii 164keV. V 98% dochází k vnitřní
konverzi (IC) emisí obalového elektronu atomu xenonu,
převážně ze slupky K (61%), částečně i ze slupky L (28%)
a z vyšších slupek M,N (8%). Takto emitované konverzní
elektrony pak mají řadu diskrétních energií v
rozsahu 129-163,8 keV. Na "uprázdněná místa" po
konverzních elektronech vzápětí přeskakují elektrony z
vyšších hladin, což vede k intenzívní emisi fotonů charakteristického
X-záření s diskrétními energiemi v rozsahu cca
29-34keV. Částečnou vnitřní konverzí tohoto X-záření
jsou dále emitovány Augerovy elektrony o
energiích 23-34keV (a též o velmi
nízkých energiích 2,5-5,5keV).
Na obrázku vpravo je výsledné gama-spektrum
změřené s takto odseparovaným vzorkem 131mXe. Dominuje zde charakteristické X-záření (linie Ka,b)
xenonu 30keV, vznikající v důsledku silné vnitřní konverze
při deexcitaci vzbuzené hladiny 164keV. Fotopík vlastní gama
linie 164keV 131mXe je podstatně nižší, ve spektru je však velmi
dobře patrný, zvláště ve zvětšeném výřezu.
Výroba a použití radiojódu 131I
Isotop 131I
lze získat ozařováním teluru neutrony v jaderném reaktoru
reakcí 130Te(n,g)131mTe, s následnými
radioaktivními přeměnami 131mTe(g, T1/2=30hod..)®131Te(b-, T1/2=25min.)®131I. Většinou se však radiojód 131I připravuje separací ze štěpných produktů 235U.
Jód 131I má v nukleární medicíně klíčový význam pro
diagnostiku (složka gama) a hlavně terapii
(složka beta) onemocnění štítné žlázy (§4.9.1 "Thyreologická
radioisotopová diagnostika"
a §3.6, část "Radioisotopová
terapie"). Používá se též pro cílenou radioisotopovou
terapii neuroendokrinních nádorů (131I-MIBG) a lymfomů (131I-Bexxar).
Pro scintigrafickou diagnostiku má 131I nevýhodu v
poměrně vysoké radiační zátěži,
způsobené ozářením tkáně energetickými beta částicemi.
Tam, kde je nezbytně potřeba jód, je proto 131I v poslední době
pro diagnostiku nahrazován isotopem 123I (viz níže). V řadě vyšetření pak ještě lépe
např. 99mTc,
které je čistým gama-zářičem s ještě daleko nižší
radiační zátěží.
Jód
123I
Dalším radioisotopem jódu používaným
v nukleární medicíně je 123I. S poločasem T1/2=13,2
hod. se přeměňuje elektronovým záchytem
na tellur 123Te *), především na jeho excitovanou hladinu 159keV
(97%), z níž pochází hlavní energie záření g používaná pro
scintigrafii. Záření gama emitované při dexcitaci z
vyšších energetických hladin (cca 400-1000keV) má velmi
malou intenzitu, takže se prakticky neuplatňuje.
Deexcitačními přechody v atomovém obalu po elektronovém
záchytu dále vzniká intenzívní charakteristické
X-záření (Ka,b) 27-31 keV.
*) Dceřinný telur-123 je slabě radioaktivní,
přeměňuje se s velmi dlouhým poločasem 12 miliard roků
elektronovým záchytem na antimon (stibium)-123. Aktivita 123Te v používaných
preparátech (desítky MBq) po rozpadu 123I je však neměřitelně nízká,
milionkrát menší než je přírodní pozadí.

Přeměnové schéma a spektrum záření gama jódu 123I
Isotop 123I se připravuje protonovým či deuteronovým
ozařováním teluru nebo xenonu v cyklotronu pomocí několika
jaderných reakcí. S telurem (obohaceným
příslušným isotopem) je to reakcemi 123Te(p,n)123I, 122Te(d,n)123I, nebo 124Te(p,2n)123I. Častější
metodou výroby isotopu 123I je ozařování xenonu (vysoce
obohaceného isotopem 124Xe) protony o energii 25MeV, při
němž dochází souběžně ke třem druhům jaderných reakcí:
124Xe(p,2n)123I - přímý vznik 123-jódu ; 124Xe(p,pn)123Xe(b+,EC, T1/2=3,9min.)®123I ; 124Xe(p,2n)123Cs(b+,EC, T1/2=5,9min.)®123Xe(b+,EC, T1/2=2,08hod..)®123I. Po ozařování se z terčíkové komůrky s xenonem
za cca 12hod. (až se 123Xe rozpadne na 123I) odseparuje výsledný 123I a zbylý xenon 124Xe se recykluje pro
opakované použití.
Jódem-123 se značí některá radiofarmaka
pro scintigrafii. Především je to jodid sodný Na123I pro scintigrafii
štítné žlázy (§4.9.1 "Thyreologická radioisotopová
diagnostika"). Pro scintigrafii receptorových systémů v mozku se
používá 123I-ioflupane a 123I-IBZM (§4.9.8, část "Scintigrafie receptorových
systémů v mozku"). Ve srovnání s jódem 131I má 123I vhodnější energii gama, a jelikož neemituje
záření beta, způsobuje při vyšetření podstatně nižší
radiační zátěž pro pacienta.
Jód 125I
Radiojód 125I (X 27+31keV, g 35keV) se s poločasem T1/2=59,4
dnů přeměňuje elektronovým záchytem
na excitovanou hladinu 35,5keV telluru 125Te. Deexcitací na základní stav se emituje záření
gama energie 35,5keV (6,63%). Po elektronovém záchytu
se dále emitují fotony charakteristického X-záření
telluru Ka 27,2-27,4 keV (100%) a Kb 30,9-31,8 keV
(25%); toto X-záření je dominantní. Kromě toho se po
elektronovém záchytu v důsledku vnitřní konverze gama a X z
elektronového obalu dceřinného teluru emituje větší
množství Augerových a konverzních elektronů
s energiemi 0,7-30 keV (cca 20
elektronů/1rozpad). V gama-spektru 125I jsou vidět píky
charakteristického X-záření kolem 30keV a pík gama 35keV (na scintilačním detektoru splývají v jeden širší
pík) a při dobré detekční účinnosti
též sumační pík kolem 65keV, vznikající
koincidenční detekcí fotonů gama+X *). Při měření vzorků
125I ve
studnovém scintilačním detektoru s detekční účinností cca
80% může být sumační pík dokonce dominantní.
*) Při elektronovém záchytu zde
dochází k přeskoku elektronů v obalu za vzniku fotonu
charakteristého X-záření a prakticky současně k
deexcitaci vzbuzené hladiny 35,5keV 125Te s emisí fotonu gama. Oba tyto fotony pak
přicházejí do detektoru současně a mohou být koincidenčně
detekovány za vzniku impulsu odpovídajícího součtu
obou energií, cca 65keV.

Přeměnové schéma a gama-spektrum radiojódu 125I.
Isotop 125I se připravuje ozařováním xenonu (obohaceného isotopem 124Xe) neutrony v reakci 124Xe(n,g)125Xe s následnou
radioaktivní přeměnou 125Xe(EC, T1/2=16,9hod.)®125I.
Jód 125I se v nukleární medicíně používá pro in vitro radioimunoanalýzu
(§3.5 "Radioisotopové
stopovací metody") a v radioterapii pro permanentní intersticiální
brachyterapii (§3.6, část "Brachyradioterapie").
Jód 129I
se s dlouhým poločasem T1/2=1,57.107roků přeměňuje beta--radioaktivitou na excitovaný stav 39,6keV
xenonu 129Xe,
při jehož dexcitaci jsou emitovány gama-fotony
o téže energii. Vzhledem k vysoké vnitřní konverzi
fotonů gama jsou též emitovány konverzní elektrony a
výrazné charakteristické X-záření o
energii kolem 30-34keV (avšak přece jen
ne tak intenzívní jako při elektrovém záchytu u jódu-125).
129I se ve
stopových nmožstvích vyskytuje v přírodě - v zemské kůře
vzniká při štěpení uranu, v atmosféře vzniká jako
kosmogenní radionuklid z xenonu reakcemi vyvolanými kosmickým
zářením. V novější době 129I vzniká při štěpení uranu-235 a plutonia-238,
odkud se uvolňuje při přepracování vyhořelého jaderného
paliva. Vzhledem k podobnosti gama-spektra I-129 a I-125 se
etalony 129I
používají při kalibraci detekčních
systémů pro měření vzorků 125I v radioimunoanalýze.
Pozn.: Za
zajímavost stojí využití radioisotopu 129I, resp. analýzy zvýšeného obsahu
jeho stabilního dceřinného isotopu 129Xe v některých meteoritech, v tzv. jód-xenonové
chronometrii pro určování doby jejich vzniku -
viz výše část "Radioisotopové
(radiometrické) datování",
pasáž "Datování
pomocí rozpadlých radionuklidů".

Přeměnové schéma a gama-spektrum radiojódu 129I.
Spektrum je velice podobné výše
zobrazenému spektru jódu 125I. Drobný rozdíl je v poněkud menším relativním
zastoupení charakteristického X-záření vzhledem ke
gama-linii 39,6keV. Dále není přítomen sumační pík X(Ka,b)+g, neboť
charakteristické X-záření zde vzniká v důsledku vnitřní
konverze fotonů gama, které tím zanikají a místo nich
emitované fotony X nemají s čím "koincidovat". Při
každé radioaktivní přeměně 129I se emituje buď foton gama 39,6keV, nebo foton X
30-34keV, nikdy oba současně.
Jód
124I
je pozitronový radionuklid, který se s
poločasem 4,18 dní přeměňuje beta+-radioaktivitou
(23%) a elektronovým
záchytem (77%)
na základní stav (27%) a řadu excitovaných stavů 124Te: 603 (30%),
1325(6%), 2295 (19%) keV a další. V poměrně složitém
gama-spektru 124I dominuje anihilační e-e+ pík 511keV
(46%), dále gama píky 603 (63%), 723 (10,4%), 1326 (1,5%), 1376
(1,7%), 1509 (3,1%) a 1691 (11%) keV. Řada dalších slabých
gama píků (až po téměř 3000keV) je vidět teprve při velkém zvětšení. Na začátku
spektra jsou v důsledku elektronového záchytu patrné slabší
Ka,b
píky 27-31keV charakteristického X-záření teluru. Pro
aplikace 124I je důležité pouze pozitronové záření
a z něho vznikající anihilační g-záření
511keV.
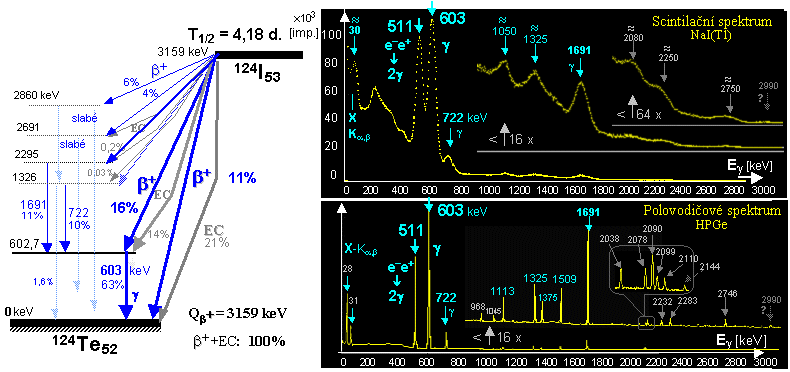
Přeměnové schéma a gama spektrum jódu 124I (vzorek I-124 pro
spektrometrické měření laskavě poskytli Mgr.A.Čepa a
Ing.J.Červenák z ÚJV Řež)
Isotop 124I se připravuje v cyklotronu ozařováním isotopů
teluru protony či deuterony v reakcích 124Te(p,n)124I, nebo 124Te(d,2n)124I, či 126Te(p,3n)124I.
Jódem-124 značená radiofarmaka se pokusně
využívají v pozitronové emisní tomografii PET
("§4.3 "Pozitronová emisní tomografie PET", §4.8 "Radionuklidy a radiofarmaka pro
scintigrafii", pasáž "Radionuklidy a radiofarmaka pro PET"). V nukleární
thyreologii se ve formě jodidu Na124I může použít při scintigrafii u ca
štítné žlázy, kde vzhledem k vyšší citlivosti a
rozlišení PET ve srovnání s planární a SPECT scintigrafií
může 124I-PET/CT
zlepšit detekci metastáz a reziduální tkáně štítné
žlázy, stanovení metabolických objemů nádorů a
preterapeutickou dozimetrii při terapii radiojódem, přesné
měření příjmu jódu během léčby.
Vzhledem k poměrně delšímu poločasu (ve srovnání např. s 18F nebo 68Ga) může být 124I vhodný pro PET
zobrazování pomalejších biologických a fyziologických
procesů sloučenin s vysokou molekulovou hmotností. Je to
zvláště radioimunodiagnostika se značením těžších
monoklonálních protilátek s pomalejší farmakokinetikou.
Zkouší se značený 124I-MIBG
(meta-jodbenzylguanidin) pro zobrazení neuroblastomu a feochromocytomu (s příp. následnou radionuklidovou terapií 131I-MIBG). Dále se zkouší 124I-beta-CIT (2beta-carbomethoxy-3beta-(4-iodophenyl)tropane) pro PET zobrazení dopaminového transportéru v mozku
u Parkinsonovy choroby. Značený jódouracyl 124I-2´-deoxyuridin
(UdR), pomocí jeho včlenění do molekul DNA a RNA, zobrazuje
potenciál růstu nádorů.
Vyskytují se i úvahy o terapeutickém
využití Augerových elektronů z 124I (je diskutováno §3.6, části
"Radioisotopová terapie", pasáž "Beta a alfa radionuklidy pro
terapii", odstavec "Terapie
Augerovými elektrony").
Pozn.: Určitým problémem 124I pro PET aplikace
je poměrně nízké zastoupení potřebých pozitronů (23%) a
naopak nežádoucí intenzívní gama-záření 603keV (63%),
emitované často současně, které je energeticky blízké
anihilačnímu záření 511keV - v poměrně širokém
pracovním okně analyzátoru není od 511keV prakticky
odlišitelné. Může tím docházet ke zhoršování kontrastu
obrazu vlivem nepravých koincidencí. Dále, značně vysoká
energie vyzařovaných pozitronů kolem 2100keV, které proto
mají v tkáni poměrně dlouhý dosah cca 5mm, poněkud
zhoršuje prostorové rozlišení PET obrazu.
 Xenon Xe54,
se svým radioaktivním isotopem 133Xe, byl zařazen již výše do oddílu "Rubidium-Krypton-Xenon", pasáž "Xenon", z důvodu podobnosti aplikací. Metastabilní
xenon 131mXe
byl popsán výše v části "Radiojód 131I", pasáž "Metastabilní xenon 131mXe".
Xenon Xe54,
se svým radioaktivním isotopem 133Xe, byl zařazen již výše do oddílu "Rubidium-Krypton-Xenon", pasáž "Xenon", z důvodu podobnosti aplikací. Metastabilní
xenon 131mXe
byl popsán výše v části "Radiojód 131I", pasáž "Metastabilní xenon 131mXe".
 Cesium
Cesium 
Cesium Cs55 je lehký měkký stříbřitě nažloutlý alkalický
kov, snadno tavitelný (teplota tání
28,4°C, teplota varu 670,8°C), který je
velmi reaktivní, takže se v přírodě vyskytuje jen ve
sloučeninách, a to poměrně vzácně (cca 1-5mg/kg v zemské
kůře). Kovové cesium má nízkou energii pro emisi elektronů.
V atomové a jaderné fyzice se proto používá ve
fotoelektrických součástkách, jako jsou fotonásobiče
- fotokatoda bývá slitinou cesia a antimonu (§2.4 "Scintilační detekce a spektrometrie
záření gama", část "Fotonásobiče"). Hyperjemná struktura
elektronů v atomech cesia se využívá ve velmi přesných tzv.
atomových hodinách (pasáž
"Exaktní -ideální -
měření prostoru a času"
v §1.6 "Čtyřrozměrný prostoročas a speciální teorie
relativity" monografie "Gravitace, černé díry a
fyzika prostoročasu").
Cesium má jediný stabilní isotop 133Cs. Velmi důležitý je radioaktivní isotop cesia :
Cesium
137Cs
Jedním z nejznámějších a nejpoužívanějších
radionuklidů vůbec je cesium 137Cs.
Je to b-+g zářič s jedinou energií záření gama 662keV.
137Cs se s
poločasem 30,05 let přeměňuje beta--radioaktivitou na stabilní baryum 137Ba - v 5,6% na
základní stav, v 94,4% na excitovanou hladinu 662keV (za zmínku stojí, že hladina 662keV je metastabilní
s poločasem 2,55min., který je však vzhledem k základnímu
poločasu 137Cs 30let zcela zanedbatelný). 137Cs se používá jako hlavní etalon
pro gama-spektroskopii (§2.4, část
"Spektrometrie záření gama"), dále k ozařování v
radioterapii (§3.6, část "Isocentrická
radioterapie"), v defektoskopii (§3.3, část
"Radiační
defektoskopie") a v řadě dalších měřících a technických
aplikací.
137Cs vzniká při neutronovém štěpení uranu 235U (popř. plutonia
239) v jaderném reaktoru z primárního štěpného produktu
jódu 137I
dvěma přeměnami beta-: 137I(b-, T1/2=23s.)®137Xe(b-, T1/2=3,9min.)®137Cs; výtěžek je 6%. Preparáty 137Cs se získávají radiochemickou separací ze
štěpných produktů (metodou PUREX
- §1.3 "Jaderné reakce a jaderná energie", pasáž
"Jaderné odpady").

Přeměnové schéma a gama-spektrum cesia 137Cs.
 Baryum
Baryum 
Baryum Ba56 je měkký lehký kov ze skupiny alkalických zemin,
který je velmi reaktivní, takže se v přírodě vyskytuje
pouze v barnatých sloučeninách, a to poměrně vzácně (cca
0,02-0,04% v zemské kůře). Rozpustné soli barya jsou značně
toxické. Důležitou minerální sloučeninou barya je síran
barnatý BaSO4 nazývaný baryt, jehož vodní
suspenze má poměrně vysokou hustotu a účinně
pohlcuje X-záření. Využívá se proto jako kontrastní
látka při rentgenovém snímkování zažívacího
traktu (§3.2, část "Kontrastní látky") a jako složka barytových
omítek, kterými jsou pokrývány stěny rentgenových
vyšetřoven pro zabránění nežádoucímu prozařování do
okolních prostorů.
Přírodní baryum je směsí 7 stabilních isotopů: 130Ba (0,11%), 132Ba (0,1%), 134Ba (2,42%), 135Ba (6,59%), 136Ba (7,85%), 137Ba (11,23%), 138Ba (71,7%). Z
radioaktivních isotopů barya má praktické využití jen
133-Ba:
Baryum
133Ba
se s poločasem 10,54 roků přeměňuje elektronovým
záchytem na excitované stavy 133Cs; při jeho deexcitaci jsou emitovány fotony g-záření
převážně o energiích 81, 276, 303, 356 a 384 keV. Po
elektronovém záchytu se dále emitují fotony charakteristického
X-záření cesia Ka 30,6-31 keV (60%) a Kb 34,9-36,8 keV
(18%) a Augerovy elektrony. Isotop 133Ba se připravuje protonovým ozařováním v cyklotronu
reakcí 133Cs(p,n)133Ba.
Pro
blízkost hlavní energie gama 356keV 133-barya k energii 364keV 131I se na některých
pracovištích nukleární medicíny používají baryové
pointery pro vyznačování pozice a struktur při
scintigrafii štítné žlázy radiojódem (§4.9.1
"Thyreologická radioisotopová
diagnostika"). Někdy se též 133Ba používá jako kalibrační etalon u
radiometrů.
Pozn.: V minulosti se isotop 133-Ba
zkoušel jako stopovací radioindikátor pro zjišťování
kinetiky radia v životním prostředí.

Přeměnové schéma a gama-spektrum barya 133Ba.
 Samarium
Samarium 
Samarium Sm62 je měkký stříbřitě lesklý kov ze skupiny
lantanoidů (jeho objevitel P.E.L.Biosbaudran
v r.1879 odvodil název od minerálu samarskitu, který
v r.1847 na jižním Uralu nalezl V.E.Samarskij-Bychovec). V pozemské přírodě se vyskytuje ve formě
sloučenin, koncentrace v zemské kůře je cca 6mg/kg. V
kombinaci s kobaltem se samarium používá pro výrobu silných
permanentních magnetů. Samarium má 5 stabilních isotopů: 144Sm (3,07%), 149Sm (13,82%), 150Sm (7,38%), 152Sm (26,75%), 154Sm (22,75%).
Přírodní samarium obsahuje též dva velmi dlouhodobé
radioaktivní isotopy 147Sm (14,99%) a 148Sm (11,24%):
Samarium 147Sm
se s poločasem 1,06.1011 roků se přeměňuje alfa-radioaktivitou
(Ea=2,31MeV)
na základní stav 143Nb. Tento primordiální radioisotop 147Sm se svým
dceřinným produktem 143Nb se používá v jaderné geochrologii (viz výše "Radioisotopové
(radiometrické) datování").
Samarium 148Sm
se s poločasem 7.1015 roků se přeměňuje alfa-radioaktivitou
(Ea=1,96MeV)
na základní stav 144Nb. Tento primordiální radioisotop nemá žádné
využití.
Uměle se vyrábí isotop samaria-153:
Samarium
153Sm
se s poločasem 46,5 hodin přeměňuje beta--radioaktivitou (Ebmax=808keV)
na stabilní isotop 153Eu. Přeměny probíhají v 18,4% na základní stav (Ebmax=803keV) a dále na excitované stavy 153Eu 103keV (49,4%) a
173keV (31,3%). Jen v nepatrném procentu (<0,02%) vznikají
vyšší excitované stavy 270, 585, ...., 764 keV. Při
postupné deexcitaci 153Eu probíhá větší množství přechodů s emisí
gama-fotonů o energiích především 69,7keV (4,7%) a 103keV
(29%). Vnitřní konverzí excitovaných hladin jsou emitovány
konverzní elektrony a dále vzniká charakteristické
X-záření o energii 40-48 keV.

Přeměnové schéma a gama-spektrum
samaria 153Sm
.
Pozn: V pravé
části spektra jsou ve zvětšeném výřezu zobrazeny některé
gama-píky z radionuklidových nečistot 152Eu a 154Eu (podrobné spektrum radionuklidových kontaminantů
je na obrázku níže).
V gama-spektru 153Sm jsou, vedle brzdného záření, patrné především
výrazné fotopíky 70keV a 103keV; píky vyšších energií
jsou vidět až při silnějším zvětšení. Na začátku
spektra je přítomno charakteristické X-záření s liniemi Ka,b o
energii cca 45keV, vznikající při vnitřní konverzi z
excitovaných hladin 172 a 103 keV.
Radionuklidové nečistoty v samariu-153
V našem spektru vzorku samaria-153 ("Quadramet",
dodaného laskavostí kolegů prim.MUDr.A.Chodackého a vrchní
sestry H.Mixové z ONM Chomutov) nejsou
patrné slabé vyšší gama-píky, neboť jsou přezářeny radionuklidovými
kontaminanty europiem 152Eu a 154Eu. Na obrázku níže je gama-spektrum
samotných dlouhodobých kontaminantů, které bylo změřeno s 3
měsíce starým vzorkem samaria, v němž vlastní samarium-153
se již zcela rozpadlo a zůstaly jen nečistoty s delšími
poločasy rozpadu.

Gama-spektrum dlouhodobých radionuklidových nečistot ve 3
měsíce "vymřelém" vzorku samaria 153Sm.
Ve spektru, obsahujícím velké množství
gama-píků, jsme našli tři radioaktivní isotopy europia: 152Eu
(T1/2=13,5
let; jeho fyzikální vlastnosti a gama-spektrum je uvedeno
níže v pasáži Europium 152Eu), 154Eu
(T1/2=8,6
let) a 155Eu (T1/2=4,7 let).
Příslušné fotopíky těchto isotopů jsou vyznačeny podle
barevného přiřazení vpravo nahoře.
Isotop 153Sm se připravuje v jaderném reaktoru ozařováním
samaria (obohaceného isotopem 152Sm na 99%) neutrony reakcí 152Sm(n,g)153Sm. Ze stopových isotopových
nečistot v terčíku vznikají přitom neutronovou fúzí i
výše zmíněné radionuklidové nečistoty 152,154,155Eu.
Beta-záření samaria-153 s fosfátovým ligandem
EDTMP (který se váže na kostní
hydroxyapatit v místech zvýšené osteoblastické aktivity) se v nukleární medicíně používá k paliativní terapii
kostních metastáz ca prsu a prostaty (§3.6, část "Radioisotopová
terapie").
 Europium
Europium 
Europium Eu63 je měkký lesklý kov ze skupiny lanthaniodů.
V pozemské přírodě se vyskytuje jen ve sloučeninách a je
poměrně řídce zastoupeno (cca 1,2mg/kg v zemské kůře).
Nejčastější použití europia je v luminiscenčních
materiálech. Europium má dva stabilní isotopy 151Eu (47,8%) a 153Eu (52,2%) (u 151Eu byla v poslední době objevena
nepatrná a-radioaktivita s extrémně dlouhým poločasem cca 5.1018let
- z praktického hlediska jej lze ale považovat za stabilní). Z radioaktivních isotopů je poněkud významné
europium-152:
Europium
152Eu
S poločasem 13,54 roků se přeměňuje
značně složitým rozvětveným rozpadovým schématem. V 27,9%
dochází k b--radioaktivitě na excitované hladiny 152Gd, v 71,9%
probíhá elektronový záchyt (v nepatrném procentu též konkurenční beta+-přeměna) na excitované hladiny 152Sm *). Při deexcitacích vzniklých vzbuzených stavů
dceřinného gadolinia-152 a samaria-152 je emitováno velké
množství (téměř 100) fotonů gama-záření,
z nichž významnou intenzitu mají fotony s energií: 122, 245,
344, 779, 867, 964, 1086, 1112 a 1408 keV. Pro tento velký
energetický rozsah výrazných linií gama je 152Eu používáno jako
výhodný kalibrační etalon v gama-spektrometrii
(kap.2 "Detekce a
spektrometrie ionizujícího záření",
§2.4, část "Spektrometrie záření gama").
*) Dceřinné samarium 152Sm je stabilní,
avšak dceřinné gadolinium 152Gd je nepatrně radioaktivní - s
obrovsky dlouhým poločasem 1,1.1014let
se přeměňuje alfa-radioaktivitou na 148Sm (a to pak s
ještě delšími poločasy dalšími dvěma alfa-přeměnami na 144Nd a nakonec na
stabilní 140Ce). Radiace těchto terciálních radionuklidů je
zcela zanedbatelná.
Isotop 152Eu vzniká při ozařování europia pomalými neutrony
v jaderném reaktoru v reakci 151Eu(n,g)152Eu.

Rozpadové schéma a gama-spektrum europia 152Eu
Europium 152mEu
je jeden z nemnoha metastabilních jader (izomerů), které mají
natolik odlišné kvantové vlastnosti od
základního stavu (především hodnotu spinu), že nedochází
k obvyklému přechodu do základního stavu emisí fotonů g-záření, ale k
radioaktivní přeměně beta-, beta+ či elektronovému záchytu, na jiné
sousední jádro (§1.2, pasáž "Jaderná izomerie a metastabilita"). 152mEu vůbec nedeexcituje na
základní 152Eu, ale s poločasem 9,31
hod. se ze 73% b--radioaktivitou
přeměňuje na 152Gd a z 27% elektronovým záchytem
a b+ na 152Sm. Isotop 152mEu
vzniká ozařováním europia v jaderném reaktoru reakcí 151Eu(n,g)152mEu.
Poměrně "exotický" isotop 152mEu nemá
žádné praktické využití a kromě zvláštní nefotonové
přeměny izomeru jej zde zmiňujeme i proto, že jej v r.1958
použil M.Goldhaber a spol. ke zjištění tzv. helicity
neutrina (§1.2, část "Neutrina - "duchové"
mezi částicemi",
pasáž "Odlišnost neutrin a antineutrin -
helicita neutrin. Goldhaberův pokus.").
Europium 154Eu
se s poločasem 8,6 let z 99,8% přeměňuje beta--radioaktivitou
na excitované hladiny 154Gd, z 0,2% elektronovým záchytem na excitované
stavy 154Sm. Při
deexcitacích je emitováno záření gama především o
energiích 123, 248, 592, 723, 996, 1005 keV.
Europium 155Eu
se s poločasem 4,7 let přeměňuje beta--radioaktivitou
na excitované hladiny a na základní stav 155Gd. Při deexcitacích je emitováno záření gama
především o energiích 87 a 105 keV.
Směsné gama-spektrum isotopů europia 152,154,155Eu můžeme vidět výše na
spektrometrickém měření radionuklidových
nečistot ve vzorku samaria-153.
 Gadolinium
Gadolinium 
Gadolinium Gd64 je tvárný lesklý kov ze skupiny lanthaniodů.
V pozemské přírodě se vyskytuje jen ve sloučeninách a je
poměrně řídce zastoupeno (cca 6,2mg/kg v zemské kůře),
těží se především z minerálu monazitu. Gadolinium má
zajímavé magnetické vlastnosti: při nižších teplotách pod
20°C je feromagnetický, při vyšších teplotách
paramagnetický. Používá se jako kontrastní látka v
nukleární magnetické rezonanci MRI. Další použití
gadolinia je v luminiscenčních materiálech v
rentgenologii. Isotop 157Gd má velmi vysoký účinný průřez (cca 260 000 barnů) pro záchyt
tepelných neutronů, používá se proto v některých
jaderných reaktorech.
Gadolinium má šest stabilních isotopů: 154Gd (2,2%), 155Gd (4,8%), 156Gd (20,5%), 157Gd (15,6%), 158Gd (24,8%) a 160Gd (21,9%). V přírodním gadoliniu se dále vyskytuje
přírodní radionuklid primordiálního původu 152Gd (0,2%) s velmi
dlouhým poločasem cca 1014 let (alfa radioaktivitou se
přeměňuje na 148Sm).
Z radioaktivních isotopů se občas používá gadolinium-153 :
Gadolinium
153Gd
S poločasem 240,2 dní se přeměňuje elektronovým
záchytem na 153Eu v základním stavu (4%) a v excitovaných stavech
97keV (38%), 103keV (42%) a 173keV (16%). Při dexcitaci se
emitují fotony gama záření především o
energiích 97 a 103 keV. Na začátku spektra jsou výrazné
píky Ka,b charakteristického X-záření
europia s energiemi kolem 44keV.
Isotop 153Gd se většinou připravuje z europia. Ozařováním
neutrony v jaderném reaktoru vzniká kombinací: 153Eu(n,g)152mEu(b-,T1/2=92min)®153Eu® 152Gd; 152Gd(n,g)153Gd. Nebo ozařováním alfa-částicemi v cyklotronu
vzniká posloupností procesů: 151Eu(a,2n)153Tb(b+,T1/2=2,3d)®153Gd.
Gadolinium 153Gd se používalo jako dvoufotonový zdroj záření
gama 103keV a X 44keV v kostní denzitometrii metodou
DEXA (§3.2, pasáž "Kostní
densitometrie"), dělaly se i
experimenty s využitím v CT. Občas se dosud využívají gadoliniové
tyče u scintigrafického zobrazení SPECT pro korekci
intenzity gama záření na zeslabení při průchodu tkání (§4.3, pasáž "Nepříznivé
vlivy u SPECT a jejich korekce",
bod "Absopce záření gama"). Tyto metody se ale příliš neosvědčily a jsou
vetšinou již opuštěné...

Přeměnové schéma a gama-spektrum gadolinia 153Gd .
 Erbium , Yterbium , Terbium
Erbium , Yterbium , Terbium 
Názvy pro některé lantanoidy "terbium,
ytrium, erbium, yterbium" vznikly historicky podle
švédské vesnice Ytterby, poblíž které byly v
těžebním lomu na živec v minerálech gadolinitu a monazitu
tyto prvky poprve objeveny.
 Erbium Er71 je měkký stříbřitě lesklý kov ze skupiny
lantanoidů. V zemské kůře je obsaženo ve formě sloučenin v
koncentraci cca 2,5mg/kg. Má 6 stabilních isotopů: 162Er (0,14%), 164Er (1,6%), 166Er (33,5%), 167Er (22,87%), 168Er (26,98%), 170Er (14,91%).
Erbium Er71 je měkký stříbřitě lesklý kov ze skupiny
lantanoidů. V zemské kůře je obsaženo ve formě sloučenin v
koncentraci cca 2,5mg/kg. Má 6 stabilních isotopů: 162Er (0,14%), 164Er (1,6%), 166Er (33,5%), 167Er (22,87%), 168Er (26,98%), 170Er (14,91%).
Z radioaktivních isotopů má praktický význam jeden:
Erbium
169Er
je uměle vyráběný radionuklid, který se s poločasem 9,39
dní přeměňuje b--radioaktivitou z 55% na základní (Ebmax=353keV) a ze 45% na nízký excitovaný stav 169Tm s energií
8,41keV (při deexcitaci je emitováno
nízkoenergetické záření g této energie). S velmi malou
intenzitou vzniká excitovaný stav 118keV. Erbium-169 je prakticky
čistým zářičem beta, neboť měkké záření gama
8,4keV podléhá téměř z 99% vnitřní konverzi, především
na slupkách M a N atomu Tm (s výraznou
emisí nízkoenergetických konverzních elektronů 0,7-8,4 keV,
cca 250%) a linie 110, 118keV je primárně
velmi slabá.

Přeměnové schéma a gama-spektrum erbia 169Er .
Pozn.: Erbium 169 má jen dva
velmi slabé gama-píky 110 a 118
keV (ve spektru jsou vyznačeny modrými šipkami). Množství
dalších píků naměřených v našem spektru pochází z
drobných radionuklidových nečistot, které
měřený vzorek erbia-169 obsahoval. Naměřili jsme
především yterbium 169Yb s píky: 50,57,59keV (X-Ka,b Tm), 63, 110,
118, 130, 177, 198, 308 keV (jeho fyzikální vlastnosti a
gama-spektrum je uvedeno níže v pasáži Yterbium 169Yb). Dále samarium 153Sm: 70, 103 keV (jeho fyzikální
vlastnosti a gama-spektrum je uvedeno výše v pasáži Samarium 153Sm); erbium 172Er: 407, 610 keV; lutetium 177Lu:
113, 208, 250, 321 keV (jeho fyzikální vlastnosti a
gama-spektrum je uvedeno níže v pasáži Lutetium 177Lu); nakonec stopové množství thulia 172Tm:
79, 182, 1093, 1120, 1387, 1466, 1529, 1608 keV. Vzhledem k velmi
slabému záření gama vlastního 169Er se i malé množství uvedených nečistot (<0,1%)
ve spektru výrazně projeví, přezáří dokonce vlastní gama
erbia-169.
Ostatně, píky 110 a 118 keV patřící 169Er má i kontaminant 169Yb, takže v našem vzorku možná převážně ani
nepocházely z erbia-169..?..
Gama spektrum 169Er je tvořeno
především poměrně měkkým brzdným zářením se spojitým
spektrem, které se s klesající tendencí táhne až asi k
300keV. Při delší akvizici se na tomto spojitém pozadí
objevují sotva patrné gama-píky 110 a 118 keV.
Ze spektrometrického
hlediska je tedy samotný radionuklid 169Er celkem
nezajímavý a fádní - na spojitém pozadí brzdného
záření jsou vidět jen dva velmi slabé sotva patrné
gama-píky 110 a 118 keV. Jaké
bylo však naše překvapení, když jsme vzorek cca 100kBq
preparátu erbia-169 (citrátu určeného
pro radiační synovektomii malých kloubů)
vložili do citlivého gama-spektrometru: po několika
desítkách minut akvizice se spektrum doslova
"ježilo" množstvím gama-píků, které však
samozřejmě nepatřily 169Er, ale radionuklidovým
nečistotám *) - viz obrázek výše s doprovodným textem.
*) Ze spektra na obrázku by se na první
pohled mohlo zdát, že těch radionuklidových nečistot je tam
neúnosně mnoho..?.. Je to však jen "optický klam"!
Erbium-169 má totiž velmi slabé zastoupení záření gama -
jen zhruba na každých 20 000 přeměn se emituje jeden
detekovatelný foton gama 110keV. Ty nečistoty jako je
yterbium-169, samarium-153, ...., však mají mnohonásobně
větší emisi gama (cca 1000-krát), takže i jejich velmi malá
koncentrace (na úrovni setin %) se ve spektru projeví
výrazněji než samotné 169Er..!..
Isotop 169Er se připravuje v jaderném reaktoru neutronovým
ozařováním oxidu erbia (obohaceného
isotopem 168Er) reakcí 168Er(n,g)169Er. Erbium-169 se ve formě koloidního roztoku citrátu
používá v nukleární medicíně pro radiační synovektomii
malých kloubů (prsty, zápěstí) - vzhledem k nízké
energii emitovaných beta-částic, s dosahem v tkáni cca 1mm.
 Yterbium
Yb70 je rovněž měkký stříbřitě bílý kov ze skupiny
lantanoidů. V zemské kůře je obsaženo ve formě sloučenin v
koncentraci cca 2,5-3mg/kg. Má 7 stabilních isotopů: 168Yb (0,13%), 170Yb (3,04%), 171Yb (14,28%), 172Yb (21,83%), 173Yb (16,13%), 174Yb (31,83%), 176Yb (12,76%).
Yterbium
Yb70 je rovněž měkký stříbřitě bílý kov ze skupiny
lantanoidů. V zemské kůře je obsaženo ve formě sloučenin v
koncentraci cca 2,5-3mg/kg. Má 7 stabilních isotopů: 168Yb (0,13%), 170Yb (3,04%), 171Yb (14,28%), 172Yb (21,83%), 173Yb (16,13%), 174Yb (31,83%), 176Yb (12,76%).
Občas se používá jeden uměle vyráběný
radioisotop yterbia :
Yterbium
169Yb
se s poločasem 32,02 dní přeměňuje elektronovým
záchytem (EC) na řadu excitovaných stavů thulia 169Tm: 316keV (5%),
379keV (82%), 473keV (13%); přeměny na
další vyšší excitované stavy mají velmi nízkou intenzitu
(<0,01%). Při kaskádových
deexcitacích se emituje mnoho energií fotonů gama, z nichž
významnější intenzitu mají energie 63, 110, 130, 177, 198 a
308 keV.

Přeměnové schéma a gama-spektrum yterbia 169Yb. Omluva: Polovodičové
spektrum bylo měřeno na starším detektoru Ge(Li) se
zhoršenými vlastnostmi.
V gama-spektru 169Yb dominují píky
charakteristického X-záření Ka,b 49-59keV,
dále gama-píky 63, 110, 130, 177, 198 a 308 keV. Píky z
přechodů 139->118keV a 9,4->0keV jsou slabé, protože
více než z 99% podléhají vnitřní konverzi. Řada dalších
vyšších píků v rozmezí 316-781keV je natolik nízká
(<0,01%), že u našeho slabého vzorku (cca
3kBq) se ve spektru nezobrazily.
Isotop 169Yb se připravuje v cyklotronu ozařováním oxidu
thulia protony v reakci 169Tm(p,n)169Yb....a dalšími reakcemi.....
Yterbium-169 se používalo v nukleární medicíně pro scintigrafickou
diagnostiku, především mozko-míšního řečiště (§4.9.8, pasáž "Scintigrafie
likvorových cest"). 169Yb se též zkoumá jako potenciální radioisotop pro brachyterapii
(§3.6, část "Brachyradioterapie") či defektoskopii
(§3.3, část "Radiační defektoskopie") s nižší průměrnou
energií gama (93keV) než obvykle používané iridium 192Ir.
 Terbium Tb65 je další měkký stříbřitě lesklý kovový prvek
ze skupiny lantanoidů. V zemské kůře je obsaženo ve formě
sloučenin v koncentraci cca 0,9mg/kg. Používalo se v
luminoforech v obrazovkách a v RTG zesilujících fóliích -
bylo vytlačeno elektronickým vývojem ditálního zobrazení;
nyní se používá jako součást záznamových vrstev
magnetooptických médií.
Terbium Tb65 je další měkký stříbřitě lesklý kovový prvek
ze skupiny lantanoidů. V zemské kůře je obsaženo ve formě
sloučenin v koncentraci cca 0,9mg/kg. Používalo se v
luminoforech v obrazovkách a v RTG zesilujících fóliích -
bylo vytlačeno elektronickým vývojem ditálního zobrazení;
nyní se používá jako součást záznamových vrstev
magnetooptických médií.
Terbium má jeden stabilní isotop 159Tb (100%). Z radioaktivních isotopů terbia se
experimentálně v nukleární medicíně zkoušejí čtyři
radionuklidy :
Terbium
149Tb
Tento uměle připravovaný radionuklid se s poločasem 4,12
hod. přeměňuje velmi složitým rozvětveným
rozpadovým schématem. V 76,2% dochází k elektronovému
záchytu a v 7,1% probíhá b+-radioaktivita
(střední Eb+=730keV), v obou případech na excitované hladiny 149Gd. V 16,7%
dochází alfa-radioaktivitě (Ea=3,97MeV)
na základní stav 145Eu. Při deexcitacích vzniklých vzbuzených stavů
dceřinného gadolinia-149 je emitováno velké množství (více
než 300 !) fotonů gama-záření, z nichž
významnou intenzitu mají fotony s energií: 165keV (26%),
352keV (29%), 389keV (18%), 652keV (16%), 817keV (12%), 853keV
(15%); další gama-píky vysoké energie až do více než
3000keV jsou slabé.
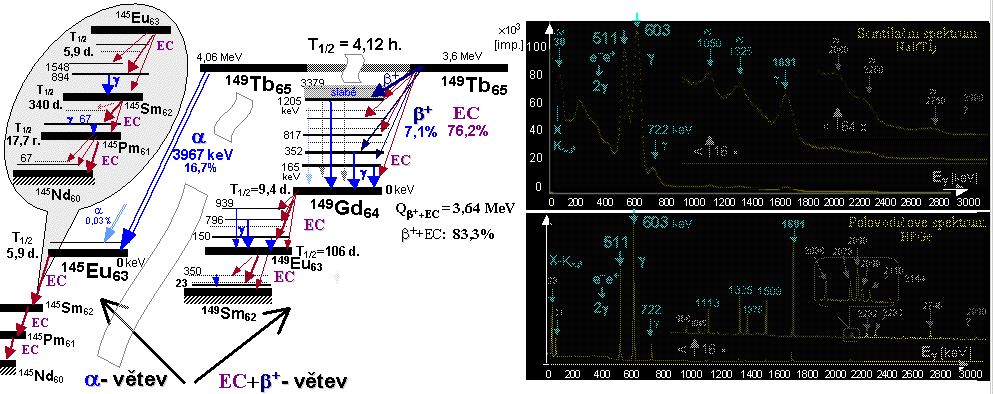
Přeměnové schéma a gama spektrum terbia
149Tb (.. gama-spektrum přijde změřit,
až se mi podaří opatřit vzorek 149Tb...) .
Z důvodu místa je složité rozpadové
schéma 149Tb
nakresleno zjednodušeně, bez podrobností slabě zastoupených
energetických hladin a přechodů.
Oba dceřinné radionuklidy jsou opět
radioaktivní. Dceřinné gadolinium 149Gd
z větve e-b+ se
spoločasem 9,4 dní přeměňuje elektronovým záchytem
na řadu excitovaných stavů europia 149Eu o energiích především 150, 490, 790, 950 a 1083
keV, s následnou emisí řady linií gama záření . Toto
europium 149Eu se pak opět elektronovým záchytem
přeměňuje s poločasem 106 dní na excitované stavy již
stabilního samaria 149Sm. Dceřinné europium 145Eu z alfa-větve se s poločasem 5,9
dne elektronovým záchytem přeměňuje nejprve na excitované
stavy samaria 145Sm za emise řady linií gama, především o energiích
653, 893, a 1658 keV. Toto samarium se pak s poločasem 340 dní
opět elektronovým záchytem přeměňuje na 145Pm, které se s
poločaem 17,7 roků též e-záchytem nakonec přeměňuje na
stabilní neodym 145Nd.
Příprava:
149Tb je zatím nestandardní isotop a v malých
množstvích se experimentálně připavuje třemi způsoby 1.
Přímé jaderné reakce s urychlenými protony (energie cca 100MeV) či jádry
hélia: 149Gd(p,
4n)149Tb,
nebo 151,153Eu(3,4He, x n)149Tb; 2.
Reakce vyvolané urychlenými těžšími ionty, např. jádry 12C: 141Pr(12C, 4n)149Tb, nebo 142Nd(12C, 5n)149Dy (b+,EC, T1/2 4min.)®149Tb; 3.
Tříštivé (spalační) reakce vysokoenergetických protonů,
např. na tantalový terčík: Ta(p, ..x..)149Tb, s isotopovou separací.
Pro nukleární
medicínu je terbium 149Tb zajímavé tím, že emituje jak alfa-částice,
tak pozitrony beta+. V chelatačním spojení 149Tb s vhodnými cílovými biomolekulami může být tentýž
preparát (radiofarmakum) použit jak pro diagnostické
zobrazení nádorových lézí pomocí pozitronové emisní
tomografie PET *), tak pro následnou biologicky cílenou
radionuklidovou terapii pomocí alfa-částic, s
příp. současným PET monitorováním průběhu
terapie - tedy pro teragnostiku (§4.9, pasáž "Kombinace
diagnostiky a terapie - teragnostika"); je to "monoteranostický"
radionuklid.
*) Pro gamagrafické zobrazení lze alternativně použít i
jednofotonovou planární či SPECT scintigrafii pomocí gama
záření 165 či 352 keV, emitovaného při deexcitaci
dceřinného 149Gd; vlivem velkého množství rušivého
vysokoenergetického g záření však kvalita obrazů není dobrá.
Radionuklid 149Tb se zatím
experimentálně zkouší v radioimunoterapii lymfomu pro
označení rituximabu pomocí chelátorů typu DOTA či
DTPA, s předběžně slibnými scintigrafickými i
terapeutickými výsledky.
Problémem teranostického
použití 149Tb může být složité rozpadové schéma,
obsahující několik dceřinných radioisotopů, některých
dlouhodobých. Vzhledem k poměrně krátkému poločasu 4,1hod.
je 149Tb
vhodné pro značení radiofarmak s menší molekulovou
hmotností, které jsou rychle odstraňovány z organismu. V
takovém případě by se potenciální radiotoxicita
dceřinných radiolanthanidů (přeměňujících
se nízkozátěžovými elektronovými záchyty) nemusela významněji projevit. Vzhledem ke svým
fyzikálním vlastnostem terbium-149 patrně zůstane jen jako
zajímavost, pravděpodobně se neosvědčí jako
teranostický radionuklid.
Terbium
152Tb
se s poločasem 17,5 hod. přeměňuje elektronovým
záchytem (79,7 %) a beta+-radioaktivitou (20,3 %) na excitované
stavy 152Gd
. Při deexcitacích jsou emitovány fotony gama o eneriích
271keV (9,5 %), 344 (63,5 %), 686 (3,2 %), 779keV (5,5 %) a při
pozitronové anihilaci fotony gama 511 keV (41 %).
Terbium-152 může být použito v nukleární medicíně pro
scintigrafii PET. Spíše než pro základní PET diagnostiku, se
zkouší v teranostickém přístupu, jako
doprovodný diagnostický isotop při PET/CT monitorování
biodistribuce terapeutických ligandů značených terbiem l61Tb - teranostická
dvojice l52Tb/l61Tb.
Terbium
155Tb
se s poločasem 5,32 dní přeměňuje elektronovým
záchytem (100 %) na excitované stavy 155Gd. Při
deexcitacích jsou emitovány fotony gama o energiích 105,3keV
(25,1%), 180,1 (7,5%), 262,3keV (5,3%).
Terbium-155 může být použito v nukleární medicíně pro
(jednofotonové) scintigrafické zobrazení planární/SPECT, v
zásadě podobně jako jód 123I nebo indium 111In. Avšak jeho hlavní potenciální využití se
očekává v teranostickém přístupu, jako
diagnostický isotop při scintigrafickém monitorování
biodistribuce terapeutických ligandů značených terbiem l61Tb - teranostická
dvojice l55Tb/l61Tb.
Terbium
161Tb
je uměle vyráběný radionuklid, který se s poločasem 6,9
dní přeměňuje beta--radioaktivitou
(Ebmax=593keV) na 161Dy - z 10% na
základní stav, dále na excitované stavy 25,6keV (10%),
74,5keV (65%), 131,7keV (25,7%) a dalších pět vyšších
energetických hladin v rozmezí 213-550 keV s velmi nízkým
zastoupením cca 0,01-0,06 %. Při deexcitaci vzbuzených jader
161-dysprosia jsou emitovány fotony záření gama
o energiích především 25,6keV (23%), 49keV (17%), 74,5keV
(10%), 88keV (0,2%), s nízkou intenzitou (cca 0,001-0,1 %) pak
vyšší energie v rozmezí 100-550 keV. Na začátku spektra
jsou píky charakteristického X-záření (Ka,b Dy) 45-54 keV (0,3-12 %).
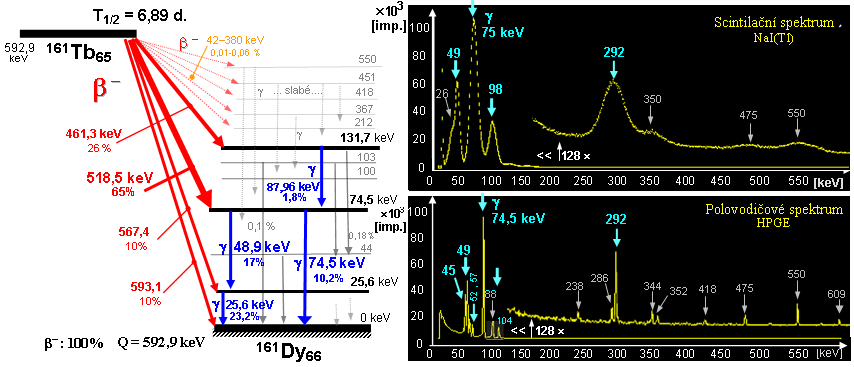
Přeměnové schéma a gama-spektrum terbia 161Tb .
Vzorek 161Tb byl připraven na reaktoru v ÚJV Řež z iniciativy
RNDr. Martina Vlka, PhD. Polovodičové spektrum pak bylo
změřeno za spolupráce Ing. Matěje Grapy ve Spektrometrické
laboratoři SÚRO v Ostravě. Autor moc děkuje oběma kolegům.
Radionuklid 161Tb se obvykle vyrábí v jaderném reaktoru neutronovým
ozařováním gadolinia vysoce obohaceného isotopem 160Gd pomocí reakce 160Gd(n,g)160Gd(b-, T1/2 3,6min.)
-->161Tb.
Terbium-161 se zatím experimentálně
používá v nukleární medicíně k biologicky cílené radioisotopové
terapii nádorových onemocnění (§3.6,
část "Radioisotopová
terapie"). 161Tb má podobné vlastnosti a terapeutické využití
jako již úspěšně používané lutetium 177Lu , oproti
němuž se očekává poněkud zvýšená terapeutická
účinnost, způsobená větším zastoupením konverzních
a Augerových elektronů 2,2 na 1 rozpad. Vysoké LET těchto
nízkoenergetických elektronů může být účinné při
likvidaci nádorových buněk (pokud je radionuklid internalizován
uvnitř nádorových buněk).
Pro terapii neuroendokrinních nádorů
lze použít konjugát chelátu 161Tb-DOTA s peptidem octreotidem, který
se váže na buňky neuroendokrinních nádorů s dostatečně
vysokou koncentrací somatostatinových receptorů.
Velmi dobré výsledky však ukazují především 161Tb- značené monoklonální
protilátky, jako je 161Tb-PSMA617 anti-prostatický specifický
membránový antigen (PSMA).
Tyto metody jsou stručně popsány v §3.6,
pasáž "Radioimunoterapie".
Terapeutický účinek má záření beta
o střední energii 154 keV (100%) a též konverzní a Augerovy
elektrony (220%) (které jsou hojněji
zastoupeny na jeden rozpad než u 177Lu). Emise gama
záření 74,6 keV umožňuje při terapii
současné scintigrafické zobrazení
tkání a orgánů, kam terapeutický preparát pronikl. Na
těchto scintigrafických obrazech můžeme posuzovat (vizuálně, příp. i kvantitativně) míru žádoucího vychytávání radiofarmaka v
nádorových ložiscích a nežádoucí akumulace ve zdravých
tkáních a kritických orgánech - provádět monitorování
průběhu radioisotopové terapie. Zastoupení
záření gama rovněž umožňuje snadné měření
aktivity preparátů 161Tb v běžných měřičích aktivity s ionizační
komorou (§2.3 "Ionizační komory"), za použití
příslušné kalibrace gama-konstanty.
Uvažuje se též o výborné teranostické
dvojici 155Tb pro scintigrafickou
diagnostiku planární/SPECT, nebo 155Tb pro PET a 161Tb pro biologicky cílenou radionuklidovou terapii
(zmíněné výše). Jedná se o radionuklidy téhož
prvku Tb, s identickými chemickými a tudíž i
biochemickými vlastnostmi a metabolismem.
 Lutetium
Lutetium 
Lutecium Lu71 je měkký bíle lesklý kov, poslední člen skupiny
lanthanoidů, který se ve formě sloučenin poměrně vzácně
vyskytuje v přírodě (0,5-0,7mg/kg v zemské kůře).
Využívá se ve scintilačních detektorech LSO
pro pozitronovou emisní tomografii (§2.4., část "Scintilátory a jejich vlastnosti", §4.3, část "Kamery PET "). Má jediný stabilní isotop 175Lu (97,4%), přičemž přírodní lutetium obsahuje
též 2,6% isotopu 176Lu, který je radioaktivní :
Lutetium
176Lu
je přírodní (primordiální) radionuklid, který se s velmi
dlouhým poločasem 3,76.1010 roků b--radioaktivitou přeměňuje na
stabilní hafnium 176Hf - na excitovaný stav 597keV. Deexcitace nastává
postupnou (kaskádovou) emisí fotonů gama o energiích 307, 202
a 88keV (slabě zastoupená je vyšší
energie 401keV, ve spektru se dále objevuje slabý sumační
pík 306+202keV). Využívá se pro
dlouhodobé datování v jaderné geochronologii při lutetium-hafniové
metodě (viz výše "Radioisotopové
datování"). Obsah přírodního 176Lu se poněkud nepříznivě projevuje na
"vnitřní kontaminaci" scintilátorů LSO
a jejich poměrně vysokém radiačním pozadí (viz §2.4 "Scintilátory a jejich vlastnosti " a
§4.3 "Kamery PET").
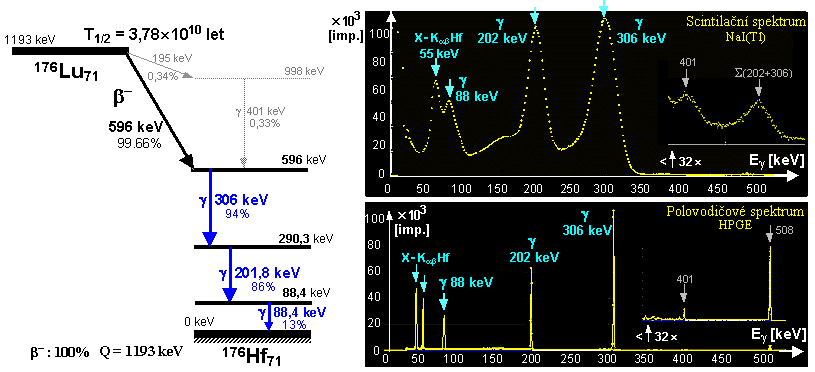
Přeměnové schéma a gama-spektrum lutetia 176Lu
Lutetium
177Lu
je uměle vyráběný radionuklid, který se s poločasem 6,65
dní přeměňuje beta--radioaktivitou
(Ebmax=498keV) na 177Hf - z 79,4% na
základní stav, dále na excitované stavy 113keV (9%) a 321keV
(11,6%). Při deexcitaci vzbuzených jader 177-hafnia jsou
emitovány fotony záření gama o energiích
především 113keV (6,2%) a 208keV (10,4%), s nízkou intenzitou
(cca 0,2%) pak 72, 250 a 321 keV. Na začátku spektra je pík
charakteristického X-záření (Ka,b Hf) 55-63 keV.

Přeměnové schéma a gama-spektrum lutetia 177Lu.
Pro zajímavost je vlevo nahoře náznakově zakresleno i
zjednodušené rozpadové schéma metastabilního izomeru 177mLu, který často
vzniká spolu s 177Lu.
Isotop 177Lu se vyrábí ozařováním neutrony v jaderném
reaktoru dvěma způsoby:
- Přímý způsob
spočívá v ozařování lutetia, obohaceného isotopem 176Lu, neutrony v
reakci 176Lu(n,g)177Lu. Díky vysokému
účinnému průřezu této reakce lze získat radionuklid o
poměrně vysoké specifické aktivitě. Určitou nevýhodou
tohoto postupu je současně probíhající reakce 176Lu(n,g)177mLu, při níž
vzniká jaderný izomer 177mLu s poločasem 160 dní. Tento nevítaný kontaminant
ve 22% dexcituje postupnými izomerními přechody na základní
stav 177Lu
a v 88% se přeměňuje samostatně b--radioaktivitou (Ebmax=153keV) na
poměrně vysoký excitovaný stav 1315keV dceřinného 177Hf, který
deexcituje řadou g-přechodů směrem k nižším hladinám. Při této
radioaktivitě 177mLu emituje řadu energií gama, z nichž některé jsou
stejné jako u 177Lu, avšak jsou zastoupeny i vyšší energie 228, 281,
319, 378, 418 keV a řada dalších. Radiace kontaminantu 177mLu dlouhodobě
zvyšuje radiační zátěž a zhoršuje kvalitu
scintigrafických obrazů.
- Nepřímý způsob spočívající v kombinaci
neutronového ozařování yterbia, obohaceného isotopem 176Yb, neutrony v
reakci 176Yb(n,g)177Yb a následné
beta-přeměny 177Yb(b-, T1/2=1,9hod.)®177Lu na výsledné lutetium-177. Při tomto způsobu
nevzniká rušivé 177mLu (při beta-přeměně 177Yb není sycena
metastabilní hladina 970keV 177mLu), může být přítomno pouze
stopové množství isotopů Yb, ....
 |
Gama-spektrum 3 měsíce starého
vzorku 177Lu
(preparát Betalutin).
Omluva: Při grafickém
zpracování spekter došlo k deformaci měřítek na
vodorovné ose. Číselné hodnoty energií nad píky
jsou však přesné. |
Lutetium-177 se používá v nukleární
medicíně k biologicky cílené radioisotopové terapii
nádorových onemocnění (§3.6, část
"Radioisotopová
terapie"). Okrajové je zde použití ve formě 177Lu-
EDTMP pro paliativní terapii kostních metastáz (neboť pro tento účel je odzkoušené stroncium 89Sr, samaruim 153Sm a rhenium 186Re). Častější je terapie neuroendokrinních
nádorů za použití konjugátu chelátu 177Lu-DOTA
s peptidem octreotidem, který se váže na buňky
neuroendokrinních nádorů s dostatečně vysokou koncentrací somatostatinových
receptorů. Velmi dobré výsledky však ukazují
především 177Lu- značené monoklonální protilátky,
jako je 177Lu-J591anti-prostatický specifický
membránový antigen (PSMA), nebo 177Lu-tetulomab anti CD-37 pro terapii lymfomů.
Tyto metody jsou stručně popsány v §3.6,
pasáž "Radioimunoterapie".
Terapeutický účinek má záření beta
o střední energii 134keV a též konverzní a Augerovy
elektrony. Výhodou 177Lu je, že emise gama záření
113 a 208 keV umožňuje při terapii současné scintigrafické
zobrazení tkání a orgánů, kam terapeutický
preparát pronikl. Na těchto scintigrafických obrazech můžeme
posuzovat (vizuálně, příp. i
kvantitativně) míru žádoucího
vychytávání radiofarmaka v nádorových ložiscích a
nežádoucí akumulace ve zdravých tkáních a kritických
orgánech - provádět monitorování průběhu
radioisotopové terapie. Zastoupení záření gama
rovněž umožňuje snadné měření aktivity
preparátů 177Lu v běžných měřičích aktivity s ionizační
komorou (§2.3 "Ionizační komory"), za použití
příslušné kalibrace gama-konstanty.
 Wolfram , Rhenium
Wolfram , Rhenium 
 Wolfram
(Tungsten) W74 je šedbíle lesklý, těžký (hustota 19,25g/cm3) a obtížně
tavilelný kov (teplota tání 3422°C). V přírodě je
zastoupen poměrně vzácně (cca 1,5-3,5 mg/kg v zemské
kůře), ve sloučeninách (rudách -
oxidech) s železem, manganem, vápníkem
či olovem. Wolfram má široké technické využití plynoucí z
jeho vysoké hustoty a tepelné odolnosti. Pro vysokou teplotu
tání se používá jako materiál pro žhavicí vlákna
v žárovkách a katodách elektronek (včetně elektronových
zdrojů v urychlovačích). Slitiny wolframu se využívají v
metalurgii pro zvýšení tvrdosti, mechanické
a tepelné odolnosti kovů. Pro svou vysokou hustotu se
používá jako účinné radiační stínění
X a gama záření (§1.6, část "Absorbce záření v látkách", pasáž "Stínění záření
gama"), především pro
výrobu kontejnerů a precizních kolimátorů.
Wolfram
(Tungsten) W74 je šedbíle lesklý, těžký (hustota 19,25g/cm3) a obtížně
tavilelný kov (teplota tání 3422°C). V přírodě je
zastoupen poměrně vzácně (cca 1,5-3,5 mg/kg v zemské
kůře), ve sloučeninách (rudách -
oxidech) s železem, manganem, vápníkem
či olovem. Wolfram má široké technické využití plynoucí z
jeho vysoké hustoty a tepelné odolnosti. Pro vysokou teplotu
tání se používá jako materiál pro žhavicí vlákna
v žárovkách a katodách elektronek (včetně elektronových
zdrojů v urychlovačích). Slitiny wolframu se využívají v
metalurgii pro zvýšení tvrdosti, mechanické
a tepelné odolnosti kovů. Pro svou vysokou hustotu se
používá jako účinné radiační stínění
X a gama záření (§1.6, část "Absorbce záření v látkách", pasáž "Stínění záření
gama"), především pro
výrobu kontejnerů a precizních kolimátorů.
Má 5
stabilních isotopů: 180W (0,12%), 182W (26,5%), 183W (14,31%), 184W (30,64%), 186W (28,43%).
Pozn.: U isotopu 180W byla zjištěna velmi slabá radioaktivita - alfa-přeměna
na hafnium 176Hf s obrovsky dlouhým poločasem 1,8.1018roků. Je
podezření, že i ostatní přírodní isotopy wolframu jsou
snad z dlouhodobého hlediska a-radioaktivní (přeměňují se na příslušné
isotopy hafnia), s ještě delšími poločasy. Prověřit to je
velmi obtížné (ve vzorku 1 gramu
wolframu by to představovalo méně než jednu alfa-přeměnu za
rok).
Z radioaktivních isotopů
wolframu zde stojí za zmínku jen jeden:
Wolfram 188W
se s poločasem 69,4 dní přeměňuje b--radioaktivitou
z 99% na základní stav rhenia 188Re, z 1% do několika excitovaných hladin, při
jejichž deexcitaci je emitováno několik fotonů gama
záření, především s energiemi 227 a 290 keV. Isotop 188W se připravuje
neutronovým ozařováním kovového wolframu (obohaceného na
cca 95% isotopem 186W) v jaderném reaktoru dvojitým záchytem neutronu: 186W(n,g)187W(n,g)188W. Slouží jako
mateřský isotop v 188W/188Re generátoru pro získávání
radionuklidu 188Re v nukleární medicíně (viz níže Re-188).
 Rhenium
Re75 je rovněž velmi těžký, tvrdý a obtížně
tavitelný kov, v přírodě zastoupený velmi vzácně (cca 1-5 ng/kg v zemské kůře).
Přírodní rhenium je směsí 37,4% stabilního isotopu 185Re a 62,6%
radioaktivního isotopu 187Re (b-,
poločas 4,33.1010 roků). Praktický význam mají tři radioaktivní
isotopy rhenia:
Rhenium
Re75 je rovněž velmi těžký, tvrdý a obtížně
tavitelný kov, v přírodě zastoupený velmi vzácně (cca 1-5 ng/kg v zemské kůře).
Přírodní rhenium je směsí 37,4% stabilního isotopu 185Re a 62,6%
radioaktivního isotopu 187Re (b-,
poločas 4,33.1010 roků). Praktický význam mají tři radioaktivní
isotopy rhenia:
Rhenium 187Re
je přírodní (primordiální) radionuklid, který se s velmi
dlouhým poločasem 4,33.1010 roků b--radioaktivitou přeměňuje na
základní stav osmia 187Os. Používá se v dlouhodobém radiosotopovém
datování - jaderné geochronologii - pro
určování stáří hornin metodou 187Re/187Os (viz výše "Radiometrické
datování").
Rhenium
186Re
je uměle vyráběný radionuklid, který se s poločasem 3,72
dní přeměňuje rozvětveně v 92,53% beta--radioaktivitou na 186Os a v 7,47% elektronovým
záchytem na 186W. b--přeměny
probíhají ze 71% na základní stav (Ebmax=1070keV) a z 21,5% na excitované hladiny 186Os s energií 137keV
(v malém zlomku procenta i na vyšší
excitované hladiny). Elektronový záchyt
probíhá v 5,8% na základní stav a v 1,7% na excitovaný stav
122keV 186W.
Při deexcitacích jsou emitovány fotony g záření především o
energii 137keV (9,4%) a 122keV (0,6%).
Isotop
186Re se
získává neutronovým ozařováním rhenia (nejlépe obohaceného isotopem 185Re) v jaderném reaktoru pomocí
reakce 185Re(n,g)186Re, nebo v
cyklotronu protonovým ozařováním wolframu (vysoce obohaceného isotopem 186W) v reakci 186W(p,n)186Re.
Rhenium-186
se používá v nukleární medicíně ve formě
fosfonátového komplexu pro paliativní terapii
kostních metastáz (§3.6, část
"Radioisotopová
terapie", pasáž "Radionuklidová
terapie nádorů a metastáz") a
ve formě koloidního sulfitu pro radiační synovektomii
u revmatické artritidy kloubů střední velikosti (zápěstí,
loket, rameno) - §3.6, pasáž "Radionuklidová
synovektomie".

Rozpadové schéma a gama-spektrum rhenia 186Re.
Rhenium 188Re
je rovněž uměle vyráběný radionuklid, který se s
poločasem 16,98 hodin přeměňuje b--radioaktivitou
(Ebmax=2115keV) na 188Os - z 70,6% na
základní stav, z 26% na excitovanou hladinu 155keV, při
jejíž následné deexcitaci je emitováno záření gama
stejné energie. S nízkým zastoupením probíhají
beta-přeměny i do dalších excitovaných stavů 188Os, jejichž radiace
má velmi malou intenzitu.
Isotop
188Re se
získává nejčastěji elucí z 188W/188Re generátoru (byl
zmíněn výše), nebo se připravuje
neutronovým ozařováním rhenia (vysoce obohaceného isotopem 187Re) v jaderném
reaktoru: 187Re(n,g)188Re. Používá se v posledních letech v nukleární
medicíně k obdobným aplikacím jako shora zmíněné
obvyklejší 186Re (výhodou 188Re je snadnější příprava z generátoru, vyšší
měrná aktivita, kratší poločas a vyšší energie
beta-částic).
 Iridium
Iridium 
Těžký ušlechtilý kov iridium Ir77 je
v přírodě zastoupen vzácně (cca 0,001mg/kg v zemské kůře)
svými dvěma stabilními isotopy 191Ir (29,5%) a 193Ir (62,7%). Má vysokou hustotu (22,6g/cm3) a je chemicky velmi
odolné *). Spolu s platinou se používá v metalurgii a řadě
technických aplikací.
*) Ze slitiny platiny a iridia byly
zhotoveny známé etalony metru a kilogramu v Mezinárodním
institutu pro míry a váhy v Sevres u Paříže.
Iridium
192Ir
Těžkým radionuklidem často využívaným jako gama-zářič
je iridium 192Ir. S poločasem T1/2=74,2dne
se rozpadá z 95,1% b--radioaktivitou na excitované hladiny
platiny 192Pt
a z 4,9% elektronovým záchytem na excitované
hladiny osmia 192Os. Při této radioaktivitě 192Ir emituje řadu deexcitačních liní záření
gama v rozmezí 130-1380keV s výraznými píky 296keV
(29%), 308 (30%), 316keV (83%), 468 (48%) a 604+613keV (8,2%).
Několik dalších velmi slabých linií gama vyšších energií
je ve spektru vidět až při velkém zvětšení. Naopak na
začátku spektra jsou patrné linie Ka,b
charakteristického X-záření osmia a platiny 61-78 keV,
vznikající deexcitačními přechody v obalu těchto
dceřinných atomů po elektronovém záchytu elektronu ze slupky
K a po vnitřní konverzi záření gama.
Iridium-192 se používá jako intenzívní zdroj
záření gama středních energií při defektoskopii (§3.3, část "Radiační defektoskopie") a při brachyterapii
(§3.6, část "Brachyradioterapie"). Tyto zářiče o vysoké
aktivitě (GBq-TBq) se připravují jadernou reakcí 191Ir(n,g)192Ir ozařováním
kovového iridia (drátky, plíšky,
pelety) neutrony v jaderném reaktoru.
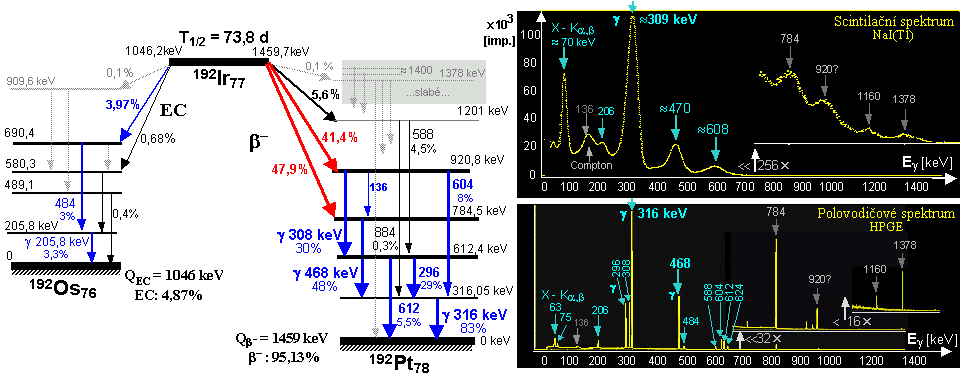
Přeměnové schéma a gama-spektrum iridia
192Ir
 Thalium
Thalium 
Thalium Tl81 je měkký bíle lesklý kov z III.B skupiny, který se
v přírodě vyskytuje jen ve sloučeninách a poměrně vzácně
(cca 0,05-2 mg/kg v zemské kůře). Má dva stabilní isotopy 203Tl (29,5%) a 205Tl (70,5%). Z
radioaktivních isotopů thalia stojí za zmínku přírodní 208Tl (jako rozpadový
produkt thoria-232) a především uměle vyráběné 201Tl:
Thalium
201Tl
je uměle vyráběný radionuklid, který se s poločasem 3dny
přeměňuje elektronovým záchytem EC na 201Hg. Z 21% je to na
základní stav, ve 41% na excitovanou hladinu 167keV a ve 13% na
hladinu 32keV. Při deexcitacích se emitují fotony gama o
energiích 135keV (2,6%), a 167keV (10%). Hlavní složkou
fotonové radiace 201Tl je však charakteristické X-záření
rtuti, vznikající při přechodech elektronů v obalu po
K-záchytu: Ka»68-71keV(73,7%) a
Kb»79-83keV(20,3%),
menší význam má měkké X záření 8-15keV (43%). Jako u
každého EC radionuklidu, i u 201Tl jsou v radiaci významně zastoupeny Augerovy
elektrony, především o energiích 53-58keV (100%),
64-68keV (55%), 75-83keV (7,6%), též nízkoenergetické
elektrony 5-15keV(>50%).
Isotop thalium-201 se připravuje ozařováním
přírodního thalia (příp. obohaceného
isotopem 203Tl) protony v cyklotronu jadernou
reakcí 203Tl(p,3n)201Pb, s následnou
radioaktivní přeměnou 201Pb s poločasem 9,4hod. elektronovým záchytem na
výsledné 201Tl (alternativní možností
přípravy meziproduktu 201Pb je reakce 205Tl(p,5n)201Pb).
Pozn.: Těmito reakcemi se obtížně
získává absolutně čisté 201Tl - v závislosti na energii ozařovacích protonů
často dochází k vyrážení o jednoho více nebo méně
neutronů. Většinou jsou proto v preparátu obsaženy i radionuklidové
nečistoty sousedních isotopů thalia 200,202Tl - viz dolní
část obrázku spektra 201-Tl.
Radionuklid 201Tl ve formě
chloridu se používá v nukleární medicíně pro scintigrafii
perfuze myokardu *), jako analog draslíku, v jednodenním
protokolu - §4.9.4 "SPECT perfuze myokardu". Kationty 201Tl se v buňkách srdečního svalu akumulují podobně
jako ionty draslíku. Po aplikaci radioindikátoru 201Tl se místa
srdečního svalu se sníženým prokrvením na scintigramu
zobrazují jako hypoaktivní oblasti.
*) 201Tl
se široce používalo zvláště v 80.-90. letech. Jeho
nevýhodou je nízká energie dominantního X záření, což
způsobuje horší rozlišení a výraznou absorbci v tkáni;
rovněž značnou radiační zátěž (k níž přispívají i výrazně zastoupené Augerovy
elektrony). Nyní bylo vytlačeno 99mTc značenými
isonitrily, s nimiž se při podstatně nižší radiační
zátěži získají mnohem kvalitnější obrazy. V blízké
budoucnosti však lze možná očekávat částečnou
"renezanci" thalia v souvislosti se zaváděním polovodičových
CZT kamer (§4.2., část "Alternativní fyzikální principy
scintilačních kamer", pasáž
"Polovodičové kamery"), které mají vyšší
citlivost pro fotonové X záření »73keV 201Tl.
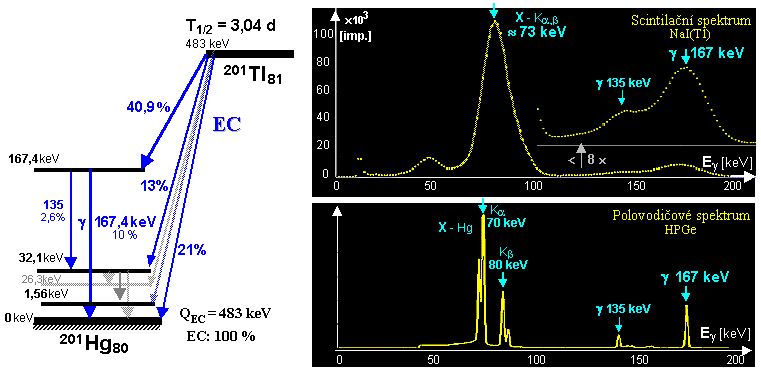
Přeměnové schéma a gama-spektrum thalia 201Tl. Nahoře:
Čisté thalium-201. |
Dole:
201-thalium připravené v cyklotronu jadernou reakcí
[203Tl(p,3n)201Pb; 201Pb(EC,T1/2=9,3hod.)®201Tl]
často obsahuje cca 0,1% radionuklidových
nečistot 200,202Tl.
V gama-spektru takového preparátu jsou kromě
základních píků 201Tl po zvětšení vidět i slabší píky o
vyšších energiích:
367,579,828,1205 keV z kontaninantu 200Tl a píky 439,520 keV z 202Tl. |
 |
 Olovo ,
Bismut
Olovo ,
Bismut 
Těžké kovy olovo a vismut jsou
posledními prvky Mendělejevovy periodické tabulky, které
ještě mají stabilní isotopy (u vismutu se jedná jen o "prakticky"
stabilní isotop, viz níže). Jsou též
koncovými členy radioaktivních rozpadových řad thoria, uranu
a transuranů (viz výše "přírodní
radionuklidy").
 Olovo Pb82 (Plumbum) je měkký nízkotavitelný kov (teplota
tání 327,5°C), který je v přírodě
zastoupen poměrně vzácně (cca 0,05-2 mg/kg v zemské kůře)
*). Většinou se vyskytuje ve sloučeninách jako je sulfid
olovnatý (galenit), síran olovnatý a uhličitan olovnatý.
Klasicky se používá ve výrobě akumulátorů, olovnatého
skla, střeliva. V oblasti radiační fyziky je důležitá jeho
vysoká hustota a absorbční schopnost pro X a gama záření -
využívá se jako účinný stínící materiál
(§1.6, část "Absorbce záření v látkách", pasáž "Stínění
ionizujícího záření").
Olovo Pb82 (Plumbum) je měkký nízkotavitelný kov (teplota
tání 327,5°C), který je v přírodě
zastoupen poměrně vzácně (cca 0,05-2 mg/kg v zemské kůře)
*). Většinou se vyskytuje ve sloučeninách jako je sulfid
olovnatý (galenit), síran olovnatý a uhličitan olovnatý.
Klasicky se používá ve výrobě akumulátorů, olovnatého
skla, střeliva. V oblasti radiační fyziky je důležitá jeho
vysoká hustota a absorbční schopnost pro X a gama záření -
využívá se jako účinný stínící materiál
(§1.6, část "Absorbce záření v látkách", pasáž "Stínění
ionizujícího záření").
*) Obsah olova je však přece jen poněkud
vyšší, než by podle kosmické nukleogeneze
odpovídalo jeho vysokému protonovému číslu. Je to proto, že
isotopy olova jsou konečným produktem radioaktivních
rozpadových řad uranu a thoria (viz obr.1.4.1), takže v průběhu miliard let se obsah olova v
zemské kůře postupně zvyšoval.
Olovo
má 4 stabilní isotopy: 204Pb (9,4%), 206Pb (24,1%), 207Pb (22,1%), 208Pb (15,4%). Z radioaktivních isotopů olova stojí za
zmínku především tři:
Olovo 210Pb
se s poločasem 22,3 roků přeměňuje beta--radioaktivitou na 210Bi - v 20% do
základního stavu, v 80% do excitovaného stavu 46,5keV. Max.
energie záření beta je poměrně nízká, 63keV.
V přírodě neustále vzniká jako jeden z produktů postupné
přeměny 238U v uranové rozpadové řadě (obr....). V uzavřených
materiálech obsahujících uran, jakou jsou horniny, je isotop 210Pb v trvalé
radioaktivní rovnováze s 238U a dceřinnými isotopy jeho přeměny. ....
Olovo 214Pb
se s poločasem 26,9min. přeměňuje beta--radioaktivitou na 214Bi, především na
excitované hladiny 295 a 362 keV, při jejichž deexcitacích je
emitováno záření gama o energiích 352, 195 a 242 keV - viz níže spektrum Radium 226Ra. Podobně jako 214Bi v přírodě neustále vzniká jako jeden z produktů
v uranové rozpadové řadě (obr....). V uzavřených
materiálech obsahujících uran, jakou jsou horniny, je isotop 214Pb v trvalé
radioaktivní rovnováze s 238U a dceřinnými isotopy jeho přeměny. ........
 Bismut Bi83 (Bismuthum), zvaný též vizmut, je lesklý
stříbřitě narůžovělý krystalický nízkotavitelný kov (teplota tání 271°C), v
přírodě vzácně zastoupený (cca 0,2mg/kg v zemské kůře),
jak odpovídá jeho vysokému protonovému číslu. Používá se
pro přípravu nízkotavitelných slitin jako je Woodův kov
(50% Bi, 25% Bb, 12,5% Sn, 12,5% Cd), který má teplotu tavení 60,5°C. Pro svou vysokou
hustotu a absorpční schopnost pro X-záření se Bi někdy
používá v RTG diagnostice ve stínících rouškách pro
radiační ochranu.
Bismut Bi83 (Bismuthum), zvaný též vizmut, je lesklý
stříbřitě narůžovělý krystalický nízkotavitelný kov (teplota tání 271°C), v
přírodě vzácně zastoupený (cca 0,2mg/kg v zemské kůře),
jak odpovídá jeho vysokému protonovému číslu. Používá se
pro přípravu nízkotavitelných slitin jako je Woodův kov
(50% Bi, 25% Bb, 12,5% Sn, 12,5% Cd), který má teplotu tavení 60,5°C. Pro svou vysokou
hustotu a absorpční schopnost pro X-záření se Bi někdy
používá v RTG diagnostice ve stínících rouškách pro
radiační ochranu.
Přírodní
vizmut je tvořen isotopem 209Bi, který byl donedávna považován
za stabilní. V r.2003 však bylo zjištěno,
že je tento isotop slabě radioaktivní - s
nesmírně dlouhým poločasem 1,9.1019let
podléhá alfa-radioaktivitě. Z praktického hlediska se však
přírodní vizut jeví jako neradioaktivní (300kg bismutu by mělo aktivitu 1Bq), s radiací hluboko pod přírodním pozadím. Z
(opravdu) radioaktivních isotopů bismutu jsou částečně
důležité tři přírodní a dva umělé radionuklidy:
Bismut 212Bi
se v přírodě vyskytuje jako jeden z produktů thoriové
rozpadové řady (....). S poločasem 60,5min. se z 36%
přeměňuje a-radioaktivitou na 208Tl a z 64% b--radioaktivitou
na 212Po.
...........
.....................
Bismut 213Bi
se z 97,8% přeměňuje b--radioaktivitou
na 213Po a
z 2,2% a-radioaktivitou
na 209Tl
..........
Isotopy 214,213Bi se zkušebně používají v nukleární medicíně
pro radioimunoterapii (§3.6, část "Radioisotopová
terapie", pasáž "Radioimunoterapie").
Bismut 214Bi
je jedním z pomíjivých, avšak důležitých produktů
uranové rozpadové řady (...). S poměrně krátkým poločasem
19,8 minut se přeměňuje složitým rozpadovým schématem
především beta--radioaktivitou
na řadu excitovaných hladin a na základní stav polonia 214Po, v nepatrné
míře (0,021%) též alfa-radioaktivitou na excitované
hladiny 210Tl.
Při deexcitacích (především hladin 214Po) je emitována řada energií záření gama, z nichž
významné zastoupení mají zvláště 609,3 keV (45,5%), 665
(1,5%), 768 (4,5%), 1120..... - viz
obrázek Ra-226 vlevo.
Výrazné
gama-linie 214Bi můžeme pozorovat u uranu a radia (pokud je v rovnováze se svými dceřinnými nuklidy -
viz níže Radium 226Ra) a též ve většině
přírodních vzorků, kam se tento radionuklid dostává s
plynným radonem (viz např. výše
uvedený obr.1.4.2).
 Thorium ,
Uran , Radium , Aktinium , Radon
Thorium ,
Uran , Radium , Aktinium , Radon 
Z těžkých jader uranové
skupiny, které jsou všechny a-radioaktivní, jsou důležité zvláště
následující přírodní (primární)
radionuklidy thorium a uran:
 Thorium Th90 je stříbřitě bílý kov, který je v minerálních
sloučeninách poměrně hojně zastoupen v zemské kůře (9,6
mg/kg). Nemá žádný stabilní isotop, v pozemské přírodě
se vyskytuje především slabě radioaktivní thorium-232:
Thorium Th90 je stříbřitě bílý kov, který je v minerálních
sloučeninách poměrně hojně zastoupen v zemské kůře (9,6
mg/kg). Nemá žádný stabilní isotop, v pozemské přírodě
se vyskytuje především slabě radioaktivní thorium-232:
Thorium 232Th
Thorium 232Th90 patří k
nejrozšířenějším přírodním radionuklidům
obsaženým v horninách zemské kůry (spolu
s 40K), jeho obsah je cca 9mg/kg. S velmi dlouhým poločasem T1/2=14,02.109 let
se rozpadá alfa-radioaktivitou na radium 228Ra a dále pak celou
rozpadovou řadou podle levé části obr.1.4.1. Zatím nemá přímé radiační využití, v budoucnu
ale může být potenciálním štěpným materiálem v
množivých jaderných reaktorech s thorium-uranovým cyklem - §1.3, část "Rychlé množivé
reaktory FBR". Vzhledem k nízké měrné aktivitě a nemožnosti
použití pro přímé řetězové štěpení můžeme z hlediska
jaderné fyziky a radiační ochrany thorium-232 považovat za
téměř neradioaktivní materiál, s nepatrným rizikem.
Thorium
může být použito jako materiál pro účinné stínění
ionizujícího záření. Dále se 232Th v technické praxi někdy používá jako příměs
do elektrod výbojek, kde ionizace plynové
náplně alfa-částicemi usnadňuje zapálení elektrického
výboje při nižším napětí (§3.7,
pasáž "Radioaktivita ve výbojkách"). Další využití thoria
(230-Th) je v uran-thoriovém radiometrickém datování (viz výše "Radiometrické datování").
Thorium
227Th
je uměle vyráběný radioisotop pro použití v biologicky
cílené radionuklidové terapii. S poločasem T1/2=18,7
dne se alfa-radioaktivitou přeměňuje
na radium 223Ra - ve 25% do základního stavu, 24%
na hladinu 61,5keV, 20% na 286keV, 5% na 329keV, v 8% na 334kev,
s nižším zastoupením na řadu dalších excitovaných stavů.
Při deexcitaci se emituje řada fotonů gama, především
energií 50keV (8%), 236keV (12,4%) a 256keV (7%), slabší jsou
300keV (2,3%) a 330keV (2,7%). Energie alfa-částic se pohybují
v rozmezí 5,7-6 MeV, podle excitovaných hladin. Dceřinné 223Ra se pak opět a-radioaktivitou s
poločasem 11,4 dne přeměňuje na radon-219 a dále celým rozpadovým
řetězcem krátkodobých isotopů až na stabilní
olovo-207 (srov. níže obrázek v pasáži
"Radium 223Ra"), za emise mnoha dalších
energií částic alfa, elektromů beta a fotonů gama.
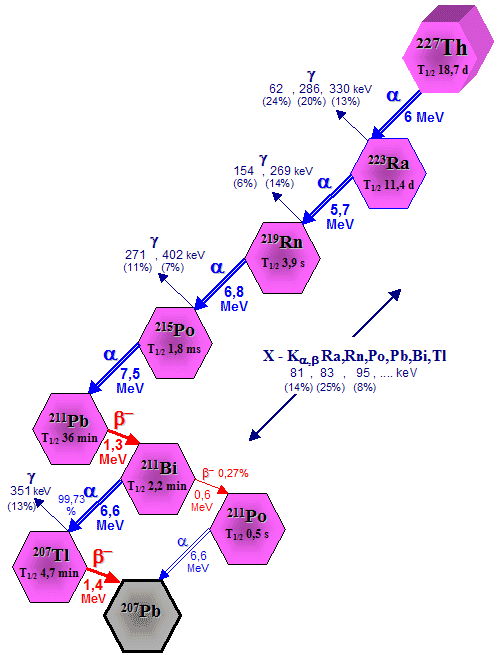 |
Jak
je typické pro těžké nuklidy uranové skupiny
(a vyšší), i 227Th se přeměňuje celou rozpadovou
řadou:
227Th(18,7d.; a) ® 223Ra(11,4d.; a) ® 219Rn(4s.; a) ® 215Po(1,8ms.; a) ® 211Pb(36,1min.; b-)
® 211Bi(2,2min.; a) ® 207Tl(4,8min.; b-)
® 207Pb(stab.).
Při první přeměně 227Th (na radium 223Ra) je emitováno
záření alfa o energiích 5,7-6 MeV a záření
gama o energiích především 50, 236 a 256 keV.
Při radioaktivitě dceřinných
nuklidů rozpadové řady je pak emitována řada
dalších energií částic alfa, beta a fotonů
gama, především: z 223Ra je to a
5,6 a 5,7MeV a záření gama o energiích
především 154 a 269 keV; z 219Rn je to a
6,4 a 6,8 MeV a g 271 a 402
keV; z 215Po je to a
7,4MeV; z 211Pb je to beta 540 a
1372 keV a slabé g 404 a 832
keV; z 211Bi je to a
6,3 a 6,6 MeV a g 351keV; z 207Tl se emituje beta max.
energie 1423keV a slabé gama 898keV.
Vedlejší větev 211Bi(b-)®211Po
vzhledem ke svému nízkému zastoupení (0,27%)
nemá žádný praktický význam.
Rozpadový řetězec 227-Th funguje jako
"in vivo radionuklidový generátor"
- viz výše "In vivo generátory".
Zjednodušené přeměnové
schéma 227Th na 223Ra je nakresleno
níže v levé části obrázku.
Změřené spektrum
záření gama emitovaného všemi nuklidy z
celé rozpadové řady 227-Th je zobrazeno níže
v pravé části obrázku.ę |
|
 |
Přeměnové
schéma thoria 227Th (první přeměna na
radium-223) a celkové
gama-spektrum 227Th a jeho rozpadových produktů.
Spektrum bylo měřeno s hermeticky
uzavřeným preparátem, z něhož nemohl uniknout
plynný radon 219Rn. Ve spektru jsou proto obsaženy gama-linie i
všech dceřinných radionuklidů rozpadové řady, s
nimiž je 227Th v radioaktivní rovnováze. Linie gama
pocházející z přeměny 227-Th na 213-Ra jsou ve
spektru uvedeny bez označení (jen s hodnotou energie),
u fotopíků ze sekundárních přeměn v rozpadové
řadě jsou uvedeny příslušné radionuklidy, z nichž
pocházejí (především 223Ra, 219Rn, 211Bi, 211Pb a 207Tl). |
Při jedné úplné
radioaktivní přeměně jádra 227Th v celé rozpadové řadě až na
stabilní 207Pb se uvolní celková jaderná energie Q = 36,132 MeV, která je z asi 95% odnášena pěti
alfa-částicemi, ze 3% elektrony beta+neutriny a z asi
1% fotony *) gama a X-záření.
*) Toto zdánlivě malé procentuální
zastoupení fotonového záření je důsledkem energetického
přepočtu vzhledem k vysoenergetickým a-částicím. Absolutní
počet emitovaných fotonů gama a X je ve skutečnosti poměrně
vysoký, pro energie v rozmezí 80-400keV představuje
cca 96%! Nejvíce zastoupené X a gama-energie jsou: X 81(14%),
83(25%) a 95keV(8%), gama 154(5,8%), 269(14%), 351(13%) a
401keV(7%).
U thoria 227Th a dceřinných produktů rozpadové řady je
využíváno především emitované alfa-záření
o energiích 5,4-7,4 MeV (celkem
5 alfa-částic/1přeměnu 227Th) v nukleární
medicíně pro biologicky cílenou radionuklidovou terapii.
Záření gama
227Th a
jeho dceřinných nuklidů se při terapii prakticky
neuplatňuje, ale může být využito pro gamagrafické
monitorování distribuce radiofarmaka v organismu. Emise gama záření
umožňuje při terapii současné scintigrafické
zobrazení tkání a orgánů, kam terapeutický
preparát pronikl. Na těchto scintigrafických obrazech můžeme
posuzovat (vizuálně, příp. i
kvantitativně) míru žádoucího
vychytávání radiofarmaka v nádorových ložiscích a
nežádoucí akumulace ve zdravých tkáních a kritických
orgánech - provádět monitorování průběhu
radioisotopové terapie.
Chemické vlastnosti thoria (oxidační
stav +4) umožňují, s pomocí
makrocyklického ligandu typu DOTA, chelatační navázání 227Th k monoklonálním
protilátkám za vzniku radioimunokonjugátů,
které se cíleně vychytávají v nádorových buňkách (struktura a vlastnosti monoklonálních protilátek
jsou podrobněji rozebírány v §3.6, část "Cílená biologická léčba - monoklonální protilátky"). Vysokoenergetické a-částice,
emitované při radioaktivních přeměnách, pak mohou účinně
ničit tyto nádorové buňky. Ve stadiu
laboratorního zkoušení je cílená imunoterapie s použitím alfa-značených
monoklonálních protilátek thoriem: u lymfomů 227Th - rituximabu nebo
anti CD22, u akutní myeloidní leukemie 227Th - konjugátu CD33 lintuzumab.
Určitým problémem může být uvolňování
dceřinného radia-223 z chemické vazby v radioimunokonjugátu v
důsledku zpětného odrazu jádra při emisi
alfa-částice (§1.2, pasáž "Zpětný odraz jader") a rozdílnosti chemických
vlastností radia (oxidační číslo 2). Pokud dceřinné radium
během své přeměny (T1/2 =11,4 dne) uniká z cílové tkáně, účinnost terapie se tím snižuje
o 4 energetické alfa-částice z rozpadové řady radia-223.
Uvolněné 223Ra se pak může vychytávat v jiných tkáních (např. v kostech) a způsobovat
tam nežádoucí radiační zátěž.
Příprava:
Isotop 227Th
se uměle připravuje ozařováním radia-226 neutrony za vzniku
radia-227: 226Ra(n,g)227Ra, s následnou přeměnou beta--radioaktivitou 227Ra(b-,T1/2=41min.)® 227Ac na aktinium-227, které se s poločasem 21,8let
přeměňuje na výsledné thorium-227: 227Ac(b-,T1/2=21,8r.)® 227Th. Vzhledem k dlouhému poločasu aktinia-227 lze 227Th průběžně
získávat elucí z 227Ac/227Th generátoru.
 Uran U92 je
velmi těžký (19g/cm3) kovový prvek stříbrobílé
barvy ze skupiny aktiniodů. Na vzduchu vlivem oxidace získává
tmavě šedé zabarvení. Byl izolován v r.1841 a název získal
podle tehdy nově objevené planety Uran. Používal se
k barvení skla. V r.1896 H.Becquerel u minerálů obsahujících
uran zjistil dříve neznámé pronikavé záření - objevil
radioaktivitu (§1.2 "Radioaktivita"). Uran nemá žádný
stabilní isotop, všech 28 známých isotopů je radioaktivních.
Přírodní kovový prvek uran U92 sestává především z isotopů 235U (0,7204%) a 238U (99,2742%), což jsou důležité přírodní
primordiální radionuklidy; dále je přítomno stopové
množství 234U (0,0054%), který vzniká jako sekundární
meziprodukt rozpadové řady 238U.
Uran U92 je
velmi těžký (19g/cm3) kovový prvek stříbrobílé
barvy ze skupiny aktiniodů. Na vzduchu vlivem oxidace získává
tmavě šedé zabarvení. Byl izolován v r.1841 a název získal
podle tehdy nově objevené planety Uran. Používal se
k barvení skla. V r.1896 H.Becquerel u minerálů obsahujících
uran zjistil dříve neznámé pronikavé záření - objevil
radioaktivitu (§1.2 "Radioaktivita"). Uran nemá žádný
stabilní isotop, všech 28 známých isotopů je radioaktivních.
Přírodní kovový prvek uran U92 sestává především z isotopů 235U (0,7204%) a 238U (99,2742%), což jsou důležité přírodní
primordiální radionuklidy; dále je přítomno stopové
množství 234U (0,0054%), který vzniká jako sekundární
meziprodukt rozpadové řady 238U.
Uran 235U se s dlouhým poločasem T1/2=7,04.108
let rozpadá alfa-radioaktivitou
na thorium 231Th a dále pak celou rozpadovou řadou podle
prostřední části obr.1.4.1. Pohlcením neutronu
se jádro 235U rozštěpí na dvě lehčí jádra.
Uran-235 je základním štěpným materiálem v
jaderných reaktorech, při jehož štěpení se získává
velké množství energie v jaderných elektrárnách; jaderné
reaktory slouží též jako mohutný zdroj neutronů
pro řadu aplikací jaderné fyziky a chemie. Podrobnosti viz §1.3 "Jaderné reakce",
část "Štěpení
atomových jader".
Uran 238U se s velmi dlouhým poločasem T1/2=4,47.109
let rozpadá alfa-radioaktivitou
na thorium 234Th a dále pak celou rozpadovou řadou podle pravé
části obr.1.4.1. Díky svému delšímu poločasu je 238U
nejrozšířenějším druhem uranu v přírodě. Lze jej
rovněž využít jako štěpný materiál, avšak ne přímo,
ale přes plutonium, které v jaderném reaktoru vzniká
z 238U
pohlcením neutronu (§1.3, část "Rychlé množivé
reaktory FBR"). Uran-238 (jakožto tzv. "ochuzený
uran") má jen poměrně nízkou
radioaktivitu (viz tabulku v pasáži
"Vztah poločasu a aktivity"
§1.2 "Radioaktivita") a někdy se používá
jako účinný stínící materiál pro
vysokoenergetické záření gama.
Při vlastní
alfa-radioaktivitě uranu vzniká jen poměrně málo záření
gama. V g-spektru můžeme z uranu vidět jen nepříliš
výrazné linie 185keV a 205keV z přeměny 235U na metastabilní hladiny 231Th. Většina gama-radiace uranu pochází z
dceřinných radionuklidů rozpadové řady, především z
thoria 234Th
(63keV, 93keV), dále z radia-226 (185keV) a především z olova
214Pb a
bismutu 214Bi
(214, 295, 352, 609 keV a řada dalších...).
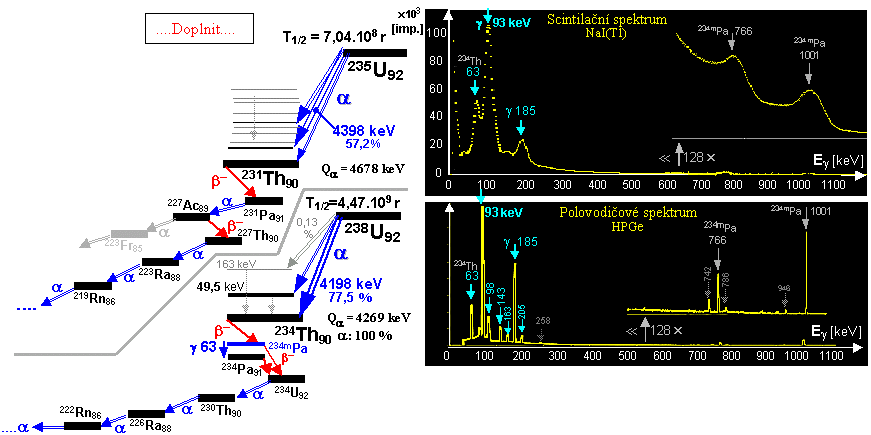
Zjednodušené přeměnové schéma uranu 235U a 238U a gama-spektrum přírodního uranu a některých jeho
rozpadových produktů.
Gama-spektrum bylo měřeno ze vzorku
volného tenkého plechu kovového uranu tloušťky 0,3mm. Série
dceřinných radionuklidů v rozpadové řadě zde byla
přerušena u radonu 219,222Rn, který vzhledem ke svému plynnému skupenství
plynule uniká ze vzorku. Proto se ve spektru nevyskytují
gama-linie dalších radionuklidů rozpadové řady, např. 214Pb a 214Bi, které můžeme
vidět třebas ve spektru vzorku zapouzdřeného radia (viz
níže "Ra-226.gif"), nebo ve
vzorcích přírodního prostředí (např. "NaturalRadioactivity.gif").
Uran 234U se s poločasem T1/2=245,5 tisíc let rozpadá alfa-radioaktivitou
na thorium 230Th a pak 238-uranovou rozpadovou řadou na olovo-206.
Vzniká v malém množství jako součást rozpadové řady 238U. Nemá praktický
význam, není štěpným materiálem.
Posledním poněkud technicky významným isotopem
uranu je uměle vyráběný :
Uran 233U, který se s poločasem T1/2=159,2 tisíc let rozpadá alfa-radioaktivitou
na thorium 229Th (a pak neptuniovou
rozpadovou řadou na Bi-209 - je zobrazeno níže v pasáži
"Aktinium
225Ac", na
obrázku vlevo nahoře). Uran-233 vzniká z
thoria 232Th
pohlcením neutronu v reakci 232Th90(n,g)233Th90 ®(b-;12min)® 233Pa91 ®(b-;27dnů)® 233U92. Uran 233U může potenciálně sloužit jako štěpný
materiál v reaktorech s thoriovým palivovým cyklem
(Rychlé množivé
reaktory FBR).
Rozpadovými
produkty thoria a uranu je řada dalších radioisotopů (tvoří tzv. rozpadové řady popsané
výše, obr.1.4.1), z nichž nejdůležitější je
radium :
 Radium Ra88 je důležitý radioaktivní prvek, spojený s
historií objevování radioaktivity na počátku 20.století.
Radium je stříbrobílý, těžký a značně reaktivní kov ze
skupiny alkalických zemin. Všechny jeho isotoy jsou radioaktivní.
V přírodě se ve stopovém množství vyskytují čtyři
isotopy radia: 223Ra (T1/2=11,4
d.), 224Ra
(T1/2=3,64 d.), 226Ra (T1/2=1602 let), 228Ra (T1/2=5,75 let). Pocházejí z
rozpadových řad uranu a thoria. Isotopy radia se
alfa-radioaktivitou přeměňují na příslušné isotopy
plynného radonu a dále celou rozpadovou řadou o 5-6
členech na stabilní isotop olova (výjimkou
je 228Ra v
thoriové řadě, které se přeměňuje 10-člennou řadou,
jejíž součástí je radium-224 a radon-220).
Radium Ra88 je důležitý radioaktivní prvek, spojený s
historií objevování radioaktivity na počátku 20.století.
Radium je stříbrobílý, těžký a značně reaktivní kov ze
skupiny alkalických zemin. Všechny jeho isotoy jsou radioaktivní.
V přírodě se ve stopovém množství vyskytují čtyři
isotopy radia: 223Ra (T1/2=11,4
d.), 224Ra
(T1/2=3,64 d.), 226Ra (T1/2=1602 let), 228Ra (T1/2=5,75 let). Pocházejí z
rozpadových řad uranu a thoria. Isotopy radia se
alfa-radioaktivitou přeměňují na příslušné isotopy
plynného radonu a dále celou rozpadovou řadou o 5-6
členech na stabilní isotop olova (výjimkou
je 228Ra v
thoriové řadě, které se přeměňuje 10-člennou řadou,
jejíž součástí je radium-224 a radon-220).
Radium
226Ra
Nejdůležitějším isotopem radia je 226Ra, objevené a izolované z uranové
rudy v r.1898 M. a P. Curieovými. 1 gram 226Ra, izolovaný heroickým úsilím paní M.Curieové a
jejich spolupracovníků, dlouhou dobu sloužil jako etalon
dřívější jednotky aktivity 1 Curie (1Ci).
226-radium se s poločasem T1/2=1602
let přeměňuje alfa-radioaktivitou na
radon 222Rn
(a pak celou rozpadovou řadou až na
stabilní olovo 206Pb). V 94,4% probíhá a-přeměna do
základního stavu radonu, v 5,5% do excitovaného stavu 186keV,
slabě zastoupeny jsou další tři vyšší excitované hladiny.
Samotné 226Ra je smíšeným a+g zářičem (Ea=4,78MeV,
Eg=186keV), avšak ve skutečnosti
je v rovnováze se svými dceřinnými isotopy v rozpadové
řadě. Ve spektru záření gama 226Ra sice vidíme vlastní pík 186keV, avšak daleko
výraznější jsou linie dceřinných produktů 214Pb
a 214Bi (o vyšších
energiích: 295, 352, 609, 768, 1120, 1238, 1378, 1764, 2204,
2448 keV). Radiofory 226Ra se dříve používaly v brachyradioterapii
(§3.6, část "Brachyradioterapie"), nyní jsou vytlačeny
především iridiem-192 (viz
výše "Iridium").

Přeměnové schéma radia 226Ra a gama-spektrum 226Ra a jeho rozpadových produktů. Ve výřezu v levé
části obrázku jsou zjednodušená rozpadová schémata
důležitých radionuklidů 214Pb a 214Bi z rozpadové řady radia-226.
Spektrum bylo měřeno se zapouzdřeným
etalonem 226Ra, z něhož nemohl uniknout plynný radon 222Rn, takže 226Ra je v
radioaktivní rovnováze se svými dceřinnými produkty. Ve
spektru jsou proto (na rozdíl od výše uvedeného spektra
uranu) zobrazeny gama-linie všech dceřinných radionuklidů
rozpadové řady, především 214Pb a 214Bi.
Radium
223Ra
je na rozdíl od předchozích přírodních nuklidů uměle
vyráběným radioisotopem pro účely radionuklidové
terapie v nukleární medicíně (v
přírodě se isotop 223Ra vyskytuje jen v nepatrném množství jako jeden z
produktů přeměn uranu 235U v uran-aktiniové rozpadové řadě - obr.1.4.1). 223-radium se přeměňuje alfa-radioaktivitou
*) s poločasem 11,43 dní na radon 219Rn (a dále pak rozpadovou řadou až na stabilní olovo 207Pb, viz níže). Jen z 1% probíhá přeměna na základní stav, ve
většině případů je to řada excitovaných stavů 219Rn. Nejvíce
zastoupené jsou přeměny na hladiny o energiích 127keV (9,5%),
154keV (52,5%), 269keV (24,2%), 338keV (9,2%), při jejichž
deexcitacích je emitováno záření gama (největší
zastoupení zde mají energie 154 a 269keV, slabší je 324keV). Záření alfa z přeměny 223Ra má energie v rozmezí 5,5-5,7MeV. Další energie
alfa, beta a gama jsou emitovány z dceřinných produktů
rozpadové řady, viz níže - srov. též
výše obrázek v pasáži "Thorium 227Th".
*) Drobná zajímavost:
223Ra byl první isotop, u kterého byla v r.1984 objevena
nová radioaktivní přeměna s emisí částic těžších
než alfa-částice - "uhlíková radioaktivita"
s emisí jádra 14C: 223Ra ® 209Pb + 14C (viz §1.2, část "Exotické druhy radioaktivity",
pasáž "Radioaktivita vyšší než a-héliová").
Tento proces je však velmi slabý, na hranicích měřitelnosti,
poměr počtu emisí 14C a emisí alfa (t.j. 4He) je 6,4.10-10.
Příprava:
Isotop 223Ra
se uměle připravuje ozařováním radia-226 neutrony
za vzniku radia-227: 226Ra(n,g)227Ra, s následnou přeměnou beta--radioaktivitou 227Ra(b-,T1/2=41min.)®227Ac na aktinium-227, které se s poločasem 21,8let přes
thorium-227 přeměňuje na výsledné radium-223: 227Ac(b-,T1/2=21,8r.)®227Th(a,T1/2=18,7d.)®223Ra. Vzhledem k dlouhému poločasu aktinia-227 lze 223Ra průběžně
získávat elucí z 227Ac/223Ra generátoru (selektivní
eluce se provádí roztokem cca 0,1mol. HCl nebo HNO3).
 |
Jak
je typické pro těžké nuklidy uranové skupiny
(a vyšší), i 223Ra se přeměňuje celou rozpadovou
řadou:
223Ra(11,4d.; a) ® 219Rn(4s.; a) ® 215Po(1,8ms.; a) ® 211Pb(36,1min.; b-)
® 211Bi(2,2min.; a) ® 207Tl(4,8min.; b-)
® 207Pb(stab.).
Při první přeměně 223Ra (na radon 219Rn) je emitováno
záření alfa o energiích 5,6 a 5,7MeV a
záření gama o energiích především 154 a
269 keV.
Při radioaktivitě dceřinných
nuklidů rozpadové řady je pak emitována řada
dalších energií částic alfa, beta a fotonů
gama, především: z 219Rn je to a
6,4 a 6,8 MeV a g 271 a 402
keV; z 215Po je to a
7,4MeV; z 211Pb je to beta 540 a
1372 keV a slabé g 404 a 832
keV; z 211Bi je to a
6,3 a 6,6 MeV a g 351keV; z 207Tl se emituje beta max.
energie 1423keV a slabé gama 898keV.
Vedlejší větev 211Bi(b-)®211Po
vzhledem ke svému nízkému zastoupení (0,27%)
nemá žádný praktický význam.
Rozpadový řetězec 223-Ra funguje jako
"in vivo radionuklidový generátor"
- viz výše "In vivo generátory".
Změřené spektrum záření gama
emitovaného všemi nuklidy z celé rozpadové
řady 223-Ra je zobrazeno níže v pravé části
obrázku.ę |
|
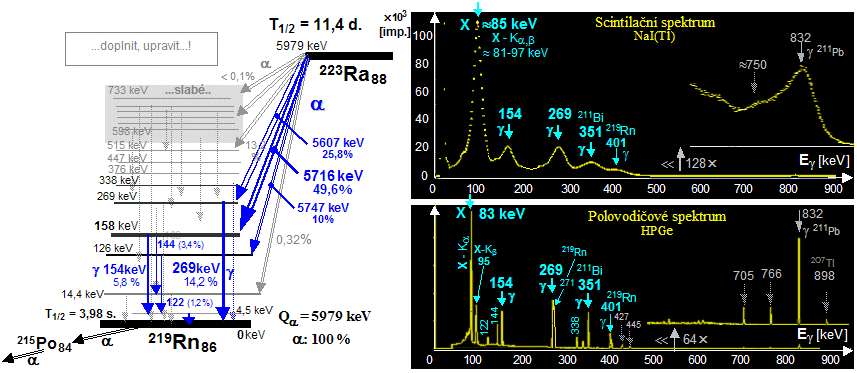 |
Přeměnové
schéma radia 223Ra (první přeměna na
radon-219) a celkové gama-spektrum
223Ra
a jeho rozpadových produktů.
Spektrum bylo měřeno s hermeticky
uzavřeným preparátem, z něhož nemohl uniknout
plynný radon 219Rn. Ve spektru jsou proto obsaženy gama-linie i
všech dceřinných radionuklidů rozpadové řady, s
nimiž je 223Ra v radioaktivní rovnováze. Linie gama
pocházející z přeměny 223-Ra na 219-Rn jsou ve
spektru uvedeny bez označení (jen s hodnotou energie),
u fotopíků ze sekundárních přeměn v rozpadové
řadě jsou uvedeny příslušné radionuklidy, z nichž
pocházejí (především 219Rn, 211Bi, 211Pb a 207Tl). |
Při jedné úplné
radioaktivní přeměně jádra 223Ra v celé rozpadové řadě až na
stabilní 207Pb se uvolní celková jaderná energie Q = 29,986 MeV, která je z asi 95% odnášena čtyřmi
alfa-částicemi, ze 3% elektrony beta+neutriny a z asi
1% *) fotony gama a X-záření.
*) Toto zdánlivě malé procentuální zastoupení fotonového
záření je důsledkem energetického přepočtu vzhledem k
vysoenergetickým a-částicím. Absolutní počet emitovaných fotonů
gama a X je ve skutečnosti poměrně vysoký,
pro energie v rozmezí 80-400keV představuje cca 96%! Nejvíce
zastoupené X a gama-energie jsou: X 81(14%), 83(25%) a
95keV(8%), gama 154(5,8%), 269(14%), 351(13%) a 401keV(7%).
U radia 223Ra a dceřinných
produktů rozpadové řady je využíváno především
emitované alfa-záření o energiích 5,4-7,4
MeV (celkem 4
alfa-částice/1přeměnu 223Ra) v nukleární
medicíně pro radioisotovou terapii kostních metastáz,
které se často vyskytují u karcinou prsu a prostaty (§3.6, část "Radioisotopová terapie", pasáž "Radionuklidová
terapie nádorů a metastáz"). Elektrony beta mají jen zanedbatelný význam. Radium
má chemické a biologické chování podobné vápníku, takže
se 223Ra
akumuluje v metabolicky aktivní kostní tkáni v krystalcích
hydroxyapatitu. Vychytává se proto v kostních metastázách se
zvýšenou osteoblastickou aktivitou, kde
vykazuje bohužel jen paliativní účinek v
osteoblastickém lemu kolem metastázy - do vlastní nádorové
tkáně toto radiofarmakum a alfa-částice prakticky neproniknou
(viz níže "Kritická
poznámka: 223Ra není vhodný terapeutický radionuklid !").
Způsob, jakým se
mateřské 223Ra po své akumulaci v cílové tkáni přeměňuje na
řadu krátkodobějších radionuklidů, je typickým příkladem
výše zmíněného in vivo radionuklidového
generátoru.
Záření gama 223Ra a jeho
dceřinných nuklidů se při terapii prakticky neuplatňuje, ale
může být využito pro gamagrafické monitorování
distribuce radiofarmaka v organismu. Pozitivní význam poměrně
značného zastoupení záření gama spočívá rovněž v
možnosti snadného měření aktivity
preparátů 223Ra v běžných měřičích aktivity s ionizační
komorou (§2.3 "Ionizační komory"), za použití
příslušné kalibrace gama-konstanty.
Kritická
poznámka: 223Ra není vhodný
terapeutický radionuklid !
Základní podmínkou použitelnosti daného radionuklidu v
nukleární medicíně je možnost chemického
navázání jeho atomu na vhodnou biochemicky cílenou
molekulu, která zajistí "dopravu" radionuklidu do
cílových tkání a orgánů za účelem diagnostického
zobrazení nebo terapeutického účinku. Toto chemické
navázání může být přímé (u jednoduchých
molekul) nebo prostřednictvím chelatačních činidel
(tak je tomu především u moklonálních protilátek).
Dostatečně pevná vazba, přímá nebo s chelatační látkou,
závisí především na oxidačním čísle
(mocenství) atomů daného prvku.
Prvek radium, a tedy i 223Ra, má oxidační číslo 2 a nejsou pro něj
k dispozici vhodná chelatační činidla. Takže radium není
perspektivní pro vytváření 223Ra-radioimunokonjugátů! Naopak, atomy
radionuklidů thorium 227Th nebo aktinium 225Ac, s oxidačním číslem 4, jsou
schopny tvořit vysoce stabilní komplexy s chelátory a jsou
proto vhodné pro biologicky cílenou
radionuklidovou terapii.
Přes tyto skutečnosti byl s radiem 223Ra vyvinut
terapeutický preparát chlorid 223RaCl2 Alpharadin (fy Nanovector jej vyvinula s
maximální pečlivostí...), později přejmenovaný firmou
Bayer na Xofigo, pro paliativní terapii kostních
metastáz. Firemní reklama hovořila i o kurativním účinku,
což se nepotvrdilo. A paliativní účinek se nakonec ukázal
prakticky stejný jako u mnoho let používaných preparátů s
radionuklidy stronciem 89Sr (Metastron) či samariem 153Sm (s fosfátovým ligandem EDTMP),
které jsou několikanásobně levnější a odzkoušené.
Použití 223Ra pro terapii kostních metastáz u ca prostaty je
nyní již nesmyslné vzhledem k tomu, že existují účinné
monoklonální protilátky anti-PSMA značené 177Lu nebo 225Ac, které jsou
schopny kurativně působit nejen na kostní
metastázy, ale i na nádorová ložiska ve všech ostatních
tkáních a orgánech, i v pokročilém stádiu.
Prosazení radia 223Ra bylo chybné již od samého
začátku - takto jsme to na našem pracovišti reflektovali. Až
toto nahlédne většina kolegů z oboru nukleární medicíny,
bude 223Ra
pravděpodobně definitivně opuštěno...
 Aktinium Ac89 je měkký stříbřitě bílý kovový prvek, silně radioaktivní,
nemá žádný stabilní isotop. V přírodě se ve stopovém
množství vyskytují dva isotopy aktinia: 227Ac (T1/2=21,77
let) a 228Ac
(T1/2=6,15 hod.),
jako součást rozpadových řad uranu-235 a thoria-232.
Rozpadají se radioaktivitou alfa (nebo větvenou beta-alfa) na
příslušné isotopy francia (nebo thoria) a dále rozpadovou
řadou o 4-6 členech na stabilní isotopy olova. Název prvku
vznikl právě z jeho silné radioaktivity (řec.
aktis = paprsek). V jaderné
fyzice jsou známé isotopy aktinia 206-234Ac. Nejdůležitější z nich - pro radionuklidovou
terapii v nukleární medicíně - je uměle vyráběný isotop
aktinia-225 :
Aktinium Ac89 je měkký stříbřitě bílý kovový prvek, silně radioaktivní,
nemá žádný stabilní isotop. V přírodě se ve stopovém
množství vyskytují dva isotopy aktinia: 227Ac (T1/2=21,77
let) a 228Ac
(T1/2=6,15 hod.),
jako součást rozpadových řad uranu-235 a thoria-232.
Rozpadají se radioaktivitou alfa (nebo větvenou beta-alfa) na
příslušné isotopy francia (nebo thoria) a dále rozpadovou
řadou o 4-6 členech na stabilní isotopy olova. Název prvku
vznikl právě z jeho silné radioaktivity (řec.
aktis = paprsek). V jaderné
fyzice jsou známé isotopy aktinia 206-234Ac. Nejdůležitější z nich - pro radionuklidovou
terapii v nukleární medicíně - je uměle vyráběný isotop
aktinia-225 :
Aktinium
225Ac
S poločasem 10 dní se přeměňuje alfa-radioaktivitou
na francium 221Fr - v 50% na základní stav (emise Ea=5,83MeV), v
ostatních případech na řadu excitovaných stavů francia (při deexcitacích je emitováno několik desítek gama
fotonů, od nízkých energií cca 10keV, slabší píky jsou až
do 800keV). Další radioaktivní přeměny
221Fr pak
pokračují celou rozpadovou řadou až na
bismut 209Bi
- je součástí neptuniové řady :
 |
Aktinium
225Ac se přeměňuje celou rozpadovou
řadou 6 hlavních dceřinných jader :
(225Ac(10d.; a) ® 221Fr(4,8m.; a) ® 217At(32ms.; a) ® 213Bi(46m.; b-)
® 213Po(4ms.;
a) ® 209Pb(3,3h.; b-)
® 209Bi(stab.)) - obrázek vlevo.
Pozn.: 209Bi
zde můžeme považovat za stabilní (a ,
T1/2 » 2.1019let).
Při
první přeměně 225Ac (na franium 221Fr) je emitováno
záření alfa o energii 5,8 MeV a slabé
záření gama 63, 100, 110, 150 keV, nepatrné
zastoupení mají vyšší energie 250-760keV.
Při radioaktivitě dceřinných
nuklidů rozpadové řady je pak emitována řada
dalších energií částic alfa, beta a fotonů
gama: z 221Fr je to a
6,3 MeV a záření gama o energii především
218 keV; z 217At je to a
7,06 MeV ; z 213Bi je to alfa 5,8MeV,
beta 987keV a gama 440 keV; z 213Po je to alfa 8,4MeV; z
209Pb je to beta 644keV .
Vedlejší větev 213Bi(a)®209Tl
vzhledem ke svému nízkému zastoupení (2,1%)
nemá v aplikacích větší význam.
Rozpadový řetězec 225-Ac funguje jako
"in vivo radionuklidový generátor"
- viz výše "In vivo generátory". Oproti thoriu-227 zde má 225Ac
výhodu v tom, že jeho rozpadový řetězec
neobsahuje dlouhodobější dceřinné
radionuklidy, takže je menší riziko
předčasného úniku radioaktivity z cílové
tkáně.
Zjednodušené přeměnové
schéma 225Ac na 221Fr a další rozpadový řetězec je
nakresleno níže v levé části obrázku.
Změřené spektrum
záření gama emitovaného všemi nuklidy z
celé rozpadové řady 225-Ac je zobrazeno níže
v pravé části obrázku.ę |
|
 |
Přeměnové
schéma aktinia 225Ac (první přeměna na
francium-221, zjednodušeně další řetězec) a celkové gama-spektrum 225Ac a jeho rozpadových produktů.
Ve spektru jsou obsaženy
gama-linie i všech dceřinných radionuklidů rozpadové
řady, s nimiž je 225Ac v radioaktivní rovnováze. V dolní části
obrázku je zvětšený výřez spektra
nízkoenergetické oblasti cca 50-230 keV, kde je velké
nahuštění gama a X píků.
Samotné aktinium-225 při své alfa-přeměně na 221-Fr
produkuje jen poměrně málo gama-záření (ve spektru
jsou vidět jen slabé píky 63, 100, 150, 188 keV).
Většina gama záření preparátů aktinia pochází z
dceřinných radionuklidů rozpadové řady, především
z 221Fr (218keV) a 213Bi (440keV). |
Při jedné úplné
radioaktivní přeměně jádra 225Ac v celé rozpadové řadě až na
stabilní 209Bi se uvolní celková jaderná energie Q = 31 MeV, která je z asi 95% odnášena čtyřmi
alfa-částicemi, ze 3% elektrony beta+neutriny a z asi
1% fotony *) gama a X-záření.
*) Toto zdánlivě malé procentuální
zastoupení fotonového záření je důsledkem energetického
přepočtu vzhledem k vysoenergetickým a-částicím. Absolutní
počet emitovaných fotonů gama a X je ve skutečnosti poměrně
vysoký, pro energie v rozmezí 60-450keV představuje
cca 96%! Nejvíce zastoupené X a gama-energie jsou: X 81(14%),
83(25%) a 95keV(8%), gama 154(5,8%), 269(14%), 351(13%) a
401keV(7%).
U aktinia 225Ac a dceřinných produktů rozpadové řady je
využíváno emitované alfa-záření o
energiích 5,8-8,4 MeV
(celkem 4 alfa-částice/1přeměnu
225Ac) v nukleární
medicíně pro biologicky cílenou
radionuklidovou terapii. Radiofarmaka značená 225Ac (včetně monoklonálních protilátek, např. 225Ac-Trastuzumab či 225Ac-PSMA-617) se zkoušejí pro terapii leukemie, lymfomů,
neuroendokrinních nádorů, gliomů, melanomů, velmi
přínosné jsou u ca prostaty - 225Ac značené anti-PSMA.
Záření gama
dceřinných nuklidů 225Ac se při terapii prakticky neuplatňuje, ale může
být využito pro gamagrafické monitorování
distribuce radiofarmaka v organismu. Emise gama záření,
především energie 218keV, umožňuje při terapii současné scintigrafické
zobrazení tkání a orgánů, kam terapeutický
preparát pronikl. Na těchto scintigrafických obrazech můžeme
posuzovat (vizuálně, příp. i
kvantitativně) míru žádoucího
vychytávání radiofarmaka v nádorových ložiscích a
nežádoucí akumulace ve zdravých tkáních a kritických
orgánech - provádět monitorování průběhu
radioisotopové terapie.
Příprava: Isotop 225Ac ve větším
množství je zatím obtížně dostupný. Lze jej získat jako
produkt radioaktivní alfa+beta přeměny thoria 229Th(a,T1/2=7340let)®225Ra(b-,T1/2=14,8dní)®225Ac - thorium-aktiniový 229Th/225Ac
generátor, z něhož se zatím menší množství
aktinia získávalo pro experimentální použití v nukleární
medicíně. Thorium-229 se získávalo z a-rozpadu uranu 233U, jehož zásoby
jsou však velmi omezené. Pro rutinní výrobu se aktinium-225
připravuje v cyklotronu ozařováním radia-226 protony (optimální energie 17MeV)
reakcí 226Ra(p,2n)225Ac.
Aktinium 227Ac
S poločasem 21,77 roků se přeměňuje
větveně beta--radioaktivitou
na 227Th
(98,6%) a alfa-radioaktivitou na 223Fr (1,4%), dále pak
rozpadovou řadou.... Vyrábí se ozařováním radia-226
neutrony v jaderném reaktoru: 226Ra(n,g)227Ra(b-,T1/2=41min.)®227Ac. Aktinium 227Ac se používá jako mateřský isotop pro generátorovou
přípravu výše popsaného thoria 227-Th a
radia 223-Ra .
Mezi
rozpadovými produkty thoria a uranu jsou i plynné
radioisotopy radonu :
 Radon Rn86 je nejtěžším prvkem ze skupiny vzácných plynů.
Je radioaktivní, nemá žádný stabilní isotop. V přírodě
se ve stopovém množství vyskytují tři isotopy radonu: 222Rn (T1/2=3,82 d.), 220Rn (T1/2=54,5 s.) a 219Rn (T1/2=3,92 s.). Pocházejí z
rozpadových řad uranu a thoria, konkrétně vznikají při
alfa-radioaktivitě isotopů radia. Rozpadají se na
příslušné isotopy polonia a dále rozpadovou řadou o 4-6
členech na stabilní isotopy olova. Původní název radonu byl radiová
emanace - vyvěrající z radia. A radon 220Rn se dříve
nazýval thoron (je součástí thoriové
rozpadové řady - obr.1.4.1 vlevo).
Radon Rn86 je nejtěžším prvkem ze skupiny vzácných plynů.
Je radioaktivní, nemá žádný stabilní isotop. V přírodě
se ve stopovém množství vyskytují tři isotopy radonu: 222Rn (T1/2=3,82 d.), 220Rn (T1/2=54,5 s.) a 219Rn (T1/2=3,92 s.). Pocházejí z
rozpadových řad uranu a thoria, konkrétně vznikají při
alfa-radioaktivitě isotopů radia. Rozpadají se na
příslušné isotopy polonia a dále rozpadovou řadou o 4-6
členech na stabilní isotopy olova. Původní název radonu byl radiová
emanace - vyvěrající z radia. A radon 220Rn se dříve
nazýval thoron (je součástí thoriové
rozpadové řady - obr.1.4.1 vlevo).
Radon 222Rn
Alfa-rozpadem radia-226 vzniká plynný radon 222Rn,
který se dále s poločasem 3,83 dní přeměňuje alfa-radioaktivitou
na polonium 218Po, v 99,92% na základní stav, v 0,08% na excitovanou
hladinu 510keV. Další radioaktivní přeměny pak probíhají
celou rozpadovou řadou podle pravé části obr.1.4.1. Gama-spektrum radonu-222 je téměř identické s
výše uvedeným spektrem 226Ra (až na linii 186keV).
Sekundární
přírodní radon-222 se svými rozpadovými produkty je
významný z hlediska radioekologie - viz kap.5, §5.2 "Biologické účinky ionizujícího záření", pasáž "Zdroje ozáření ionizujícím
zářením". Radony 220Rn v thoriové a 219Rn v uran-aktiniové
rozpadové řadě se vzhledem ke krátkému poločasu stačí
rozpadnout dříve, než difuzí uniknou z radioaktivního
materiálu, takže je v radioekologii není třeba uvažovat.
 Transurany
Transurany

Z uměle vyráběných nejtěžších
jader skupiny transuranů (prvků
těžších než uran - jsou podrobně rozebírány v §1.3,
část "Transurany") mají praktické
uplatnění především tři radionuklidy :
Plutonium 239Pu
Plutonium 239Pu se s poločasem T1/2=24100 let alfa-radioaktivitou
rozpadá na uran 235U (na excitované hladiny 51.7,
13.4 a 0.007 keV; gama-záření se zde však téměř neemituje,
neboť příslušné přechody téměř úplně podléhají
vnitřní konverzi, takže místo toho jsou emitovány konverzní
a Augerovy elektrony). Další přeměny
probíhají celou uran-aktiniovou rozpadovou řadou
(prostřední část obr.1.4.1). Plutonium-239 vzniká v
jaderném reaktoru neutronovou fúzí z uranu 238U: 238U(n,g)239U ®(b-;25min)® 239Np ®(b-;2,3dnů)® 239Pu. Je účinným štěpným
materiálem (podobně jako uran 235U). Vedle zneužití pro jaderné zbraně se využívá
ve speciálních jaderných reaktorech (§1.3,
část "Rychlé množivé
reaktory FBR").
Americium
241Am
Americium 241Am se s poločasem T1/2=458 let
rozpadá alfa-radioaktivitou na neptunium 237Np (a dále pak celou neptuniovou rozpadovou řadou - je
zobrazeno výše v pasáži "Aktinium 225Ac", na schématu vlevo nahoře).
Alfa-rozpad 241Am probíhá především (v 84,6%) na excitovanou
hladinu 59,6keV neptunia, která při deexcitaci na základní
stav emituje záření gama 59,6 keV,
slabě zastoupeno je gama 23,6keV. V důsledku vnitřní konverze
je dále emitováno charakteristické X-záření
La,b neptunia 11-22keV. Velké množství dalších
excitovaných hladin 237Np (33, 75-1014 keV) je syceno s nepatrnou intenzitou a pro radiaci 241Am nemá žádný
význam. 241-americium je tedy smíšeným a+g
zářičem: Ea=5485keV, Eg=59,6keV. Vzhledem k velmi dlouhému poločasu
dceřinného 237Np je radiace dalších členů rozpadové řady
zanedbatelně nízká ve srovnání s americiem.
Isotop
241Am
vzniká v jaderném reaktoru z plutonia neutronovou fúzí v
reakcích 239Pu(n,g)240Pu(n,g)241Pu®(b-)®241Am.
Americium-241
se často používá jako etalon
měkkého záření gama 59,6keV, jako zdroj a-částic
např. v ionizačních požárních hlásičích, ve směsi s
beryliem za využití reakce (a,n) jako laboratorní zdroj neutronů (§1.6, část "Neutronové záření a jeho interakce").
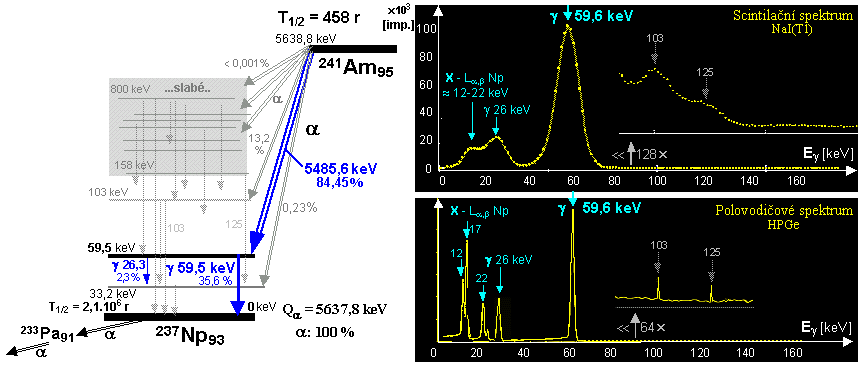
Rozpadové schéma a gama-spektrum americia 241Am
Kalifornium 252Cf
je nejtěžším radionuklidem, který má ještě praktické
uplatnění. Kalifornium 252Cf (T1/2=2,65 roku)
se kromě a-radioaktivity (97%) na 248Cm rozpadá i spontánním
štěpením (3%) *), při němž jsou emitovány neutrony
(cca 3,7 neutronů/1štěpení) - využívá se proto jako intenzívní neutronový
zdroj, např. pro neutronovou aktivační analýzu
a pro neutronovou záchytovou radioterapii (kap.3.6.,
pasáž "NeutronTerapie"). Kalifornium-252 vzniká v
jaderném reaktoru z plutonia 239Pu postupným několikanásobným neutronovým
záchytem, kombinovaným s beta--přeměnami.
*) Pozn.: Z
hlediska produkce neutronů by byl snad ještě zajímavější
isotop 254Cf,
který se spontánním štěpením rozpadá dokonce v 99%
případů; jeho nevýhodou je však obtížnější příprava a
kratší poločas T1/2=60,5dne.
Transurany se radioaktivně
rozpadají celými rozpadovými řadami (podobně jako uran a thorium - viz výše obr.1.4.1), kde jednotlivé dceřinné
produkty vykazují alfa i beta radioaktivitu a excitovaná jádra
emitují záření gama. Konečným produktem jsou stabilní
isotopy olova nebo vizmutu (odhlédneme-li
od zcela nepatrné radioaktivity 209Bi s poločasem 1,9.1019let).
Níže uvádíme velmi
stručnou tabulku některých nejdůležitějších
radionuklidů, která slouží jen pro ilustraci teoretického
rozboru radioaktivity v §1.2 a
vlastností radionuklidů v tomto §1.4. Úplný a podrobný
přehled radionuklidů, s rozpadovými schématy a uvedením
všech jejich charakteristik, je možno nalézt např. ve
vynikající "Table of isotopes"
autorů Lederer, Hollander, Perlman (nová elektronická verze http://ie.lbl.gov/toipdf/toi20.pdf ).
Tabulka
nejčastěji používaných radionuklidů
| Radionuklid |
Poločas T1/2 |
Způsob
rozpadu |
Energie[keV]
Ea nebo Ebmax |
Energie[keV]
gama Eg |
Nejčastější
způsob výroby |
Použití |
| 1n 0 |
13 min |
b- |
782 |
- |
reaktor 235U,
(a,n) |
jaderná
analýza |
| 3H1 |
12,3 roku |
b- |
18,6 |
- |
6Li(n,a)3H |
biologie |
| 14C6 |
5730 roků |
b- |
156 |
- |
14N(n,p)14C |
biologie
analýza |
| 18F9 |
110 min. |
b+(97%)
EC (3%) |
633 |
511 (194%)
(anihilace) |
18O(p,n)18F |
nukleární
medicína |
| 32P15 |
14,3 dne |
b- |
1710 |
- |
32S(n,p)32P |
nukleární
medicína |
| 40K 19 |
1,28 . 109
roků |
b- (89%)
EC (11%) |
1314 |
1460 (11%) |
přírodní
radionuklid |
isotop.
datování |
| 51Cr 24 |
27,7 dne |
EC |
- |
320 (9,8%) |
50Cr(n,g)51Cr |
nukleární
medicína |
| 57Co27 |
271 dnů |
EC |
- |
14 (9%)
122 (86%)
136 (11%)
692 (0,15%) |
56Fe(d,n)57Co
56Fe(p,g)57Co
55Mn(a,2n)57Co |
zdroj
gama |
| 58Co27 |
70,8 dne |
b+, EC |
- |
511 (30%)
810 (99%)
865 (1,5%)
1670 (0,6%) |
55Mn(a,n)58Co |
biologie,
nukleární
medicína |
| 60Co27 |
5,271 roků |
b- |
310 (99,88%)
1480 (0,12%) |
1173 (100%)
1332 (100%) |
59Co(n,g)60Co |
zdroj
gama |
| 67Ga31 |
3,26 dne |
EC |
- |
93 (40%)
184 (20%)
300 (17%)
393 (5%) |
68Zn(p,2n)67Ga |
nukleární
medicína |
| 68Ga31 |
68 min. |
b+(89%)
EC (11%) |
|
511 (178%)
(anihilace) |
68Zn(p,n)68Ga |
nukleární
medicína |
81Rb37
ęęęę |
4,6 hod.
ęęę |
EC
ęęę |
- |
190 (66%)
446 (19%)
|
79Br(a,2n)81Rb
|
generátor
81mKr
ęęę |
| 81mKr36 |
13 sec. |
IT |
- |
190 (67%) |
81Rb®81mKr |
scintigrafie
plic |
| 90Sr38 |
28,8 let |
b- |
546 |
- |
235U(n,f)90Sr |
|
| 90Y39 |
64 hod. |
b- |
2280 |
- |
90Sr®90Y
89Y(n,g)90Y |
nukleární
medicína |
99Mo42
ęęęę |
66 hod.
ęęę |
b-
ęęę |
436 (17%)
1214 (83%) |
140 (6%)
181 (7%)
740 (13%)
778 (5%) |
98Mo(n,g)99Mo
235U(n,f)99Mo
|
generátor
99mTc
ęęę |
| 99mTc 43 |
6 hod. |
IT |
- |
140 (90%) |
99Mo®99mTc |
scintigrafie |
| 111In 49 |
2,8 dne |
EC |
- |
171 (90%)
245 (94%) |
111Cd(p,n)111In |
nukleární
medicína |
| 123I 53 |
13,2 hod. |
EC |
- |
Ka 27 (71%)
Kb 31 (16%)
159 (83%) |
121Sb(a,2n)123I |
nukleární
medicína |
| 125I 53 |
60 dní |
EC |
- |
Ka 27 (112%)
Kb 31 (25%)
35 (6,5%) |
124Xe(n,g)125Xe
âEC
125I |
nukleární
medicína
(RIA) |
| 131I 53 |
8,04 dne |
b- |
334 (7,5%)
606 (90%) |
80 (2,5%)
284 (6%)
364 (81%)
637 (7%)
723 (2%) |
130Te(n,g)131Te
235U(n,f)131Te
b-(25min):
131Te®131J |
nukleární
medicína |
| 133Xe 54 |
5,3 dne |
b- |
346 |
Ka 31 (39%)
Kb 35 (9%)
81 (37%) |
235U(n,f)133Xe |
nukleární
medicína |
| 137Cs 53 |
30 roků |
b- |
1176 |
Ka 32 (6%)
Kb 36
(1,5%)
g 662
(85%) |
235U(n,f)137Cs |
zdroj
gama |
| |
|
|
|
|
|
|
| |
|
|
|
|
|
|
| |
|
|
|
|
|
|
| |
|
|
|
|
|
|
| |
|
|
|
|
|
|
| 192Ir 77 |
74,2 dne |
b-(95%)
EC(5%) |
240 (8%)
536 (41%)
672 (46%) |
296 (29%)
308 (30%)
317 (81%)
468 (49%)
604 (9%)
612 (6%) |
191Ir(n,g)192Ir
192Os(d,2n)192Ir |
zdroj
gama |
| 201Tl 81 |
73 hod. |
EC |
- |
Ka 70 (74%)
Kb 80 (21%)
135 (2,6%)
167 (9%) |
203Tl(p,3n)201Pb
âEC
201Tl |
nukleární
medicína |
| |
|
|
|
|
|
|
| 226Ra 88 |
1602
roků |
a |
4782 |
186 (4%) |
přírodní
radionuklid |
zdroj
alfa |
| 232Th 90 |
1,41 . 1010
roků |
a |
4011 |
|
přírodní
radionuklid |
potenciální
jaderné
palivo |
| 235U 92 |
7,1 . 108
roků |
a |
4580 |
143 (11%)
185 (54%)
204 (5%)
|
přírodní
radionuklid |
štěpný
materiál |
| 238U 92 |
4,51 . 109
roků |
a |
4195 |
|
přírodní
radionuklid |
jaderný
reaktor |
| 239Pu 94 |
2,44 . 104
roků |
a |
5160 |
|
238U(n,g)239U
®(b-) 239Np3
®(b-® 239Pu |
štěpný
materiál |
| 241Am 95 |
458 roků |
a |
5486 |
La 13,9 (14%)
Lb 17,8
(20%)
Lg 20,8 ( 5%)
g 26,4
( 3%)
g 59,6
(36%) |
239Pu(n,g)240Pu
(n,g)241Pu
âb-
241Am |
zdroj
alfa
a
gama |
| 252Cf 98 |
2,65 roku |
a (97%)
spont.
štěpení
(3%)
® n |
a:
6119 (97%)
+
štěpné fragm.
+
neutrony |
- |
238U, 239Pu
(n,g),(n,g),....
...,(n,g),..b-...
â
252Cf |
zdroj
neutronů |
Pozn.: Barevným
pozadím jsou označeny dvojice mateřský®dceřinný radionuklid používané v
generátorech.
Vojtěch Ullmann































































